この記事 きじ 検証 けんしょう 可能 かのう 参考 さんこう 文献 ぶんけん 出典 しゅってん 全 まった 示 しめ 不十分 ふじゅうぶん 出典 しゅってん 追加 ついか 記事 きじ 信頼 しんらい 性 せい 向上 こうじょう 協力 きょうりょく (このテンプレートの使 つか 方 かた ) 出典 しゅってん 検索 けんさく ? "ペプチド結合 けつごう – ニュース · 書籍 しょせき · スカラー · CiNii · J-STAGE · NDL · dlib.jp · ジャパンサーチ · TWL (2011年 ねん
ペプチド結合 けつごう 円 えん 内 ない ペプチド結合 けつごう (ペプチドけつごう、英 えい peptide bond )とは、アミド結合 けつごう のうちα あるふぁ アミノ酸 あみのさん 同士 どうし 脱水 だっすい 縮 ちぢみ 合 あい 形成 けいせい 共有 きょうゆう 結合 けつごう [1] 分類 ぶんるい 上 じょう 級 きゅう 分類 ぶんるい タンパク質 たんぱくしつ 中 ちゅう α あるふぁ アミノ酸 あみのさん 連続 れんぞく 場合 ばあい 結合 けつごう 呼 よ 単 たん 結合 けつごう 呼 よ
このようにして生成 せいせい 物質 ぶっしつ ペプチド と呼 よ 縮 ちぢみ 合 あわ アミノ酸 あみのさん 数 かず 多数 たすう アミノ酸 あみのさん 縮 ちぢみ 合 あわ 高分子 こうぶんし 物質 ぶっしつ タンパク質 たんぱくしつ タンパク質 たんぱくしつ ポリペプチド とも呼 よ
アミド結合 けつごう 強固 きょうこ 結合 けつごう 加水 かすい 分解 ぶんかい 強 つよ 酸性 さんせい 強 つよ アルカリ性 あるかりせい 条件 じょうけん 起 お 生体 せいたい 内 ない 結合 けつごう 選択 せんたく 的 てき 加水 かすい 分解 ぶんかい 酵素 こうそ プロテアーゼ が存在 そんざい 中 なか 中性 ちゅうせい 近 ちか 生物 せいぶつ 体温 たいおん 程度 ていど 温度 おんど 迅速 じんそく 結合 けつごう 加水 かすい 分解 ぶんかい
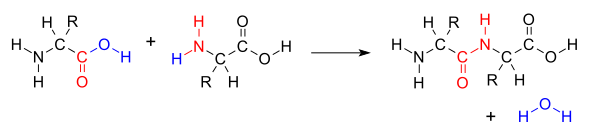
脱水 だっすい 反応 はんのう 結合 けつごう 形成 けいせい 2つのアミノ酸 あみのさん 結合 けつごう 介 かい ジペプチド 形成 けいせい 場合 ばあい [1] 縮 ちぢみ 合 あい 反応 はんのう 一種 いっしゅ [2] 種 たね 縮 ちぢみ 合 あい アミノ酸 あみのさん 互 たが 接近 せっきん 一方 いっぽう 非 ひ 側 がわ 鎖 くさり カルボン酸 さん 部分 ぶぶん 他方 たほう 非 ひ 側 がわ 鎖 くさり アミノ 部分 ぶぶん 接近 せっきん 一方 いっぽう 基 もと 水素 すいそ 酸素 さんそ 失 うしな 一方 いっぽう 基 もと NH2 )から水素 すいそ 失 うしな 反応 はんのう 分子 ぶんし 水 みず H2 O )とペプチド結合 けつごう -CO-NH- )で結合 けつごう アミノ酸 あみのさん 生成 せいせい アミノ酸 あみのさん 結合 けつごう 呼 よ
アミド結合 けつごう 脱水 だっすい 合成 ごうせい 反応 はんのう 一方 いっぽう アミノ酸 あみのさん 分子 ぶんし カルボキシル基 もと と他方 たほう アミノ酸 あみのさん 分子 ぶんし アミノ基 もと が反応 はんのう 分子 ぶんし 水 みず H2 O )が放出 ほうしゅつ 合成 ごうせい 行 おこな
2つのアミノ酸 あみのさん 脱水 だっすい 縮 ちぢみ 合 あわ 結合 けつごう 赤 あか 形成 けいせい 水 みず 青 あお 排出 はいしゅつ ペプチド結合 けつごう 形成 けいせい 必要 ひつよう 生物 せいぶつ 場合 ばあい ATP が使 つか [3] タンパク質 たんぱくしつ アミノ酸 あみのさん 結合 けつごう イソペプチド結合 けつごう の場合 ばあい 結合 けつごう 鎖 くさり 生物 せいぶつ 酵素 こうそ 使 つか 非 ひ 作 つく [4] リボソーム は脱水 だっすい 合成 ごうせい 細部 さいぶ 異 こと 反応 はんのう 使 つか タンパク質 たんぱくしつ 作 つく [5]
α あるふぁ 作 つく 呼 よ [6] 多 おお 特殊 とくしゅ 酵素 こうそ 合成 ごうせい 非 ひ 呼 よ グルタチオン は、遊離 ゆうり アミノ酸 あみのさん 酵素 こうそ グルタミン酸 ぐるたみんさん (英語 えいご 版 ばん 結合 けつごう 結合 けつごう 形成 けいせい グルタチオン合成 ごうせい 酵素 こうそ (ペプチド結合 けつごう 形成 けいせい 段階 だんかい 合成 ごうせい [7] [8]
ペプチド結合 けつごう 加水 かすい 分解 ぶんかい 水 みず 添加 てんか 切断 せつだん 可能 かのう 性 せい 水 みず 存在 そんざい 下 か 分解 ぶんかい kJ /mol (2~4 kcal /mol)のギブスエネルギー を放出 ほうしゅつ [9] 非常 ひじょう 遅 おそ 半減 はんげん 期 き 結合 けつごう 年 ねん [10]
生体 せいたい 内 ない 通常 つうじょう プロテアーゼ としても知 し 酵素 こうそ 触媒 しょくばい タンパク質 たんぱくしつ 天然 てんねん 構造 こうぞう フォールド (折 お 際 さい 立体 りったい 配 はい 座 ざ 的 てき 歪 ゆが 結合 けつごう 加水 かすい 分解 ぶんかい 報告 ほうこく [11] 非 ひ 酵素 こうそ 的 てき 遷移 せんい 状態 じょうたい 安定 あんてい 化 か 基底 きてい 状態 じょうたい 不安定 ふあんてい 化 か 促進 そくしん
ペプチド結合 けつごう 吸収 きゅうしゅう 波長 はちょう [12] 特 とく 紫外線 しがいせん 影響 えいきょう 受 う
窒素 ちっそ 原子 げんし 上 じょう 孤立 こりつ 電子 でんし 対 たい 大 おお 非 ひ 局在 きょくざい 化 か 基 もと 部分 ぶぶん 二 に 重 じゅう 結合 けつごう (英語 えいご 版 ばん 特性 とくせい 持 も 部分 ぶぶん 二 に 重 じゅう 結合 けつごう 基 もと 平面 へいめん 的 てき シス型 がた またはトランス型 がた 異性 いせい 体 たい が存在 そんざい タンパク質 たんぱくしつ 展開 てんかい 状態 じょうたい 基 もと 自由 じゆう 異性 いせい 化 か 両方 りょうほう 異性 いせい 体 たい 採用 さいよう 状態 じょうたい 各 かく 位置 いち 単一 たんいつ 異性 いせい 体 たい 採用 さいよう 例外 れいがい 除 のぞ 結合 けつごう 型 がた 圧倒的 あっとうてき 好 この 型 がた 型 がた 比 ひ 約 やく 群 ぐん 比率 ひりつ 約 やく 割合 わりあい 存在 そんざい 傾向 けいこう プロリン (Pro)の
C
α あるふぁ
{\displaystyle \mathrm {C^{\alpha }} }
原子 げんし
C
δ でるた
{\displaystyle \mathrm {C^{\delta }} }
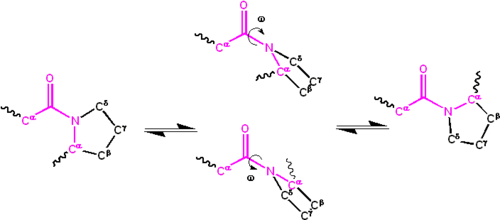
原子 げんし 間 あいだ 対称 たいしょう 性 せい 型 がた 型 がた 異性 いせい 体 たい 等 ひと 考 かんが 下図 したず 参照 さんしょう
X-Proペプチド結合 けつごう 異性 いせい 化 か 異性 いせい 体 たい 左端 ひだりはし 右 みぎ 端 はし 遷移 せんい 状態 じょうたい 区切 くぎ ペプチド基 もと
C
α あるふぁ
−
C
′
−
N
−
C
α あるふぁ
{\displaystyle C^{\alpha }-C^{\prime }-N-C^{\alpha }}
原子 げんし 定義 ていぎ 関連 かんれん 二 に 面 めん 角 かく
ω おめが
{\displaystyle \omega }
型 がた 異性 いせい 体 たい シンペリプラナー 配 はい 座 ざ
ω おめが =
0
∘
{\displaystyle \omega =0^{\circ }}
型 がた 異性 いせい 体 たい アンチペリプラナー 配 はい 座 ざ
ω おめが =
180
∘
{\displaystyle \omega =180^{\circ }}
基 もと 型 がた 型 がた 間 あいだ 結合 けつごう 中心 ちゅうしん 異性 いせい 化 か 室温 しつおん
τ たう ∼
{\displaystyle \tau \sim }
秒 びょう 遷移 せんい 状態 じょうたい
ω おめが =
±
90
∘
{\displaystyle \omega =\pm 90^{\circ }}
部分 ぶぶん 二 に 重 じゅう 結合 けつごう 切断 せつだん 必要 ひつよう 活性 かっせい 化 か 約 やく 基 もと 疎水 そすい 性 せい 環境 かんきょう 配置 はいち 基 もと 窒素 ちっそ 原子 げんし 水素 すいそ 結合 けつごう 供与 きょうよ 単 たん 結合 けつごう 型 がた 有利 ゆうり 変化 へんか 与 あた 活性 かっせい 化 か 下 さ 異性 いせい 化 か 触媒 しょくばい 活性 かっせい 化 か 低下 ていか 結合 けつごう 異性 いせい 化 か 触媒 しょくばい 天然 てんねん 酵素 こうそ ペプチジルプロリルイソメラーゼ (PPIases)にも見 み
立体 りったい 配 はい 座 ざ タンパク質 たんぱくしつ 通常 つうじょう 異性 いせい 化 か 秒 びょう 速 はや 通常 つうじょう 秒 びょう 基 もと 非 ひ 天然 てんねん 異性 いせい 体 たい 立体 りったい 配 はい 座 ざ 大 おお 混乱 こんらん 天然 てんねん 異性 いせい 体 たい 到達 とうたつ 遅 おく 妨 さまた 基 もと 同 おな 影響 えいきょう 与 あた 他 た 基 もと 非 ひ 天然 てんねん 異性 いせい 体 たい 全 まった 影響 えいきょう 与 あた
ペプチド結合 けつごう 共鳴 きょうめい 安定 あんてい 化 か 生理学 せいりがく 的 てき 条件下 じょうけんか 比較的 ひかくてき 反応 はんのう 性 せい 低 ひく エステル などの類似 るいじ 化合 かごう 物 ぶつ 少 すく 結合 けつごう 化学 かがく 反応 はんのう 起 お カルボニル 炭素 たんそ 電気 でんき 陰性 いんせい 原子 げんし 攻撃 こうげき 二 に 重 じゅう 結合 けつごう 切断 せつだん 四 よん 面体 めんてい 中間 なかま 体 たい 形成 けいせい 可能 かのう 性 せい タンパク質 たんぱくしつ 分解 ぶんかい 一般 いっぱん 的 てき インテイン のようなN-Oアシル交換 こうかん 反応 はんのう 経路 けいろ 結合 けつごう 攻撃 こうげき 官能 かんのう 基 もと チオール 、ヒドロキシル またはアミン である場合 ばあい 得 え 分子 ぶんし シクロール と呼 よ 具体 ぐたい 的 てき 呼 よ
^ a b “Nomenclature and Symbolism for Amino Acids and Peptides. Recommendations 1983”. European Journal of Biochemistry 138 (1): 9-37. (1984). doi :10.1111/j.1432-1033.1984.tb07877.x . ISSN 0014-2956 . PMID 6692818 .
^ Muller, P (1994-01-01). “Glossary of terms used in physical organic chemistry (IUPAC Recommendations 1994)”. Pure and Applied Chemistry 66 (5): 1077-1184. doi :10.1351/pac199466051077 . ISSN 1365-3075 . ^ Watson, James; Hopkins, Nancy; Roberts, Jeffrey; Agetsinger Steitz, Joan; Weiner, Alan (1987). Molecualar Biology of the Gene 168 . ISBN 978-0805396140 . https://archive.org/details/molecularbiology0004unse/page/168 ^ Miller BR, Gulick AM (2016). “Structural Biology of Nonribosomal Peptide Synthetases” . Methods in Molecular Biology 1401 : 3-29. doi :10.1007/978-1-4939-3375-4_1 . ISBN 978-1-4939-3373-0 . PMC 4760355 . PMID 26831698 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4760355/ . ^ Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart WM (2000). Protein synthesis ISBN 978-0716735205 . https://www.ncbi.nlm.nih.gov/books/NBK22022/ ^ Walton JD, Hallen-Adams HE, Luo H (2010). “Ribosomal biosynthesis of the cyclic peptide toxins of Amanita mushrooms” . Biopolymers 94 (5): 659-664. doi :10.1002/bip.21416 . PMC 4001729 . PMID 20564017 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4001729/ . ^ Wu G, Fang YZ, Yang S, Lupton JR, Turner ND (March 2004). “Glutathione metabolism and its implications for health”. The Journal of Nutrition 134 (3): 489-492. doi :10.1093/jn/134.3.489 . PMID 14988435 . ^ Meister A (November 1988). “Glutathione metabolism and its selective modification” . The Journal of Biological Chemistry 263 (33): 17205-17208. PMID 3053703 . http://www.jbc.org/cgi/pmidlookup?view=long&pmid=3053703 . ^ Martin RB (December 1998). “Free energies and equilibria of peptide bond hydrolysis and formation” . Biopolymers 45 (5): 351-353. doi :10.1002/(SICI)1097-0282(19980415)45:5<351::AID-BIP3>3.0.CO;2-K . https://doi.org/10.1002/(SICI)1097-0282(19980415)45:5%3C351::AID-BIP3%3E3.0.CO;2-K . ^ Radzicka, Anna; Wolfenden, Richard (1996-01-01). “Rates of Uncatalyzed Peptide Bond Hydrolysis in Neutral Solution and the Transition State Affinities of Proteases”. Journal of the American Chemical Society 118 (26): 6105-6109. doi :10.1021/ja954077c . ISSN 0002-7863 . ^ Sandberg A, Johansson DG, Macao B, Härd T (April 2008). “SEA domain autoproteolysis accelerated by conformational strain: energetic aspects”. Journal of Molecular Biology 377 (4): 1117-1129. doi :10.1016/j.jmb.2008.01.051 . PMID 18308334 . ^ Goldfarb AR, Saidel LJ, Mosovich E (November 1951). “The ultraviolet absorption spectra of proteins” . The Journal of Biological Chemistry 193 (1): 397-404. PMID 14907727 . http://www.jbc.org/content/193/1/397.long .