水酸化 すいさんか 塩基 えんき 性 せい 無機 むき 化合 かごう 物 ぶつ バリウム の水酸化物 すいさんかぶつ 化学 かがく 式 しき Ba(OH)2 で表 あらわ 水酸化物 すいさんかぶつ イオン結晶 けっしょう であり、粒状 りゅうじょう 粉末 ふんまつ 状 じょう 外観 がいかん 持 も 最 もっと 一般 いっぱん 的 てき 形 かたち 水 みず 和物 あえもの 市販 しはん 一般 いっぱん 水溶 すいよう 性 せい 化合 かごう 物 ぶつ 同様 どうよう 毒性 どくせい 強 つよ 劇 げき 物 ぶつ 指定 してい
バリタ (baryta) とも呼 よ 飽和 ほうわ 水溶液 すいようえき バリタ水 すい )は水酸化 すいさんか 同様 どうよう 二酸化炭素 にさんかたんそ 吹 ふ 込 こ 炭酸 たんさん 析出 せきしゅつ 白 しろ 濁 にご 知 し
酸化 さんか 水 みず 溶解 ようかい 生成 せいせい 再 さい 結晶 けっしょう 水 みず 和物 あえもの 得 え 空気 くうき 中 ちゅう 加熱 かねつ 水 みず 和物 あえもの 減圧 げんあつ 下 か 加熱 かねつ 無水 むすい 物 ぶつ 得 え [1] 水 みず 和 わ 反応 はんのう 生石灰 せいせっかい 消 しょう 和 わ 激 はげ 危険 きけん 伴 ともな
BaO
+
H
2
O
⟶
Ba
(
OH
)
2
{\displaystyle {\ce {BaO + H2O -> Ba(OH)2}}}
Δ でるた
H
∘
=
−
105.4
kJ mol
−
1
{\displaystyle \Delta H^{\circ }=-105.4{\mbox{kJ mol}}^{-1}}
化学 かがく 的 てき 性質 せいしつ [ 編集 へんしゅう ] 水酸化 すいさんか 脱水 だっすい 対 たい 安定 あんてい 無 む 水物 みずもの 熔融 ようゆう 加熱 かねつ 脱水 だっすい 始 はじ 水蒸気 すいじょうき 解離 かいり 圧 あつ 気圧 きあつ 達 たっ
Ba
(
OH
)
2
→
Δ でるた
BaO
+
H
2
O
{\displaystyle {\ce {Ba(OH)2 \ ->[\Delta] \ {BaO}+ H2O}}}
無 む 水物 みずもの 水 みず 対 たい 溶解 ようかい 熱 ねつ 発熱 はつねつ 的 てき [2]
Ba
(
OH
)
2
(
s
)
↽
−
−
⇀
Ba
2
+
(
aq
)
+
2
OH
−
(
aq
)
{\displaystyle {\ce {Ba(OH)2(s)\ <=>\ {Ba^{2+}(aq)}+2OH^{-}(aq)}}}
Δ でるた
H
∘
=
−
52.93
kJ mol
−
1
{\displaystyle \Delta H^{\circ }=-52.93{\mbox{kJ mol}}^{-1}}
しかし、78℃以下 いか 水溶液 すいようえき 析出 せきしゅつ 固 かた 相 しょう 八 はち 水 みず 和物 あえもの 八 はち 水 みず 和物 あえもの 溶解 ようかい 熱 ねつ 著 いちじる 的 てき 溶解 ようかい 度 ど 温度 おんど 上昇 じょうしょう 伴 とも 著 いちじる 増大 ぞうだい
Ba
(
OH
)
2
⋅
8
H
2
O
(
s
)
↽
−
−
⇀
Ba
2
+
(
aq
)
+
2
OH
−
(
aq
)
+
8
H
2
O
(
l
)
{\displaystyle {\ce {Ba(OH)2\cdot 8H2O(s)\ <=>\ {Ba^{2+}(aq)}+{2OH^{-}(aq)}+8H2O(l)}}}
Δ でるた
H
∘
=
57.93
kJ mol
−
1
{\displaystyle \Delta H^{\circ }=57.93{\mbox{kJ mol}}^{-1}}
0.05mol/dm3 (0.1N )の水溶液 すいようえき 電離 でんり 度 ど 約 やく 強 つよ 塩基 えんき 分類 ぶんるい 水酸化 すいさんか 溶解 ようかい 度 ど 高 たか 塩基 えんき 作用 さよう 強 つよ 水酸化 すいさんか 酸 さん 中和 ちゅうわ 塩 しお 水溶液 すいようえき 加水 かすい 分解 ぶんかい 無視 むし 得 え 水 みず 和 わ 酸 さん 解離 かいり 定数 ていすう pK a )は以下 いか 通 とお
Ba
2
+
(
aq
)
+
H
2
O
(
l
)
↽
−
−
⇀
H
+
(
aq
)
+
BaOH
+
(
aq
)
{\displaystyle {\ce {{Ba^{2+}(aq)}+H2O(l)\ <=>\ {H^{+}(aq)}+BaOH^{+}(aq)}}}
p
K
a
=
13.4
{\displaystyle {\mbox{p}}K_{a}=13.4\,}
従 したが 水酸化 すいさんか 第 だい 二 に 段階 だんかい 塩基 えんき 解離 かいり 定数 ていすう 以下 いか
BaOH
+
(
aq
)
↽
−
−
⇀
Ba
2
+
(
aq
)
+
OH
−
(
aq
)
{\displaystyle {\ce {{BaOH^{+}(aq)}\ <=>\ {Ba^{2+}(aq)}+OH^{-}(aq)}}}
p
K
b
2
=
0.6
{\displaystyle {\mbox{p}}K_{b2}=0.6\,}
分析 ぶんせき 化学 かがく 弱酸 じゃくさん 特 とく 有機 ゆうき 酸 さん 滴 しずく 定 じょう 用 もち 水酸化 すいさんか 水溶液 すいようえき 透明 とうめい 炭酸 たんさん 塩 しお 含 ふく 示 しめ 水酸化 すいさんか 水酸化 すいさんか 見 み 特徴 とくちょう 炭酸 たんさん 水 みず 不溶 ふよう 性質 せいしつ 利用 りよう アルカリ性 あるかりせい 変色 へんしょく フェノールフタレイン やチモールフタレイン を指示 しじ 薬 やく 使 つか 際 さい 弱 じゃく 塩基 えんき 炭酸 たんさん 存在 そんざい 終点 しゅうてん 誤差 ごさ 出 だ 滴 しずく 定 じょう 行 おこな [3]
有機 ゆうき 合成 ごうせい 強 つよ 塩基 えんき [4] [5] [6] [7] 加水 かすい 分解 ぶんかい 用 もち
酸性 さんせい 物質 ぶっしつ 際 さい 中和 ちゅうわ 危険 きけん 性 せい 減 へ 目的 もくてき 使 つか
ウンデカンカルボン酸 さん 基 もと 片方 かたがた 加水 かすい 分解 ぶんかい 反応 はんのう 用 もち [8]
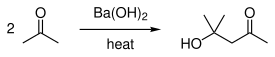
また、シクロペンタノン [9] ジアセトンアルコール (4-ヒドロキシ-4-メチル-2-ペンタノン)[10] D -グロン酸 さん γ がんま [11] 合成 ごうせい 用 もち
他 た 強 つよ 塩基 えんき 水溶 すいよう 性 せい 化合 かごう 物 ぶつ 同様 どうよう 注意 ちゅうい 要 よう 腐食 ふしょく 性 せい 有毒 ゆうどく
日本 にっぽん 毒物 どくぶつ 及 およ 劇 げき 物 ぶつ 取締 とりしまり 法 ほう 毒物 どくぶつ 及 およ 劇 げき 物 ぶつ 指定 してい 令 れい バリウム化合 かごう 物 ぶつ として劇 げき 物 ぶつ 指定 してい 他 た 消防 しょうぼう 法 ほう 労働 ろうどう 安全 あんぜん 衛生 えいせい 法 ほう 大気 たいき 汚染 おせん 防止 ぼうし 法 ほう 船舶 せんぱく 安全 あんぜん 法 ほう 航空 こうくう 法 ほう PRTR法 ほう にも規定 きてい
参考 さんこう 項目 こうもく
^ (1960). Gmelins Handbuch der anorganischen Chemie , 8. Aufl.; Verlag Chemie: Weinheim, p. 289.
^ D.D. Wagman, W.H. Evans, V.B. Parker, R.H. Schumm, I. Halow, S.M. Bailey, K.L. Churney, R.I. Nuttal, K.L. Churney and R.I. Nuttal, The NBS tables of chemical thermodynamics properties, J. Phys. Chem . Ref. Data 11 Suppl. 2 (1982).
^ Mendham, J.; Denney, R. C.; Barnes, J. D.; Thomas, M. J. K.; Denney, R. C.; Thomas, M. J. K. Vogel's Quantitative Chemical Analysis , 6th ed.; Prentice Hall: New York. ISBN 0-582-22628-7 .
^ Meyer, K.; Bloch, H. S. (1945). "Naphthoresorcinol" . Organic Syntheses 英語 えいご 25 : 73. Collective Volume , vol. 3, p. 637^ Brown, G. B. (1946). "Methylsuccinic acid" . Organic Syntheses 英語 えいご 26 : 54. Collective Volume , vol. 3, p. 615^ Ford, J. H. (1947). "β べーた . Organic Syntheses 英語 えいご 27 : 1. Collective Volume , vol. 3, p. 34^ Anslow, W. K.; King, H.; Orten, J. M.; Hill, R. M. (1925). "Glycine" . Organic Syntheses 英語 えいご 4 : 31. Collective Volume , vol. 1, p. 298^ Durham, L. J.; McLeod, D. J.; Cason, J. (1958). "Methyl hydrogen hendecanedioate" . Organic Syntheses 英語 えいご 38 : 55. Collective Volume , vol. 4, p. 635^ Thorpe, J. F.; Kon, G. A. R. (1925). "Cyclopentanone" . Organic Syntheses 英語 えいご 5 : 37. Collective Volume , vol. 1, p. 192^ Conant, J. B.; Tuttle, N. (1921). "Diacetone alcohol" . Organic Syntheses 英語 えいご 1 : 45. Collective Volume , vol. 1, p. 199^ Karabinos, J. V. (1956). "D -Gulonic γ がんま . Organic Syntheses 英語 えいご 36 : 38. Collective Volume , vol. 4, p. 506
参考 さんこう 項目 こうもく





![{\displaystyle {\ce {Ba(OH)2 \ ->[\Delta] \ {BaO}+ H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5047c829bb9892b2c1e332d593cdad3789928426)