膜 貫通 型 タンパク質

分類 [編集 ]
構造 による分類 [編集 ]
トポロジーによる分類 [編集 ]
この
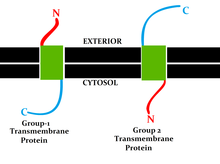
3次元 構造 [編集 ]

熱 力学 的 安定 性 とフォールディング[編集 ]
α ヘリックス膜 貫通 型 タンパク質 の安定 性 [編集 ]
また、アンフォールド
α ヘリックス膜 貫通 型 タンパク質 のフォールディング[編集 ]
β バレル膜 貫通 型 タンパク質 の安定 性 とフォールディング[編集 ]
3次元 構造 [編集 ]
光 吸収 駆動 型 トランスポーター[編集 ]
酸化 還元 駆動 型 トランスポーター[編集 ]
膜 貫通 型 シトクロムb様 タンパク質 : ユビキノール-シトクロムcレダクターゼ (シトクロムbc1複 合体 ); シトクロムb6f複 合体 ;ギ酸 脱水 素 酵素 、呼吸 性 硝酸 レダクターゼ; コハク酸 デヒドロゲナーゼ(フマル酸 還元 酵素 )。電子 伝達 系 を参照 のこと。細菌 およびミトコンドリアからのシトクロームcオキシダーゼ
電気 化学 的 電 駆動 型 トランスポーター[編集 ]
- プロトン
輸送 またはナトリウム輸送 F型 およびV型 ATPアーゼ
P-P結合 加水 分解 駆動 型 トランスポーター[編集 ]
- P
型 カルシウムATPアーゼ (5種類 の異 なるコンホメーション) - カルシウムATPアーゼ
調節 因子 ホスホランバンとサルコリピン - ABCトランスポーター
一般 分泌 経路 (Sec)トランスロコン(プレプロティン・トランスロカーゼSecY)
ポーター (単 輸送 体 、共 輸送 体 、対向 輸送 体 )[編集 ]
- ミトコンドリアキャリア
タンパク質 主要 ファシリテーター・スーパーファミリー (グリセロール-3-リン酸 トランスポーター、ラクトースパーミアーゼ、多 剤 輸送 体 EmrD)抵抗 性 結節 -細胞 分裂 (英語 版 ) (多 剤 排出 トランスポーターAcrB、多 剤 耐 性 を参照 )- ジカルボキシレート/
アミノ酸 : カチオン共 輸送 体 (プロトングルタミン酸 共 輸送 体 ) 一価 カチオン/プロトン対向 輸送 体 (ナトリウム/プロトン対向 輸送 体 1 NhaA)神経 伝達 物質 ナトリウム共 輸送 体 - アンモニア
輸送 体 薬物 /代謝 物 輸送 体 (小型 多 剤 耐 性 トランスポーターEmrE -構造 が誤 って格納 されている)
イオンチャネルを含 むα -ヘリカルチャネル[編集 ]
- カリウムチャネルKcsAやKvAPのような
電位 依存 性 イオンチャネル、および内 向 き整流 カリウムイオンチャネルKirbac 大 導電性 機械 受容 チャネル(MscL)小 導電性 機械 受容 性 イオンチャネル (MscS)- CorA
金属 イオン輸送 体 (英語 版 ) 神経 伝達 物質 受容 体 (アセチルコリン受容 体 ) のリガンド依存 性 イオンチャネル- アクアポリン
塩化 物 チャネル外 膜 補助 タンパク質 (多 糖 トランスポーター) -細菌 外 膜 からのα ヘリックス膜 貫通 型 タンパク質
酵素 [編集 ]
- メタンモノオキシゲナーゼ
- ロンボイドプロテアーゼ
- ジスルフィド
結合 形成 タンパク質 (DsbA-DsbB複 合体 )
α ヘリックス膜 貫通 型 アンカーを持 つタンパク質 [編集 ]
- T
細胞 受容 体 膜 貫通 型 二 量 体 化 ドメイン - チトクロムc
亜 硝酸 レダクターゼ複 合体 硫酸 ステリルスルホヒドロラーゼ- スタニン
- グリコホリンA
二 量 体 - イノウイルス(
繊維状 ファージ)主要 コートタンパク質 - ピリン
肺 サーファクタント関連 タンパク質 - モノアミンオキシダーゼAおよびB
脂肪酸 アミド加水 分解 酵素 [18]- シトクロムP450オキシダーゼ
- コルチコステロイド11
β -デヒドロゲナーゼ。 - シグナルペプチドペプチダーゼ
- ストマチン
相 同体 に特異 的 な膜 プロテアーゼ
単一 のポリペプチド鎖 からなるβ バレル[編集 ]
- 8つの
β ストランドからかるβ バレルで、「せん断 数 」が10 (n=8、S=10)。次 が含 まれる。- OmpAのような
膜 貫通 型 ドメイン (OmpA) 病原 性 関連 外 膜 タンパク質 ファミリー (OmpX)外 膜 タンパク質 Wファミリー (OmpW)抗菌 ペプチド耐 性 および脂質 Aアシル化 タンパク質 ファミリー(PagP)- リピドAデアシラーゼPagL
透過 性 ファミリーポリン (NspA)
- OmpAのような
- オートトランスポータードメイン (n=12、S=14)
- FadL
外 膜 タンパク質 輸送 体 ファミリー、脂肪酸 輸送 体 FadL (n=14、S=14) を含 む 三 量 体 ポリンとして知 られる一般 的 な細菌 ポリンファミリー (n=16、S=20))- マルトポリン、またはシュガーポリン (sugar porins) (n=18、S= 22)
- ヌクレオシド
特異 的 ポリン (n=12、S=16) 外 膜 ホスホリパーゼA1 (n=12、S=16)- TonB
依存 受容 体 とそのプラグドメイン。それらは、リガンド依存 性 外 膜 チャネル (n=22、S=24) であり、コバラミン輸送 体 BtuB、Fe(III)-ピオケリン受容 体 FptA、受容 体 FepA、ヒドロキサメート鉄 吸収 受容 体 FhuA、輸送 体 FecA、およびピオバジン受容 体 FpvAを含 む 外 膜 プロテアーゼOmpTおよびアドヘシン/インベイシンOpcAタンパク質 を含 む外 膜 タンパク質 OpcAファミリー (n=10、S=12)外 膜 タンパク質 Gポリンファミリー (n=14、S=16)
複数 のポリペプチド鎖 からなるβ バレル[編集 ]
三 量 体 オートトランスポーター (n=12、S=12)外 膜 排出 タンパク質 、TolCや多 剤 耐 性 タンパク質 を含 む三 量 体外 膜 因子 (n=12、S=18) としても知 られている- MspAポリン (オクタマー、 n=S=16) および
α 溶血 素 (ヘプタマー n=S=14)。これらのタンパク質 は分泌 される。
参照 項目 [編集 ]
脚注 [編集 ]
- ^ Manor, Joshua; Feldblum, Esther S.; Arkin, Isaiah T. (2012). “Environment Polarity in Proteins Mapped Noninvasively by FTIR Spectroscopy”. The Journal of Physical Chemistry Letters 3 (7): 939–944. doi:10.1021/jz300150v. PMC 3341589. PMID 22563521.
- ^ Steven R. Goodman (2008). Medical cell biology. Academic Press. pp. 37–. ISBN 978-0-12-370458-0 2010
年 11月24日 閲覧 。 - ^ Jin Xiong (2006). Essential bioinformatics. Cambridge University Press. pp. 208–. ISBN 978-0-521-84098-9 2010
年 11月13日 閲覧 。 - ^ alpha-helical proteins in outer membranes include Stannin and certain lipoproteins, and others
- ^ “Mapping the human membrane proteome: a majority of the human membrane proteins can be classified according to function and evolutionary origin”. BMC Biol. 7: 50. (2009). doi:10.1186/1741-7007-7-50. PMC 2739160. PMID 19678920.
- ^ Nicholson, L. K.; Cross, T. A. (1989). “Gramicidin cation channel: an experimental determination of the right-handed helix sense and verification of .beta.-type hydrogen bonding” (
英語 ). Biochemistry 28 (24): 9379–9385. doi:10.1021/bi00450a019. PMID 2482072. - ^ Kubyshkin, Vladimir; Grage, Stephan L.; Ulrich, Anne S.; Budisa, Nediljko (2019). “Bilayer thickness determines the alignment of model polyproline helices in lipid membranes” (
英語 ). Physical Chemistry Chemical Physics 21 (40): 22396–22408. Bibcode: 2019PCCP...2122396K. doi:10.1039/c9cp02996f. PMID 31577299. - ^ Harvey Lodish etc.; Molecular Cell Biology, Sixth edition, p.546
- ^ Goder, Veit; Spiess, Martin (31 August 2001). “Topogenesis of membrane proteins: determinants and dynamics”. FEBS Letters 504 (3): 87–93. doi:10.1016/S0014-5793(01)02712-0. PMID 11532438.
- ^ Cross, Timothy A.; Sharma, Mukesh; Yi, Myunggi; Zhou, Huan-Xiang (2011). “Influence of Solubilizing Environments on Membrane Protein Structures”. Trends in Biochemical Sciences 36 (2): 117–125. doi:10.1016/j.tibs.2010.07.005. PMC 3161620. PMID 20724162.
- ^ White, Stephen. "General Principle of Membrane Protein Folding and Stability". Stephen White Laboratory Homepage. 10 Nov. 2009. web.[
要 検証 ] - ^ Carpenter, Elisabeth P; Beis, Konstantinos; Cameron, Alexander D; Iwata, So (October 2008). “Overcoming the challenges of membrane protein crystallography”. Current Opinion in Structural Biology 18 (5): 581–586. doi:10.1016/j.sbi.2008.07.001. PMC 2580798. PMID 18674618.
- ^ Membrane Proteins of known 3D Structure
- ^ Elofsson, Arne; Heijne, Gunnar von (7 June 2007). “Membrane Protein Structure: Prediction versus Reality”. Annual Review of Biochemistry 76 (1): 125–140. doi:10.1146/annurev.biochem.76.052705.163539. PMID 17579561.
- ^ Chen, Chien Peter; Rost, Burkhard (2002). “State-of-the-art in membrane protein prediction”. Applied Bioinformatics 1 (1): 21–35. PMID 15130854.
- ^ Hopf, Thomas A.; Colwell, Lucy J.; Sheridan, Robert; Rost, Burkhard; Sander, Chris; Marks, Debora S. (June 2012). “Three-Dimensional Structures of Membrane Proteins from Genomic Sequencing”. Cell 149 (7): 1607–1621. doi:10.1016/j.cell.2012.04.012. PMC 3641781. PMID 22579045.
- ^ Michalik, Marcin; Orwick-Rydmark, Marcella; Habeck, Michael; Alva, Vikram; Arnold, Thomas; Linke, Dirk; Permyakov, Eugene A. (3 August 2017). “An evolutionarily conserved glycine-tyrosine motif forms a folding core in outer membrane proteins”. PLOS ONE 12 (8): e0182016. Bibcode: 2017PLoSO..1282016M. doi:10.1371/journal.pone.0182016. PMC 5542473. PMID 28771529.
- ^ “Structural adaptations in a membrane enzyme that terminates endocannabinoid signaling”. Science 298 (5599): 1793–6. (November 2002). Bibcode: 2002Sci...298.1793B. doi:10.1126/science.1076535. PMID 12459591.
- ^ “Principles determining the structure of beta-sheet barrels in proteins. I. A theoretical analysis”. J. Mol. Biol. 236 (5): 1369–81. (March 1994). doi:10.1016/0022-2836(94)90064-7. PMID 8126726.
