MHCクラスI分子 ぶんし (MHCクラスIぶんし、英 えい MHC class I molecules )は、主要 しゅよう 組織 そしき 適合 てきごう 遺伝子 いでんし 複 ふく 合体 がったい 分子 ぶんし 主要 しゅよう MHCクラスII分子 ぶんし )、脊椎動物 せきついどうぶつ 全 すべ 有 ゆう 核 かく 細胞 さいぼう 細胞 さいぼう 表面 ひょうめん 存在 そんざい [1] [2] 分子 ぶんし 血小板 けっしょうばん 存在 そんざい 赤血球 せっけっきゅう 存在 そんざい 分子 ぶんし 機能 きのう 細胞 さいぼう 内 ない タンパク質 たんぱくしつ 由来 ゆらい ペプチド 断片 だんぺん 細胞 さいぼう 傷害 しょうがい 性 せい 細胞 さいぼう 提示 ていじ 非 ひ 自己 じこ 抗原 こうげん 提示 ていじ 場合 ばあい 迅速 じんそく 免疫 めんえき 応答 おうとう 開始 かいし 分子 ぶんし 細胞 さいぼう 質 しつ タンパク質 たんぱくしつ 由来 ゆらい 提示 ていじ 分子 ぶんし 提示 ていじ 経路 けいろ 細胞 さいぼう 質 しつ 性 せい 経路 けいろ 内因 ないいん 性 せい 経路 けいろ 呼 よ [3]
ヒトでは、MHCクラスI分子 ぶんし 対応 たいおう 主要 しゅよう ヒト白血球 はっけっきゅう 型 がた 抗原 こうげん (HLA)は、HLA-A 、HLA-B (英語 えいご 版 ばん HLA-C (英語 えいご 版 ばん
MHCクラスI分子 ぶんし 主 おも プロテアソーム による細胞 さいぼう 質 しつ タンパク質 たんぱくしつ 分解 ぶんかい 生 しょう 結合 けつごう 後 ご 複 ふく 合体 がったい 小 しょう 膜 まく 経 へ 細胞 さいぼう 膜 まく 外側 そとがわ 挿入 そうにゅう エピトープ となるペプチドはMHCクラスI分子 ぶんし 細胞 さいぼう 外 がい 部分 ぶぶん 結合 けつごう 分子 ぶんし 細胞 さいぼう 内 ない タンパク質 たんぱくしつ 細胞 さいぼう 傷害 しょうがい 性 せい 細胞 さいぼう 提示 ていじ [1] 分子 ぶんし 外来 がいらい タンパク質 たんぱくしつ 形成 けいせい 提示 ていじ 過程 かてい 交差 こうさ 提示 ていじ 知 し [4]
正常 せいじょう 細胞 さいぼう 正常 せいじょう 細胞 さいぼう 内 ない タンパク質 たんぱくしつ 生 しょう 提示 ていじ 中枢 ちゅうすう 性 せい 末梢 まっしょう 性 せい 免疫 めんえき 寛容 かんよう 応答 おうとう 活性 かっせい 化 か ウイルス 感染 かんせん 後 のち 細胞 さいぼう 外来 がいらい 性 せい タンパク質 たんぱくしつ 発現 はつげん 分子 ぶんし 一部 いちぶ タンパク質 たんぱくしつ 由来 ゆらい 細胞 さいぼう 表面 ひょうめん 提示 ていじ 複 ふく 合体 がったい 特異 とくい 的 てき 認識 にんしき 細胞 さいぼう 死 し 行 おこな
MHCクラスI分子 ぶんし 自身 じしん ナチュラルキラー細胞 さいぼう (NK細胞 さいぼう 阻害 そがい 的 てき リガンド として機能 きのう 細胞 さいぼう 表面 ひょうめん 分子 ぶんし 低下 ていか 一部 いちぶ [5] 特定 とくてい 種 しゅ 腫瘍 しゅよう 応答 おうとう 回避 かいひ 利用 りよう 機構 きこう 同時 どうじ 細胞 さいぼう 活性 かっせい 化 か
PirBと視覚 しかく 可塑 かそ 性 せい [ 編集 へんしゅう ] PirB(Paired-immunoglobulin-like receptor B)はMHC Iに結合 けつごう 受容 じゅよう 体 たい 視覚 しかく 可塑 かそ 性 せい 調節 ちょうせつ 関与 かんよ [6] 中枢 ちゅうすう 神経 しんけい 系 けい 発現 はつげん 発生 はっせい 臨界 りんかい 期 き 成体 せいたい 眼 め 優位 ゆうい 性 せい (英語 えいご 版 ばん 可塑 かそ 性 せい 低下 ていか [6] 機能 きのう 喪失 そうしつ 変異 へんい 体 たい 全 ぜん 年齢 ねんれい 層 そう 眼 め 優位 ゆうい 可塑 かそ 性 せい 増大 ぞうだい 臨界 りんかい 期 き 単眼 たんがん 剥奪 はくだつ (英語 えいご 版 ばん 後 ご 可塑 かそ 性 せい 増加 ぞうか 示 しめ [6] 結果 けっか 視覚 しかく 野 の シナプス可塑 かそ 性 せい (英語 えいご 版 ばん 調節 ちょうせつ 関与 かんよ 可能 かのう 性 せい 示唆 しさ
MHCクラスI分子 ぶんし α あるふぁ 鎖 くさり β べーた 2 -ミクログロブリン本 ほん 鎖 くさり 構成 こうせい 鎖 くさり α あるふぁ 3 ドメイン間 あいだ 相互 そうご 作用 さよう 非 ひ 共有 きょうゆう 結合 けつごう 的 てき 連結 れんけつ 多 た 型 かた 存在 そんざい HLA 遺伝子 いでんし α あるふぁ 鎖 くさり α あるふぁ 3 ドメインは細胞 さいぼう 膜 まく 貫通 かんつう T細胞 さいぼう のCD8 コレセプター と相互 そうご 作用 さよう α あるふぁ 3 -CD8間 あいだ 相互 そうご 作用 さよう 分子 ぶんし 所定 しょてい 位置 いち 保持 ほじ α あるふぁ 1 -α あるふぁ 2 ドメインはペプチドが結合 けつごう 溝 みぞ 形成 けいせい 細胞 さいぼう 傷害 しょうがい 性 せい 細胞 さいぼう 表面 ひょうめん T細胞 さいぼう 受容 じゅよう 体 たい はα あるふぁ 1 -α あるふぁ 2 ドメインに結合 けつごう 抗原 こうげん 性 せい 調 しら 分子 ぶんし 結合 けつごう 長 なが 主 おも アミノ酸 あみのさん [7] 長 なが 結合 けつごう 報告 ほうこく [8]
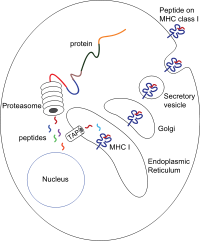
プロテアソームによる細胞 さいぼう 質 しつ タンパク質 たんぱくしつ 分解 ぶんかい 複 ふく 合体 がったい 小 しょう 輸送 ゆそう 分子 ぶんし 提示 ていじ 細胞 さいぼう 表面 ひょうめん 輸送 ゆそう 一連 いちれん 過程 かてい 模 も 式 しき 図 ず ペプチドは主 おも 細胞 さいぼう 質 しつ 生成 せいせい 巨 きょ 大分 おおいた 子 こ 細胞 さいぼう 内 ない タンパク質 たんぱくしつ 小 ちい 分解 ぶんかい 細胞 さいぼう 質 しつ 放出 ほうしゅつ 異 こと 断片 だんぺん 呼 よ 非 ひ 連続 れんぞく 的 てき 上 じょう 直線 ちょくせん 的 てき 並 なら 配列 はいれつ 持 も 産 さん 生 む 起源 きげん 同 おな タンパク質 たんぱくしつ 由来 ゆらい 断片 だんぺん 異 こと タンパク質 たんぱくしつ 由来 ゆらい トランススプライシング )[9] [10] 分子 ぶんし 結合 けつごう 部位 ぶい 小 しょう 内 ない 位置 いち 分子 ぶんし 結合 けつごう 細胞 さいぼう 質 しつ 小 しょう 移行 いこう 必要 ひつよう
移行 いこう [ 編集 へんしゅう ] ペプチドの細胞 さいぼう 質 しつ 小 しょう 内 ない 移行 いこう TAP (transporter associated with antigen processing)と呼 よ トランスポーター によって行 おこな ABCトランスポーター ファミリーのメンバーであり、TAP1 (英語 えいご 版 ばん TAP2 (英語 えいご 版 ばん タンパク質 たんぱくしつ 細胞 さいぼう 質 しつ 側 がわ 結合 けつごう 部位 ぶい 結合 けつごう 部位 ぶい 形成 けいせい 細胞 さいぼう 質 しつ 側 がわ 結合 けつごう 消費 しょうひ 小 しょう 内 ない 転移 てんい 後 ご 小 しょう 内 ない 分子 ぶんし
ペプチドのローディング過程 かてい ペプチドローディング複 ふく 合体 がったい (英語 えいご 版 ばん 呼 よ 巨大 きょだい 複 ふく 合体 がったい 形成 けいせい 分子 ぶんし 関与 かんよ [11] タパシン (英語 えいご 版 ばん カルレティキュリン 、カルネキシン 、ERp57(PDIA3 )から構成 こうせい 結合 けつごう 前 まえ 分子 ぶんし α あるふぁ 鎖 くさり 安定 あんてい 化 か 分子 ぶんし 完全 かんぜん 組 く 立 た 後 のち 解離 かいり 結合 けつごう 分子 ぶんし 不安定 ふあんてい シャペロン であるカルレティキュリンやERp57の結合 けつごう 必要 ひつよう 分子 ぶんし 結合 けつごう タンパク質 たんぱくしつ 呼 よ 選択 せんたく 繰 く 返 かえ 過程 かてい 促進 そくしん [12] [13] [14]
ペプチドがMHCクラスI分子 ぶんし 複 ふく 合体 がったい 解離 かいり 小 しょう 分泌 ぶんぴつ 経路 けいろ 経由 けいゆ 細胞 さいぼう 表面 ひょうめん 移動 いどう 分子 ぶんし 分泌 ぶんぴつ 経路 けいろ 経由 けいゆ 輸送 ゆそう 過程 かてい 分子 ぶんし 翻訳 ほんやく 後 ご 修飾 しゅうしょく 伴 ともな 翻訳 ほんやく 後 ご 修飾 しゅうしょく 一部 いちぶ 小 しょう 内 ない 起 お タンパク質 たんぱくしつ N -グリカン 領域 りょういき 変化 へんか 伴 ともな 後 ご ゴルジ体 たい でN -グリカンの広範囲 こうはんい 変化 へんか 行 おこな 細胞 さいぼう 表面 ひょうめん 到達 とうたつ 前 まえ 完全 かんぜん 成熟 せいじゅく 行 おこな
小 しょう 内 ない 分子 ぶんし 結合 けつごう Sec61 チャネルを介 かい 小 しょう 細胞 さいぼう 質 しつ 除去 じょきょ [15] [16] 受 う 分子 ぶんし 結合 けつごう 小 しょう 送 おく 返 かえ 可能 かのう 性 せい 外来 がいらい タンパク質 たんぱくしつ 交差 こうさ 提示 ていじ 際 さい 利用 りよう [17]
MHCクラスI分子 ぶんし ユビキチン化 か された細胞 さいぼう 質 しつ タンパク質 たんぱくしつ 分解 ぶんかい 形成 けいせい 自身 じしん タンパク質 たんぱくしつ 細胞 さいぼう 質 しつ 発現 はつげん 誘導 ゆうどう 産物 さんぶつ 一部 いちぶ 分解 ぶんかい 付 づ 結果 けっか 生 しょう 断片 だんぺん 小 しょう 移行 いこう 分子 ぶんし 結合 けつごう 分子 ぶんし 依存 いぞん 的 てき 抗原 こうげん 提示 ていじ 経路 けいろ 感染 かんせん 細胞 さいぼう 感染 かんせん 異常 いじょう タンパク質 たんぱくしつ 産 さん 生 む 細胞 さいぼう 送 おく
ウイルス感染 かんせん 細胞 さいぼう 隣接 りんせつ 細胞 さいぼう 感染 かんせん 起 お 低減 ていげん 常 つね 細胞 さいぼう 性 せい 免疫 めんえき 介 かい アポトーシス が誘導 ゆうどう 免疫 めんえき 監視 かんし 機構 きこう 対 たい 進化 しんか 的 てき 応答 おうとう 多 おお 分子 ぶんし ダウンレギュレーション するか、または細胞 さいぼう 表面 ひょうめん 提示 ていじ 防 ふせ 可能 かのう 細胞 さいぼう 傷害 しょうがい 性 せい 細胞 さいぼう 対照 たいしょう 的 てき 細胞 さいぼう 細胞 さいぼう 表面 ひょうめん 分子 ぶんし 認識 にんしき 通常 つうじょう 不 ふ 活性 かっせい 化 か 分子 ぶんし 存在 そんざい 場合 ばあい 細胞 さいぼう 活性 かっせい 化 か 異常 いじょう 細胞 さいぼう 認識 にんしき 分子 ぶんし 形質 けいしつ 転換 てんかん 細胞 さいぼう 感染 かんせん 細胞 さいぼう 形質 けいしつ 転換 てんかん 細胞 さいぼう 破壊 はかい 通常 つうじょう 免疫 めんえき 監視 かんし 機構 きこう 逃 のが 同様 どうよう 生存 せいぞん 上 じょう 利点 りてん 生 しょう [18]
遺伝子 いでんし [ 編集 へんしゅう ] 多 た 型 かた 非常 ひじょう 多 おお 多 た 型 かた 少 すく 進化 しんか 的 てき 歴史 れきし [ 編集 へんしゅう ] MHCクラスI分子 ぶんし 遺伝子 いでんし 顎 あご 口上 こうじょう 綱 つな 全 すべ 生物 せいぶつ 共通 きょうつう 祖先 そせん 起源 きげん 持 も 研究 けんきゅう 現存 げんそん 全 すべ 顎 あご 口上 こうじょう 綱 つな 生物 せいぶつ 存在 そんざい [2] 顎 あご 口上 こうじょう 綱 つな 出現 しゅつげん 以降 いこう 遺伝子 いでんし 種 たね 分化 ぶんか 過程 かてい 多 おお 分岐 ぶんき 進化 しんか 経路 けいろ 遺伝子 いでんし 多 た 型 がた 種 たね 間 あいだ 比較 ひかく 研究 けんきゅう 種 たね 間 あいだ 進化 しんか 的 てき 関連 かんれん 遺伝子 いでんし 特定 とくてい アレル が保存 ほぞん 記載 きさい 双方 そうほう 種 たね 感染 かんせん 病原 びょうげん 体 たい 強 つよ 平衡 へいこう 選択 せんたく (英語 えいご 版 ばん 可能 かのう 性 せい 高 たか [19] 進化 しんか 遺伝子 いでんし 大 おお 関 かん 機構 きこう 説明 せつめい
MHCクラスI遺伝子 いでんし [ 編集 へんしゅう ] Birth-and-death進化 しんか 遺伝子 いでんし 重複 じゅうふく 遺伝子 いでんし 複数 ふくすう 生 しょう 後 ご 異 こと 進化 しんか 的 てき 過程 かてい 経 へ 過程 かてい 遺伝子 いでんし 偽 にせ 遺伝子 いでんし 化 か 起 お 異 こと 機能 きのう 持 も 新 あら 遺伝子 いでんし 生 しょう [20] 遺伝子 いでんし 座 ざ 偽 にせ 遺伝子 いでんし 過程 かてい 遺伝子 いでんし 座 ざ 生 しょう 可能 かのう 性 せい 高 たか [21]
^ a b “The MHC class I antigen presentation pathway: strategies for viral immune evasion” . Immunology 110 (2): 163–9. (October 2003). doi :10.1046/j.1365-2567.2003.01738.x . PMC 1783040 . PMID 14511229 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1783040/ .
^ a b “Comparative genomic analysis of the MHC: the evolution of class I duplication blocks, diversity and complexity from shark to man”. Immunological Reviews 190 : 95–122. (December 2002). doi :10.1034/j.1600-065x.2002.19008.x . PMID 12493009 .
^ http://users.rcn.com/jkimball.ma.ultranet/BiologyPages/H/HLA.html#Class_I_Histocompatibility_Molecules Kimball's Biology Pages, Histocompatibility Molecules^ Joffre, Olivier P.; Segura, Elodie; Savina, Ariel; Amigorena, Sebastian (2012-07-13). “Cross-presentation by dendritic cells” . Nature Reviews. Immunology 12 (8): 557–569. doi :10.1038/nri3254 . ISSN 1474-1741 . PMID 22790179 . https://www.ncbi.nlm.nih.gov/pubmed/22790179 . ^ “MHC class I antigen presentation: learning from viral evasion strategies”. Nature Reviews. Immunology 9 (7): 503–13. (July 2009). doi :10.1038/nri2575 . PMID 19498380 . ^ a b c “PirB restricts ocular-dominance plasticity in visual cortex”. Science 313 (5794): 1795–800. (September 2006). Bibcode : 2006Sci...313.1795S . doi :10.1126/science.1128232 . PMID 16917027 .
^ Parham, P. (1987). “Functional sites of human class I MHC molecules: paradigms a dozen?” . Immunologic Research 6 (3): 153–178. doi :10.1007/BF02918089 . ISSN 0257-277X . PMID 2445879 . https://www.ncbi.nlm.nih.gov/pubmed/2445879 . ^ “Have we cut ourselves too short in mapping CTL epitopes?”. Trends in Immunology 27 (1): 11–6. (January 2006). doi :10.1016/j.it.2005.11.001 . PMID 16297661 . ^ Faridi, Pouya; Li, Chen; Ramarathinam, Sri H.; Vivian, Julian P.; Illing, Patricia T.; Mifsud, Nicole A.; Ayala, Rochelle; Song, Jiangning et al. (12 October 2018). “A subset of HLA-I peptides are not genomically templated: Evidence for cis- and trans-spliced peptide ligands” . Science Immunology 3 (28): eaar3947. doi :10.1126/sciimmunol.aar3947 . PMID 30315122 . http://orca.cf.ac.uk/116124/1/A%20subset%20of%20HLA-1%20peptide%20%20%20J%20ROSSJOHN%20Science%20Immunol.pdf . ^ Liepe, Juliane; Marino, Fabio; Sidney, John; Jeko, Anita; Bunting, Daniel E.; Sette, Alessandro; Kloetzel, Peter M.; Stumpf, Michael P. H. et al. (21 October 2016). “A large fraction of HLA class I ligands are proteasome-generated spliced peptides” . Science 354 (6310): 354–358. Bibcode : 2016Sci...354..354L . doi :10.1126/science.aaf4384 . hdl :10044/1/42330 PMID 27846572 . http://spiral.imperial.ac.uk/bitstream/10044/1/42330/2/Liepe2016_Science.pdf . ^ “Structure of the human MHC-I peptide-loading complex”. Nature 551 (7681): 525–528. (November 2017). Bibcode : 2017Natur.551..525B . doi :10.1038/nature24627 . PMID 29107940 . ^ “Tapasin enhances MHC class I peptide presentation according to peptide half-life” . Proceedings of the National Academy of Sciences of the United States of America 101 (32): 11737–42. (August 2004). Bibcode : 2004PNAS..10111737H . doi :10.1073/pnas.0306294101 . PMC 511045 . PMID 15286279 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC511045/ . ^ “Selective loading of high-affinity peptides onto major histocompatibility complex class I molecules by the tapasin-ERp57 heterodimer”. Nature Immunology 8 (8): 873–81. (August 2007). doi :10.1038/ni1485 . PMID 17603487 . ^ “Tapasin shapes immunodominance hierarchies according to the kinetic stability of peptide-MHC class I complexes”. European Journal of Immunology 38 (2): 364–9. (February 2008). doi :10.1002/eji.200737832 . PMID 18196518 . ^ “Export of antigenic peptides from the endoplasmic reticulum intersects with retrograde protein translocation through the Sec61p channel”. Immunity 13 (1): 117–27. (July 2000). doi :10.1016/S1074-7613(00)00013-3 . PMID 10933400 . ^ “Retrotranslocation of MHC class I heavy chain from the endoplasmic reticulum to the cytosol is dependent on ATP supply to the ER lumen”. Molecular Immunology 40 (10): 733–41. (January 2004). doi :10.1016/j.molimm.2003.08.008 . PMID 14644099 . ^ “Exogenous antigens are processed through the endoplasmic reticulum-associated degradation (ERAD) in cross-presentation by dendritic cells” . International Immunology 17 (1): 45–53. (January 2005). doi :10.1093/intimm/dxh184 . PMID 15546887 . http://intimm.oxfordjournals.org/cgi/pmidlookup?view=long&pmid=15546887 . ^ “Activation of CXCR4 triggers ubiquitination and down-regulation of major histocompatibility complex class I (MHC-I) on epithelioid carcinoma HeLa cells”. The Journal of Biological Chemistry 283 (7): 3951–9. (February 2008). doi :10.1074/jbc.m706848200 . PMID 18083706 . ^ “Trans-species polymorphism in humans and the great apes is generally maintained by balancing selection that modulates the host immune response” . Human Genomics 9 : 21. (September 2015). doi :10.1186/s40246-015-0043-1 . PMC 4559023 . PMID 26337052 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4559023/ . ^ “Concerted and birth-and-death evolution of multigene families” . Annual Review of Genetics 39 (1): 121–52. (2005-11-14). doi :10.1146/annurev.genet.39.073003.112240 . PMC 1464479 . PMID 16285855 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1464479/ . ^ “Origin and evolution of HLA class I pseudogenes”. Molecular Biology and Evolution 12 (2): 247–58. (March 1995). doi :10.1093/oxfordjournals.molbev.a040201 . PMID 7700152 .