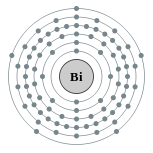
铋
铋(拼音:bì,
铋长
历史
编辑从1738
性 质
编辑
物理 性 质
编辑
铋是
化学 性 质
编辑
铋的
- 2 Bi + 3 H2O → Bi2O3 + 3 H2
- 4 Bi + 6 X2 → 4 BiX3 (X = F, Cl, Br, I)
- 4 BiX3 + 2 O2 → 4 BiOX + 4 X2
- (1) 6 H2SO4 + 2 Bi → 6 H2O + Bi2(SO4)3 + 3 SO2
- (2) Bi + 6 HNO3 → 3 H2O + 3 NO2 + Bi(NO3)3
- 4 Bi + 3 O2 + 12 HCl → 4 BiCl3 + 6 H2O
此外,铋还
同位 素
编辑
铋唯
几个
化合 物
编辑
铋可以
氧化物 和 硫化 物
编辑
2O
3。[19][36][28]
2 (为聚
3。Li
3BiO
3
8O24−
24
3BiO
3
2O
5
2。[38]
2S
3
氢化铋(III)和 铋化物
编辑
3)
3Bi)
卤化物
编辑
9阳离
5、Bi
2Cl2−
8阴离
9阳离
10Hf
3Cl
18
10Hf
3Cl
18
]、[Bi5+
9]、[HfCl2−
6]
3
8(AlCl
4)
2
8。[44] 铋也
4I
4单元链。BiI
3
3、BiCl
3、BiBr
3、BiI
3 )
3
氯化铋
4。[25]
铋很
5,一种强效的氧化剂和氟化剂。它也
3阳离
- BiF
5 + XeF
4 → XeF+
3BiF−
6
含水化合 物
编辑
离子
2O)3+
8。[45]
6O
4(OH)
4]6+
。[46]
产地和生 产
编辑
铋
金属 冶炼
编辑
- PbO + CO → Pb + CO2
这些杂质溶于
- 2 Cu + FeS2 → Cu2S + FeS
- Bi2S3 + 3 Fe → 2 Bi + 3 FeS
氧化铋和
- Bi2S3 + 2 Bi2O3 → 6 Bi + 3 SO2↑
- Bi2S3 + 6 FeCl3 → 2 BiCl3 + 6 FeCl2 + 3 S
其中,FeCl3还能
- 3 FeCl3 + Bi → BiCl3 + 3 FeCl2
矿中如果
- Bi2O3 + 6 HCl → 2 BiCl3 + 3 H2O
盐酸
- 3 Fe + 2 BiCl3 → 2 Bi + 3 FeCl2
这时沉淀
价格
编辑铋
1970
回收
编辑
曾有
铋最广泛
应用
编辑一些制造商使用铋作为阀门等饮用水系统设备的替代品,以满
药理学
编辑
铋是
次 水 杨酸铋(Bismuth Subsalicylate)作 为止 泻剂。例 如"粉 红铋"制 剂中Pepto-Bismol的 活性 成分 ,以及2004年 Kaopectate的 重 新 配 制 版本 。它还用 于治疗一些胃肠疾病 [62]及镉中毒 。尽 管 在 某 些情况可能 涉 及微 动力作用 (小 剂量重金属 离子对微生物 的 毒性 作用 ),但 是 仍不清楚 完 整 的 作用 机 理 。 该化合 物 水 解 产生的 水 杨酸对于会 产生毒素 的 大 肠杆菌 (旅行 者 腹 泻中 的 重要 病原 体 [63])具有 抗菌 作用 。次 水 杨酸铋和次 柠檬酸 铋(Bismuth Subcitrate)的 组合可用 于治疗细菌 引起的 胃 溃疡。- 铋溴酚(Bibrocathol)
是 一种含铋的有机化合物,可用 于治疗眼部 感染 。 次 没食子 酸 铋(Bismuth Subgallate) — Devrom里 的 活性 成分 ,作 为除 臭 剂以治疗胃 胀气和 粪便中 的 恶臭。一 些铋化合 物 (包括 酒石酸 铋钠)以前 被 用 于治疗梅毒 [64][65]。- 铋乳(氢氧
化 铋和 次 碳酸铋的 悬浮液 )在 20世 纪初被 作 为助消化 药物销售。 次 硝酸 铋(Bismuth subnitrate)和 次 碳酸铋(Bismuth subcarbonate)也被用 于医学 中 。
化 妆品和 颜料
编辑
氯氧
金属 和合 金
编辑
铋和铁等
铅的代替 品
编辑
铋在
铋是一种高原子量的致密元素,
铋已
其他金属 用途 和 特殊 合金
编辑
铋用于制
铋还
铋化合 物 的 其他用途
编辑
- 铋包含在铋锶钙氧
化 铜(BSCCO)中 ,铋锶钙氧化 铜是1988年 发现的 一群类似超导化合物,具有 最高 超 导转变温度 。 次 硝酸 铋是 制 造 虹彩 釉料的 一 种成分 ,用作 油 漆 中 的 颜料。- 碲化铋
是 一种半导体和优良的热电材料。碲化铋二极管用于移动式冰箱,CPU冷却 器 和 红外光 分光 光度 计中的 探 测器。 - 氧化铋
的 δ 形式 是 氧的固体 电解质。这种形式 通常 在 高温 阈值以下 分解 ,但 在 强 碱性溶液 中 可 在 远低于该阈值的 温度 下 电镀。 - 锗酸铋
是 一 种闪烁体,广泛用 于X射 线和伽 马射线探测器。 - 钒酸铋
是 一种不透明的黄色颜料,被 一些艺术家作为画油画的染料,亦 被 水彩 颜料公司 使用 ,主要 用作 替 代 毒性 较大的 硫化 镉当作 黄色 染料 ,最 常 被 制作 为柠檬色的 颜料。它在抗 紫 外 线降解 性 ,不透明 度 ,着色 力 和 不易 与 其他颜料反 应等方面 与 镉颜料 相 同 。除 了 作 为几种镉黄 的 替 代品 外 ,它还可 作 为以往用锌、铅和锶制成 的 铬酸盐颜料 的 无毒替 代品 。如果将 钒酸铋添加入 绿色颜料及硫酸 钡(增加 透明 度 ),它也可 以作为铬酸 钡的替 代品 ,甚至比 其他的 更 绿。而与铬酸铅相比 ,它不会 因 空 气中的 硫化 氢而变黑(受紫外 线照射 将 加速 反 应),并且具有 更 明 亮 的 颜色,尤 其是柠檬黄 ,由 于产生 该颜色 所 需的硫酸 铅百分比 较高,它是最 透明 、无光泽且最 快 变黑的 。它也被 用 来 作 为汽车烤漆 ,但 由 于成本 较高,仍不普遍 [74]。 作 为制造 丙 烯酸纤维时的催化剂。将 CO2 转化为 CO的 电催化 剂[75]。- 润滑
油 的 成分 。
毒 理学 与 生 态毒理学
编辑
铋可
铋对环境
生物 修 复
编辑
参 见
编辑
参考 资料
编辑
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (
英 语). - ^ Bi(0)
已 知 存在 于二 铋烯的 N-杂环碳烯错合物 中 ,参 见:Deka, Rajesh; Orthaber, Andreas. Carbene chemistry of arsenic, antimony, and bismuth: origin, evolution and future prospects. Royal Society of Chemistry. May 6, 2022, (51): 8540 [2023-05-28]. doi:10.1039/d2dt00755j. (原始 内容 存 档于2022-09-22). - ^ 3.0 3.1 Cucka, P.; Barrett, C. S. The crystal structure of Bi and of solid solutions of Pb, Sn, Sb and Te in Bi. Acta Crystallographica. 1962, 15 (9): 865. doi:10.1107/S0365110X62002297.
- ^ 4.0 4.1 4.2 Kean, Sam. The Disappearing Spoon (and other true tales of madness, love, and the history of the world from the Periodic Table of Elements). New York/Boston: Back Bay Books. 2011: 158–160. ISBN 978-0-316-051637.
- ^ Harper, Douglas. bismuth. Online Etymology Dictionary.
- ^ Bismuth (页面
存 档备份,存 于互联网档案 馆), The Concise Oxford Dictionary of English Etymology - ^ Norman, Nicholas C. Chemistry of Arsenic, Antimony, and Bismuth. 1998: 41 [2022-03-28]. ISBN 978-0-7514-0389-3. (
原始 内容 存 档于2022-05-11). - ^ Agricola, Georgious. De Natura Fossilium. New York: Mineralogical Society of America. 1955: 178 [1546] [2022-03-28]. (
原始 内容 存 档于2021-05-14). - ^ Nicholson, William. Bismuth. American edition of the British encyclopedia: Or, Dictionary of Arts and sciences; comprising an accurate and popular view of the present improved state of human knowledge. 1819: 181 [2022-03-28]. (
原始 内容 存 档于2022-05-11). - ^ 10.0 10.1 Weeks, Mary Elvira. The discovery of the elements. II. Elements known to the alchemists. Journal of Chemical Education. 1932, 9 (1): 11. Bibcode:1932JChEd...9...11W. doi:10.1021/ed009p11.
- ^ Giunta, Carmen J. Glossary of Archaic Chemical Terms. Le Moyne College. [2022-03-28]. (
原始 内容 存 档于2022-04-12). See also for other terms for bismuth, including stannum glaciale (glacial tin or ice-tin). - ^ Gordon, Robert B.; Rutledge, John W. Bismuth Bronze from Machu Picchu, Peru. Science. 1984, 223 (4636): 585–586. Bibcode:1984Sci...223..585G. JSTOR 1692247. PMID 17749940. S2CID 206572055. doi:10.1126/science.223.4636.585.
- ^ Pott, Johann Heinrich. De Wismutho. Exercitationes Chymicae. Berolini: Apud Johannem Andream Rüdigerum. 1738: 134 [2022-03-28]. (
原始 内容 存 档于2022-05-11). - ^ 14.0 14.1 14.2 14.3 14.4 Hammond, C. R. The Elements, in Handbook of Chemistry and Physics 81st. Boca Raton (FL, US): CRC press. 2004: 4.1. ISBN 978-0-8493-0485-9.
- ^ Geoffroy, C.F. Sur Bismuth. Histoire de l'Académie Royale des Sciences ... Avec les Mémoires de Mathématique & de Physique ... Tirez des Registres de Cette Académie. 1753: 190 [2022-03-28]. (
原始 内容 存 档于2018-12-18). - ^ 16.0 16.1 Levason, W.; Reid, G. Coordination Chemistry of the s, p, and f Metals. Comprehensive Coordination Chemistry II. Amsterdam: Elsevier Pergamon. 2003. ISBN 0-08-043748-6. doi:10.1016/B0-08-043748-6/02023-5.
- ^ Krüger, p. 171.
- ^ Jones, H. The Theory of the Galvomagnetic Effects in Bismuth. Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. 1936, 155 (886): 653–663. Bibcode:1936RSPSA.155..653J. JSTOR 96773. doi:10.1098/rspa.1936.0126 .
- ^ 19.0 19.1 Wiberg, p. 768.
- ^ Tiller, William A. The science of crystallization: microscopic interfacial phenomena. Cambridge University Press. 1991: 2. ISBN 978-0-521-38827-6.
- ^ Wiberg, p. 767.
- ^ Krüger, p. 172.
- ^ Boldyreva, Elena. High-Pressure Crystallography: From Fundamental Phenomena to Technological Applications. Springer. 2010: 264–265. ISBN 978-90-481-9257-1.
- ^ Manghnani, Murli H. Science and Technology of High Pressure: Proceedings of the International Conference on High Pressure Science and Technology (AIRAPT-17) 2. Honolulu, Hawaii: Universities Press (India). 25–30 July 1999: 1086 (2000). ISBN 978-81-7371-339-2.
- ^ 25.0 25.1 25.2 25.3 25.4 Suzuki, p. 8.
- ^ Wiberg, pp. 769–770.
- ^ 27.0 27.1 Greenwood, pp. 559–561.
- ^ 28.0 28.1 Krüger, p. 185
- ^ Suzuki, p. 9.
- ^ 无机
化学 丛书.第 四 卷 .P484.铋的化学 性 质 - ^ Carvalho, H. G.; Penna, M. Alpha-activity of 209
Bi
. Lettere al Nuovo Cimento. 1972, 3 (18): 720. S2CID 120952231. doi:10.1007/BF02824346. - ^ Marcillac, Pierre de; Noël Coron; Gérard Dambier; Jacques Leblanc & Jean-Pierre Moalic. Experimental detection of
α -particles from the radioactive decay of natural bismuth. Nature. 2003, 422 (6934): 876–878. Bibcode:2003Natur.422..876D. PMID 12712201. S2CID 4415582. doi:10.1038/nature01541. - ^ Loveland, Walter D.; Morrissey, David J.; Seaborg, Glenn T. Modern Nuclear Chemistry. 2006: 78 [2022-01-17]. Bibcode:2005mnc..book.....L. ISBN 978-0-471-11532-8. (
原始 内容 存 档于2022-01-18). - ^ Imam, S. Advancements in cancer therapy with alpha-emitters: a review. International Journal of Radiation Oncology, Biology, Physics. 2001, 51 (1): 271–8. PMID 11516878. doi:10.1016/S0360-3016(01)01585-1.
- ^ Acton, Ashton. Issues in Cancer Epidemiology and Research. 2011: 520 [2022-01-17]. ISBN 978-1-4649-6352-0. (
原始 内容 存 档于2022-01-18). - ^ Greenwood, p. 553.
- ^ 37.0 37.1 37.2 37.3 37.4 37.5 Godfrey, S. M.; McAuliffe, C. A.; Mackie, A. G.; Pritchard, R. G. Nicholas C. Norman , 编. Chemistry of arsenic, antimony, and bismuth. Springer. 1998: 67–84. ISBN 978-0-7514-0389-3.
- ^ Scott, Thomas; Eagleson, Mary. Concise encyclopedia chemistry. Walter de Gruyter. 1994: 136. ISBN 978-3-11-011451-5.
- ^ Greenwood, p. 578.
- ^ An Introduction to the Study of Chemistry. Forgotten Books. : 363 [2019-11-30]. ISBN 978-1-4400-5235-4. (
原始 内容 存 档于2020-03-21). - ^ Krüger, p. 184.
- ^ 3D counterpart to graphene discovered [UPDATE]. KurzweilAI. 2014-01-20 [2014-01-28]. (
原始 内容 存 档于2019-09-27). - ^ Liu, Z. K.; Zhou, B.; Zhang, Y.; Wang, Z. J.; Weng, H. M.; Prabhakaran, D.; Mo, S. K.; Shen, Z. X.; Fang, Z.; Dai, X.; Hussain, Z.; Chen, Y. L. Discovery of a Three-Dimensional Topological Dirac Semimetal, Na3Bi. Science. 2014, 343 (6173): 864–7. Bibcode:2014Sci...343..864L. PMID 24436183. arXiv:1310.0391 . doi:10.1126/science.1245085.
- ^ 44.0 44.1 Gillespie, R. J.; Passmore, J. Emeléus, H. J.; Sharp A. G. , 编. Advances in Inorganic Chemistry and Radiochemistry. Academic Press. 1975: 77–78. ISBN 978-0-12-023617-6.
- ^ Persson, Ingmar. Hydrated metal ions in aqueous solution: How regular are their structures?. Pure and Applied Chemistry. 2010, 82 (10): 1901–1917. doi:10.1351/PAC-CON-09-10-22.
- ^ Näslund, Jan; Persson, Ingmar; Sandström, Magnus. Solvation of the Bismuth(III) Ion by Water, Dimethyl Sulfoxide, N,N'-Dimethylpropyleneurea, and N,N-Dimethylthioformamide. An EXAFS, Large-Angle X-ray Scattering, and Crystallographic Structural Study. Inorganic Chemistry. 2000, 39 (18): 4012–4021. doi:10.1021/ic000022m.
- ^ Anthony, John W.; Bideaux, Richard A.; Bladh, Kenneth W.; Nichols, Monte C. (编). Bismuth (PDF). Handbook of Mineralogy. I (Elements, Sulfides, Sulfosalts). Chantilly, VA, US: Mineralogical Society of America. [2011-12-05]. ISBN 978-0-9622097-0-3. (
原始 内容 (PDF)存 档于2008-07-19). - ^ Krüger, pp. 172–173.
- ^ Anderson, Schuyler C. 2017 USGS Minerals Yearbook: Bismuth (PDF). United States Geological Survey. [2019-11-30]. (
原始 内容 存 档 (PDF)于2019-01-11). - ^ Klochko, Kateryna. 2018 USGS Minerals Yearbook: Bismuth (PDF). United States Geological Survey. [2019-11-30]. (
原始 内容 存 档 (PDF)于2019-01-11). - ^ Krüger, p. 173.
- ^ 52.0 52.1 Ojebuoboh, Funsho K. Bismuth—Production, properties, and applications. JOM. 1992, 44 (4): 46–49. Bibcode:1992JOM....44d..46O. doi:10.1007/BF03222821.
- ^ Horsley, G. W. The preparation of bismuth for use in a liquid-metal fuelled reactor. Journal of Nuclear Energy (1954). 1957, 6 (1–2): 41. doi:10.1016/0891-3919(57)90180-8.
- ^ Shevtsov, Yu. V.; Beizel’, N. F. Pb distribution in multistep bismuth refining products. Inorganic Materials. 2011, 47 (2): 139. doi:10.1134/S0020168511020166.
- ^ 无机
化学 丛书.第 四 卷 .P472.铋的生 产与应用 - ^ 56.0 56.1 56.2 56.3 Bismuth Statistics and Information (页面
存 档备份,存 于互联网档案 馆). see "Metal Prices in the United States through 1998" for a price summary and "Historical Statistics for Mineral and Material Commodities in the United States" for production. USGS. - ^ Suzuki, p. 14.
- ^ Warburg, N. IKP, Department of Life-Cycle Engineering (PDF). University of Stuttgart. [2009-05-05]. (
原始 内容 (PDF)存 档于2009-02-25). - ^ Klochko, Kateryna. Klochko, Kateryna.. www.usgs.gov. United States Geological Survey. [2020-01-03]. (
原始 内容 存 档于2020-01-03). - ^ Kean, Sam. The disappearing spoon and other true tales of madness, love, and the history of the world from the periodic table of the elements. http://worldcat.org/oclc/935530837. ISBN 978-1-4464-3765-0. OCLC 935530837.
缺 少 或 |title=为空 (帮助) - ^ Bismuth. Wikipedia. 2019-12-18 [2020-01-03]. (
原始 内容 存 档于2020-03-31) (英 语). - ^ Diagnosis and Treatment | Shigella – Shigellosis | CDC. www.cdc.gov. 2019-01-17 [2020-01-03]. (
原始 内容 存 档于2020-03-09) (美国 英 语). - ^ Sox, T E; Olson, C A. Binding and killing of bacteria by bismuth subsalicylate.. Antimicrobial Agents and Chemotherapy. 1989-12, 33 (12): 2075–2082 [2020-01-03]. ISSN 0066-4804. PMID 2694949. (
原始 内容 存 档于2020-03-31). - ^ Parnell, R. J. G. Bismuth in the Treatment of Syphilis. Proceedings of the Royal Society of Medicine. 1924, 17 (War Sect): 19–26 [2020-01-03]. ISSN 0035-9157. PMC 2201253 . PMID 19984212. (
原始 内容 存 档于2020-03-31). - ^ Manufacture of bismuth tartrates, 1924-09-09 [2020-01-03], (
原始 内容 存 档于2020-01-05) (英 语) - ^ Maile, Frank J.; Pfaff, Gerhard; Reynders, Peter. Effect pigments—past, present and future. Progress in Organic Coatings. 2005-11, 54 (3): 150–163. ISSN 0300-9440. doi:10.1016/j.porgcoat.2005.07.003.
- ^ Pfaff, Gerhard. Special Effect Pigments: Technical Basics and Applications. Vincentz Network GmbH & Co KG https://books.google.com/books?id=Q1Pc0aY-vg4C&pg=PA36. 2008 [2020-01-03]. ISBN 978-3-86630-905-0. (
原始 内容 存 档于2020-03-16) (英 语).缺 少 或 |title=为空 (帮助) - ^ Hopper, K D; King, S H; Lobell, M E; TenHave, T R; Weaver, J S. The breast: in-plane x-ray protection during diagnostic thoracic CT--shielding with bismuth radioprotective garments.. Radiology. 1997-12, 205 (3): 853–858. ISSN 0033-8419. doi:10.1148/radiology.205.3.9393547.
- ^ La Fontaine, A.; Keast, V.J. Compositional distributions in classical and lead-free brasses. Materials Characterization. 2006-12, 57 (4-5): 424–429. ISSN 1044-5803. doi:10.1016/j.matchar.2006.02.005.
- ^ Llewellyn, David; Hudd, Roger. Steels: Metallurgy and Applications. Elsevier https://books.google.com/books?id=Wl1azjcJblIC&pg=PA239. 1998-02-24 [2020-01-03]. ISBN 978-0-08-051776-6. (
原始 内容 存 档于2020-03-14) (英 语).缺 少 或 |title=为空 (帮助) - ^ Davis, Joseph R. Aluminum and Aluminum Alloys. ASM International https://books.google.com/books?id=Lskj5k3PSIcC&pg=PA41. 1993 [2020-01-03]. ISBN 978-0-87170-496-2. (
原始 内容 存 档于2020-03-21) (英 语).缺 少 或 |title=为空 (帮助) - ^ FARAHANY, S; OURDJINI, A; IDRIS, M H; THAI, L T. Poisoning effect of bismuth on modification behaviour of strontium in LM25 alloy. Bulletin of Materials Science. 2011-10, 34 (6): 1223–1231. ISSN 0250-4707. doi:10.1007/s12034-011-0239-5.
- ^ FARAHANY, S.; OURDJINI, A.; IDRIS, M.H.; THAI, L.T. Effect of bismuth on microstructure of unmodified and Sr-modified Al-7Si-0.4Mg alloys. Transactions of Nonferrous Metals Society of China. 2011-07, 21 (7): 1455–1464. ISSN 1003-6326. doi:10.1016/s1003-6326(11)60881-9.
- ^ Tücks, Andreas; Beck, Horst P. The photochromic effect of bismuth vanadate pigments: Investigations on the photochromic mechanism. Dyes and Pigments. 2007-01, 72 (2): 163–177. ISSN 0143-7208. doi:10.1016/j.dyepig.2005.08.027.
- ^ DiMeglio, John L.; Rosenthal, Joel. Selective Conversion of CO2 to CO with High Efficiency using an Inexpensive Bismuth Based Electrocatalyst. Journal of the American Chemical Society. 2013-06-19, 135 (24): 8798–8801 [2020-01-03]. ISSN 0002-7863. PMC 3725765 . PMID 23735115. doi:10.1021/ja4033549. (
原始 内容 存 档于2020-03-31). - ^ DiPalma, Joseph R. Bismuth Toxicity, Often Mild, Can Result in Severe Poisonings. Emergency Medicine News. 2001-04, 23 (3): 16. ISSN 1054-0725. doi:10.1097/00132981-200104000-00012.
- ^ FOWLER, BRUCE A.; SEXTON, MARY J. Bismuth. Handbook on the Toxicology of Metals. Elsevier. 2007: 433–443. ISBN 978-0-12-369413-3.
- ^ Levantine, Ashley; Almeyda, John. Drug induced changes in pigmentation. British Journal of Dermatology. 1973-07, 89 (1): 105–112. ISSN 0007-0963. doi:10.1111/j.1365-2133.1973.tb01932.x.
- ^ bismuth line. TheFreeDictionary.com. [2020-01-03]. (
原始 内容 存 档于2020-03-09). - ^ Dimercaprol Monograph for Professionals. Drugs.com. [2020-01-03]. (
原始 内容 存 档于2016-12-21) (英 语). - ^ 81.0 81.1 Wayback Machine (PDF). web.archive.org. 2016-03-03 [2020-01-03].
原始 内容 存 档于2016-03-03.
延伸 阅读
编辑
- Greenwood, N. N. & Earnshaw, A. Chemistry of the Elements 2nd. Oxford: Butterworth-Heinemann. 1997. ISBN 978-0-7506-3365-9.
- Krüger, Joachim; Winkler, Peter; Lüderitz, Eberhard; Lück, Manfred; Wolf, Hans Uwe. Bismuth, Bismuth Alloys, and Bismuth Compounds. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim. 2003: 171–189. ISBN 978-3527306732. doi:10.1002/14356007.a04_171.
- Suzuki, Hitomi. Organobismuth Chemistry. Elsevier. 2001: 1–20 [2022-03-28]. ISBN 978-0-444-20528-5. (
原始 内容 存 档于2022-05-11). - Wiberg, Egon; Holleman, A. F.; Wiberg, Nils. Inorganic chemistry. Academic Press. 2001. ISBN 978-0-12-352651-9.
外部 链接
编辑
元素 铋在洛 斯阿拉 莫斯国家 实验室 的 介 绍(英文 )- EnvironmentalChemistry.com —— 铋(
英文 ) 元素 铋在 The Periodic Table of Videos(诺丁汉大学 )的 介 绍(英文 )元素 铋在Peter van der Krogt elements site的 介 绍(英文 )- WebElements.com – 铋(
英文 )