タンパク質 構造 予測

概要 [編集 ]
しかし
タンパク質 がとる可能 性 がある構造 の数 は、膨大 である(レヴィンタールのパラドックス)。タンパク質 構造 の安定 性 に関 する物理 学 的 な基盤 が、あまり理解 されていない。一部 のタンパク質 では、その一 次 構造 のみで三 次 構造 を決定 できないことがある。例 えば、シャペロンという名前 で知 られる一群 のタンパク質 は、別 のタンパク質 が正 しく折 りたたむ(三 次 構造 をとる)のを助 ける。分子 動力 学 法 (MD法 )のような手法 でタンパク質 の折 りたたみを直接 シミュレートすることは、実際 的 な理由 および理論 的 な理由 から、一般 的 には扱 いにくい。
このような
タンパク質 の構造 と用語 [編集 ]
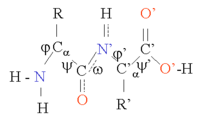
これらの
α ヘリックス[編集 ]
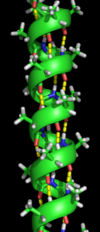
β シート[編集 ]
ループ[編集 ]
タンパク質 の分類 [編集 ]
タンパク質 の構造 や配列 を分類 するための用語 [編集 ]
活性 部位 化学 的 に特異 的 な基質 と相互 作用 することができ、タンパク質 に生物 学 的 活性 を与 える、三 次 構造 (三 次元 )または四 次 構造 (タンパク質 サブユニット)内 のアミノ酸 側 鎖 の局所 的 な組 み合 わせのこと。全 く異 なるアミノ酸 配列 のタンパク質 は、同 じ活性 部位 を持 つ構造 に折 りたたまれることがある。- アーキテクチャ
三 次元 構造 における二 次 構造 の相対 的 な向 きであり、類似 のループ構造 を共有 しているかどうかに関 わらず表 したもの。折 りたたみ(トポロジー)保存 ループ構造 を持 つアーキテクチャの一種 。- ブロック
タンパク質 ファミリーの保存 アミノ酸 配列 パターン。そのパターンには、表現 された配列 上 の各 位置 にマッチする可能 性 のある一連 のものが含 まれているが、パターンにも配列 にも挿入 や削除 の位置 はない。対照 的 に、配列 プロファイルは、挿入 や削除 を含 む類似 のパターンの集 まりを表 すスコアリングマトリックスの一種 である。- クラス
タンパク質 ドメインを、二 次 構造 の内容 や構成 に応 じて分類 するための用語 。LevittとChothia (1976)によって4つのクラスが最初 に認識 され、他 にもいくつかのクラスがSCOPデータベースに追加 されている。CATHデータベースでは、All-α 、All-β 、α -β の3つのクラスがあり、α -β クラスには交互 型 のα /β 構造 と分離 型 のα +β 構造 の両方 が含 まれる。- コア
折 りたたまれたタンパク質 分子 のうち、α ヘリックスとβ シートの疎水 性 内部 を構成 する部分 。コンパクトな構造 により、アミノ酸 の側 鎖 が十分 に接近 しているため、相互 作用 することができる。SCOPデータベースのようにタンパク質 構造 を比較 する場合 、コアとは、共通 のフォールドを持 つ、または同 じスーパーファミリーにあるほとんどの構造 に共通 する領域 である。構造 予測 では、進化 の過程 で保存 される可能 性 の高 い二 次 構造 の配列 をコアと定義 することがある。- ドメイン(
配列 の文脈 ) - ポリペプチド
鎖 上 の他 のセグメントの存在 にかかわらず、三 次元 構造 に折 りたたむことができるポリペプチド鎖 のセグメント。あるタンパク質 の別個 のドメインは、広範囲 に渡 って相互 作用 することもあれば、ポリペプチド鎖 の長 さのみで結合 することもある。複数 のドメインを持 つタンパク質 は、異 なる分子 との機能 的 な相互 作用 のために、これらのドメインを使用 する場合 がある。 - ファミリー(
配列 の文脈 ) 整列 させたときに50%以上 の同一 性 がある生化学 的 機能 が類似 したタンパク質 のグループ。この判断 基準 は、現在 もタンパク質 情報 資源 (PIR)で使用 されている。タンパク質 ファミリーは、異 なる生物 で同 じ機能 を持 つタンパク質 (オーソロガス配列 )で構成 されているが、遺伝子 の重複 や再 配列 に由来 する同 一 生物 のタンパク質 (パラロガス配列 )が含 まれる場合 もある。あるタンパク質 ファミリーの多重 整列 の結果 、タンパク質 の長 さ全体 で共通 レベルの類似 性 が見 られる場合 、PIRはそのファミリーを相 同 ファミリーと呼 んでいる。整列 した領域 は相 同 ドメインと呼 ばれ、この領域 は他 のファミリーと共有 されるいくつかの小 さな相 同 ドメインから構成 されている場合 がある。ファミリーは、配列 類似 性 の高 レベルまたは低 レベルに基 づいて、さらにサブファミリーに細分 化 されたり、スーパーファミリーにグループ化 される。SCOPデータベースでは1296ファミリーが、CATHデータベース(バージョン1.7ベータ版 )では1846ファミリーが報告 されている。:同 じ機能 を持 つタンパク質 の配列 を詳 しく調 べると、類似 性 が高 い配列 を共有 しているものがある。上記 の基準 では、これらは明 らかに同 じファミリーの一員 である。しかし、他 のファミリーメンバーとの配列 の類似 性 がほとんどないか、あるいはわずかであるものも見 られる。このような場合 、2つの遠縁 のファミリーメンバーAとCの間 のファミリー関係 は、AとCの両方 に有意 な類似 性 を共有 する追加 のファミリーメンバーBを見 つけることによって説明 されることがよくある。このように、BはAとCの間 をつなぐ役割 を果 たす。もう一 つの方法 は、遠 くのアライメントを調 べて、保存 度 が高 い一致 を探 すことである。同一 性 レベルが50%の場合 、タンパク質 は同 じ三 次元 構造 を持 つ可能 性 が高 く、配列 アライメントの同一 の原子 は構造 モデルにおいても約 1Åの範囲 で重 なり合 う。このように、あるファミリーで1つ目 のメンバーの構造 がわかっていれば、そのファミリーの別 のメンバーについても信頼 性 の高 い立体 構造 を予測 できる可能 性 があり、同一 性 レベルが高 いほど、その予測 の信頼 性 は高 くなる。タンパク質 の構造 モデリングは、アミノ酸 の置換 が三 次元 構造 のコアにどれだけ適合 するかを調 べることで行 うことができる。- ファミリー(
構造 の文脈 ) - FSSPデータベース(
構造 類似 タンパク質 ファミリーのデータベース)やDALI/FSSP Webサイトで使用 されているように、構造 的 に有意 なレベルで類似 しているが、必 ずしも有意 な配列 の類似 性 を持 たない2つの構造 。 折 りたたみ(フォールディング)構造 モチーフと同様 で、同 じ構成 の二 次 構造 単位 のより大 きな組 み合 わせを含 む。このように、同 じ折 りたたみを持 つタンパク質 は、二 次 構造 の組 み合 わせが同 じで、同 じようなループで結 ばれている。例 えば、いくつかの交互 α ヘリックスと平行 β -ストランドからなるロスマンフォールドがあげられる。SCOP、CATH、FSSPのデータベースでは、既知 のタンパク質 構造 が、構造 の複雑 さに応 じて階層 的 に分類 されていて、その基本 レベルは「フォールド(折 りたたみ)」が用 いられている。相 同 ドメイン(配列 の文脈 )一般 的 に配列 アラインメント法 によって見出 される拡張 配列 パターン。これは、整列 された配列 間 における共通 の進化 的 起源 を示 す。相 同 ドメインは一般 的 にモチーフよりも長 い。ドメインは、与 えられたタンパク質 配列 のすべてを含 むこともあれば、配列 の一部 のみを含 む場合 もある。ドメインの中 には複雑 なものもあり、進化 の過程 でいくつかの小 さな相 同 ドメインが結合 して大 きなドメインになったものもある。配列 全体 をカバーするドメインは、PIR(タンパク質 情報 資源 )によって相 同 ドメインと呼 ばれている。- モジュール
- 1つまたは
複数 のモチーフからなる保存 アミノ酸 パターンの領域 で、構造 または機能 の基本 単位 と考 えられているもの。モジュールの存在 は、タンパク質 をファミリーに分類 するのにも使用 されている。 - モチーフ(
配列 の文脈 ) - 2つ
以上 のタンパク質 に見 られる、保存 アミノ酸 パターン。Prositeカタログでは、モチーフとは、生化学 的 に同 じような活性 を持 つタンパク質 のグループに見 られるアミノ酸 パターンで、多 くの場合 、タンパク質 の活性 部位 の近 くにある。配列 モチーフデータベースの例 としては、PrositeカタログやStanford Motifs Databaseなどがある[2]。 - モチーフ(
構造 の文脈 ) - ポリペプチド
鎖 の隣接 する部分 が特定 の三 次元 構造 に折 りたたまれることによって生 じる、いくつかの二 次 構造 要素 の組 み合 わせである。たとえば、ヘリックス-ループ-ヘリックスのモチーフがある。構造 モチーフは、超 二 次 構造 や超 二 次 フォールドとも呼 ばれる。 位置 特異 的 スコアリングマトリックス(配列 の文脈 )- ギャップのない
多重 整列 における保存 領域 を表 す。マトリックスの各 列 は、多重 整列 の1列 に見 られるバリエーションを表 す。ウェイトマトリックスまたはスコアリングマトリックスとも呼 ばれる。 位置 特異 的 スコアリングマトリックス-3D (構造 の文脈 )同 じ構造 クラスに分類 されるタンパク質 のアライメントに見 られるアミノ酸 のバリエーションを表 す。マトリックスの列 は、整列 した構造 体 の1つのアミノ酸 位置 で見 つかったアミノ酸 のバリエーションを表 している。- プロファイル(
配列 の文脈 ) タンパク質 ファミリーの多重 整列 を表 すスコアリングマトリックス。プロファイルは、通常 、多重 整列 の中 で「よく保存 された領域 」から取得 される。プロファイルはマトリックスの形式 で、各 列 はアライメント内 の位置 を表 し、各行 はアミノ酸 の1つを表 す。マトリックスの値 は、各 アミノ酸 がアライメントの対応 する位置 にある可能 性 を示 す。プロファイルはターゲット配列 に沿 って移動 され、動的 計画 法 アルゴリズムによって最良 のスコアリング領域 を見 つだす。マッチング時 のギャップは許容 されており、このケースにはアミノ酸 がマッチしなかった場合 の負 のスコアであるギャップペナルティが含 まれる。配列 プロファイルは、隠 れマルコフモデルで表 すこともでき、プロファイルHMMと呼 ばれる。- プロファイル(
構造 の文脈 ) 既知 のタンパク質 構造 の連続 した位置 に、どのアミノ酸 がうまく適合 し、どのアミノ酸 がうまく適合 しないのかを表 すスコアリングマトリックス。プロファイルの列 は構造 内 の連続 した位置 を表 し、プロファイルの行 は20個 のアミノ酸 を表 している。配列 プロファイルと同様 に、構造 プロファイルもターゲット配列 に沿 って移動 され、動的 計画 法 アルゴリズムにより、可能 な限 り高 いアライメントスコアを見 つだす。ギャップが含 まれ、ペナルティを受 ける場合 がある。得 られたスコアは、対象 となるタンパク質 がそのような構造 をとる可能 性 を示 すものである。一 次 構造 タンパク質 の直 鎖 状 のアミノ酸 配列 のこと。化学 的 には、アミノ酸 がペプチド結合 で結合 したポリペプチド鎖 である。二 次 構造 - ポリペプチド
鎖 を構成 するアミノ酸 のC、O、NH基 間 の相互 作用 により、α ヘリックス、β シート、ターン、ループ、およびその他 の形態 が形成 され、三 次元 構造 への折 りたたみが促進 されること。 三 次 構造 三 次 構造 とは、ポリペプチド鎖 の二 次 構造 が折 り重 なってできた立体 的 な構造 または球状 の構造 のこと[1]。四 次 構造 複数 の独立 したポリペプチド鎖 からなるタンパク質 分子 の三 次元 構造 。- スーパーファミリー
遠 く離 れていても検出 可能 な配列 類似 性 によって関連 している、同 じまたは異 なる長 さのタンパク質 ファミリーのグループ。このように、あるスーパーファミリーのメンバーは、共通 の進化 的 起源 を持 っている。もともとはDayhoffが、スーパーファミリーであることの判断 基準 を、アライメントスコアに基 づいて、配列 が関連 していない可能 性 が10 6であると定義 した(Dayhoff et al. 1978)。配列 アライメントの同一 性 が低 いタンパク質 でも、納得 のゆく共通 の数 の構造 的 および機能 的 な特徴 を持 っていれば、同 じスーパーファミリーに分類 される。スーパーファミリータンパク質 は、三 次元 構造 のレベルでは共通 の折 りたたみなどの構造 的 特徴 を共有 するが、二 次 構造 の数 や配置 が異 なる場合 もある。 PIRリソースでは、同相 スーパーファミリー(homeomorphic superfamily)という言葉 を使用 して、配列 の端 から端 までを揃 えることができ、単一 の配列 相 同性 ドメイン(配列 全体 に広 がる類似 性 のある領域 )を共有 しているスーパーファミリーのことを指 す。このドメインは、他 のタンパク質 ファミリーやスーパーファミリーと共有 される、より小 さな相 同性 ドメインから構成 されている可能 性 もある。あるタンパク質 の配列 には、複数 のスーパーファミリーに属 するドメインが含 まれている可能 性 があり、複雑 な進化 の歴史 を示 しているが、多重 整列 全体 の類似 性 が認 められれば、配列 は1つの同相 スーパーファミリーにのみ割 り当 てられる。また、スーパーファミリーのアライメントには、アライメント内 またはアライメントの両 端 で整列 しない領域 が含 まれる場合 がある。対照 的 に、同 じファミリーの配列 は、アラインメント全体 を等 してうまく整列 する。
二 次 構造 の予測 [編集 ]
背景 [編集 ]
1960
歴史 的 展望 [編集 ]
もう
その他 の改善 [編集 ]
三 次 構造 の予測 [編集 ]
モデリング前 ステップ[編集 ]
Rosettaをはじめとするほとんどの
タンパク質 のde novoモデリング[編集 ]
エネルギーベースおよびフラグメントベースの手法 [編集 ]
de novoまたはab initioの
2009
進化 的 共 分散 による三 次元 接触 の予測 [編集 ]
1990
2011
タンパク質 の比較 モデリング[編集 ]
相 同性 モデリングは、相 同性 の高 い2つのタンパク質 は非常 に似通 った構造 をもっているという合理 的 な前提 に基 づいている。タンパク質 のフォールディングはアミノ酸 配列 よりも進化 的 に保存 されているため、配列 アライメントによってターゲット(構造 が未知 のタンパク質 )とテンプレートの関係 が識別 できる場合 には、非常 に遠 い関係 にあるテンプレート上 でターゲット配列 を合理 的 な精度 でモデル化 することができる。比較 モデリングの主 なボトルネックは、既知 の良好 なアライメントによる構造 予測 のエラーではなく、アライメントの難 しさから生 じると考 えられている[45]。当然 のことながら、相 同性 モデリングは、ターゲットとテンプレートの配列 が類似 している場合 に最 も正確 になる。タンパク質 スレッディング[46]は、未知 の構造 のアミノ酸 配列 を、解明 済 みの構造 のデータベースに対 して検索 するものである。いずれの場合 も、スコアリング関数 を用 いて、配列 と構造 の適合 性 を評価 し、可能 性 が高 い三 次元 モデルを作成 する。この種 の手法 は、三 次元 構造 と直線 的 なタンパク質 配列 の間 の適合 性 解析 であることから、「3D-1Dフォールド認識 法 」とも呼 ばれている。さらにまた、与 えられた構造 と大 規模 な配列 のデータベースとの適合 性 を評価 することで、どの配列 が与 えられたフォールディングを生 み出 す可能 性 があるかを予測 し、「逆 フォールディング検索 」を行 う方法 も生 み出 した。
側 鎖 コンフォメーションのモデリング[編集 ]
これらの
ほとんどのソフトウェアで
四 次 構造 の予測 [編集 ]
ソフトウェア[編集 ]
自動 構造 予測 サーバの評価 [編集 ]
CASPは、1994
CAMEO3Dは、
参照 項目 [編集 ]
タンパク質 設計 タンパク質 機能 予測 タンパク質 構造 予測 ソフトウェアの一覧 - de novo
タンパク質 構造 予測 分子 設計 ソフトウェア分子 力学 モデリング用 ソフトの比較 (英語 版 )生体 システムのモデリングタンパク質 フラグメントライブラリ格子 タンパク質 統計 ポテンシャルタンパク質 円 二 色 性 データバンク
脚注 [編集 ]
- ^ a b c d e f g h Mount DM (2004). Bioinformatics: Sequence and Genome Analysis. 2. Cold Spring Harbor Laboratory Press. ISBN 978-0-87969-712-9
- ^ Huang JY, Brutlag DL (January 2001). “The EMOTIF database”. Nucleic Acids Research 29 (1): 202–4. doi:10.1093/nar/29.1.202. PMC 29837. PMID 11125091.
- ^ Pirovano W, Heringa J (2010). “Protein secondary structure prediction”. Data Mining Techniques for the Life Sciences. Methods in Molecular Biology. 609. pp. 327–48. doi:10.1007/978-1-60327-241-4_19. ISBN 978-1-60327-240-7. PMID 20221928
- ^ Guzzo AV (November 1965). “The influence of amino-acid sequence on protein structure”. Biophysical Journal 5 (6): 809–22. Bibcode: 1965BpJ.....5..809G. doi:10.1016/S0006-3495(65)86753-4. PMC 1367904. PMID 5884309.
- ^ Prothero JW (May 1966). “Correlation between the distribution of amino acids and alpha helices”. Biophysical Journal 6 (3): 367–70. Bibcode: 1966BpJ.....6..367P. doi:10.1016/S0006-3495(66)86662-6. PMC 1367951. PMID 5962284.
- ^ Schiffer M, Edmundson AB (March 1967). “Use of helical wheels to represent the structures of proteins and to identify segments with helical potential”. Biophysical Journal 7 (2): 121–35. Bibcode: 1967BpJ.....7..121S. doi:10.1016/S0006-3495(67)86579-2. PMC 1368002. PMID 6048867.
- ^ Kotelchuck D, Scheraga HA (January 1969). “The influence of short-range interactions on protein onformation. II. A model for predicting the alpha-helical regions of proteins”. Proceedings of the National Academy of Sciences of the United States of America 62 (1): 14–21. Bibcode: 1969PNAS...62...14K. doi:10.1073/pnas.62.1.14. PMC 285948. PMID 5253650.
- ^ Lewis PN, Go N, Go M, Kotelchuck D, Scheraga HA (April 1970). “Helix probability profiles of denatured proteins and their correlation with native structures”. Proceedings of the National Academy of Sciences of the United States of America 65 (4): 810–5. Bibcode: 1970PNAS...65..810L. doi:10.1073/pnas.65.4.810. PMC 282987. PMID 5266152.
- ^ Froimowitz M, Fasman GD (1974). “Prediction of the secondary structure of proteins using the helix-coil transition theory”. Macromolecules 7 (5): 583–9. Bibcode: 1974MaMol...7..583F. doi:10.1021/ma60041a009. PMID 4371089.
- ^ a b Dor O, Zhou Y (March 2007). “Achieving 80% ten-fold cross-validated accuracy for secondary structure prediction by large-scale training”. Proteins 66 (4): 838–45. doi:10.1002/prot.21298. PMID 17177203.
- ^ Chou PY, Fasman GD (January 1974). “Prediction of protein conformation”. Biochemistry 13 (2): 222–45. doi:10.1021/bi00699a002. PMID 4358940.
- ^ Garnier J, Osguthorpe DJ, Robson B (March 1978). “Analysis of the accuracy and implications of simple methods for predicting the secondary structure of globular proteins”. Journal of Molecular Biology 120 (1): 97–120. doi:10.1016/0022-2836(78)90297-8. PMID 642007.
- ^ a b Pham TH, Satou K, Ho TB (April 2005). “Support vector machines for prediction and analysis of beta and gamma-turns in proteins”. Journal of Bioinformatics and Computational Biology 3 (2): 343–58. doi:10.1142/S0219720005001089. PMID 15852509.
- ^ Zhang Q, Yoon S, Welsh WJ (May 2005). “Improved method for predicting beta-turn using support vector machine”. Bioinformatics 21 (10): 2370–4. doi:10.1093/bioinformatics/bti358. PMID 15797917.
- ^ Zimmermann O, Hansmann UH (December 2006). “Support vector machines for prediction of dihedral angle regions”. Bioinformatics 22 (24): 3009–15. doi:10.1093/bioinformatics/btl489. PMID 17005536.
- ^ Kuang R, Leslie CS, Yang AS (July 2004). “Protein backbone angle prediction with machine learning approaches”. Bioinformatics 20 (10): 1612–21. doi:10.1093/bioinformatics/bth136. PMID 14988121.
- ^ Faraggi E, Yang Y, Zhang S, Zhou Y (November 2009). “Predicting continuous local structure and the effect of its substitution for secondary structure in fragment-free protein structure prediction”. Structure 17 (11): 1515–27. doi:10.1016/j.str.2009.09.006. PMC 2778607. PMID 19913486.
- ^ Zhong L, Johnson WC (May 1992). “Environment affects amino acid preference for secondary structure”. Proceedings of the National Academy of Sciences of the United States of America 89 (10): 4462–5. Bibcode: 1992PNAS...89.4462Z. doi:10.1073/pnas.89.10.4462. PMC 49102. PMID 1584778.
- ^ Macdonald JR, Johnson WC (June 2001). “Environmental features are important in determining protein secondary structure”. Protein Science 10 (6): 1172–7. doi:10.1110/ps.420101. PMC 2374018. PMID 11369855.
- ^ Costantini S, Colonna G, Facchiano AM (April 2006). “Amino acid propensities for secondary structures are influenced by the protein structural class”. Biochemical and Biophysical Research Communications 342 (2): 441–51. doi:10.1016/j.bbrc.2006.01.159. PMID 16487481.
- ^ Marashi SA, Behrouzi R, Pezeshk H (January 2007). “Adaptation of proteins to different environments: a comparison of proteome structural properties in Bacillus subtilis and Escherichia coli”. Journal of Theoretical Biology 244 (1): 127–32. doi:10.1016/j.jtbi.2006.07.021. PMID 16945389.
- ^ Costantini S, Colonna G, Facchiano AM (October 2007). “PreSSAPro: a software for the prediction of secondary structure by amino acid properties”. Computational Biology and Chemistry 31 (5–6): 389–92. doi:10.1016/j.compbiolchem.2007.08.010. PMID 17888742.
- ^ Adamczak R, Porollo A, Meller J (May 2005). “Combining prediction of secondary structure and solvent accessibility in proteins”. Proteins 59 (3): 467–75. doi:10.1002/prot.20441. PMID 15768403.
- ^ Momen-Roknabadi A, Sadeghi M, Pezeshk H, Marashi SA (August 2008). “Impact of residue accessible surface area on the prediction of protein secondary structures”. BMC Bioinformatics 9: 357. doi:10.1186/1471-2105-9-357. PMC 2553345. PMID 18759992.
- ^ Lakizadeh A, Marashi SA (2009). “Addition of contact number information can improve protein secondary structure prediction by neural networks”. Excli J. 8: 66–73.
- ^ Dorn, Márcio; e Silva, Mariel Barbachan; Buriol, Luciana S.; Lamb, Luis C. (2014-12-01). “Three-dimensional protein structure prediction: Methods and computational strategies” (
英語 ). Computational Biology and Chemistry 53: 251–276. doi:10.1016/j.compbiolchem.2014.10.001. ISSN 1476-9271. PMID 25462334. - ^ a b c Zhang Y (June 2008). “Progress and challenges in protein structure prediction”. Current Opinion in Structural Biology 18 (3): 342–8. doi:10.1016/j.sbi.2008.02.004. PMC 2680823. PMID 18436442.
- ^ Ovchinnikov S, Kim DE, Wang RY, Liu Y, DiMaio F, Baker D (September 2016). “Improved de novo structure prediction in CASP11 by incorporating coevolution information into Rosetta”. Proteins 84 Suppl 1: 67–75. doi:10.1002/prot.24974. PMC 5490371. PMID 26677056.
- ^ Hong SH, Joo K, Lee J (November 2018). “ConDo: Protein domain boundary prediction using coevolutionary information”. Bioinformatics 35 (14): 2411–2417. doi:10.1093/bioinformatics/bty973. PMID 30500873.
- ^ Wollacott AM, Zanghellini A, Murphy P, Baker D (February 2007). “Prediction of structures of multidomain proteins from structures of the individual domains”. Protein Science 16 (2): 165–75. doi:10.1110/ps.062270707. PMC 2203296. PMID 17189483.
- ^ Xu D, Jaroszewski L, Li Z, Godzik A (July 2015). “AIDA: ab initio domain assembly for automated multi-domain protein structure prediction and domain-domain interaction prediction”. Bioinformatics 31 (13): 2098–105. doi:10.1093/bioinformatics/btv092. PMC 4481839. PMID 25701568.
- ^ Shaw DE, Dror RO, Salmon JK, Grossman JP, Mackenzie KM, Bank JA, Young C, Deneroff MM, Batson B, Bowers KJ, Chow E (2009). Millisecond-scale molecular dynamics simulations on Anton. Proceedings of the Conference on High Performance Computing Networking, Storage and Analysis - SC '09. p. 1. doi:10.1145/1654059.1654126. ISBN 9781605587448。
- ^ Pierce LC, Salomon-Ferrer R, de Oliveira CA, McCammon JA, Walker RC (September 2012). “Routine Access to Millisecond Time Scale Events with Accelerated Molecular Dynamics”. Journal of Chemical Theory and Computation 8 (9): 2997–3002. doi:10.1021/ct300284c. PMC 3438784. PMID 22984356.
- ^ Kmiecik S, Gront D, Kolinski M, Wieteska L, Dawid AE, Kolinski A (July 2016). “Coarse-Grained Protein Models and Their Applications”. Chemical Reviews 116 (14): 7898–936. doi:10.1021/acs.chemrev.6b00163. PMID 27333362.
- ^ Cheung NJ, Yu W (November 2018). “De novo protein structure prediction using ultra-fast molecular dynamics simulation”. PLOS ONE 13 (11): e0205819. Bibcode: 2018PLoSO..1305819C. doi:10.1371/journal.pone.0205819. PMC 6245515. PMID 30458007.
- ^ Göbel U, Sander C, Schneider R, Valencia A (April 1994). “Correlated mutations and residue contacts in proteins”. Proteins 18 (4): 309–17. doi:10.1002/prot.340180402. PMID 8208723.
- ^ Taylor WR, Hatrick K (March 1994). “Compensating changes in protein multiple sequence alignments”. Protein Engineering 7 (3): 341–8. doi:10.1093/protein/7.3.341. PMID 8177883.
- ^ Neher E (January 1994). “How frequent are correlated changes in families of protein sequences?”. Proceedings of the National Academy of Sciences of the United States of America 91 (1): 98–102. Bibcode: 1994PNAS...91...98N. doi:10.1073/pnas.91.1.98. PMC 42893. PMID 8278414.
- ^ Marks DS, Colwell LJ, Sheridan R, Hopf TA, Pagnani A, Zecchina R, Sander C (2011). “Protein 3D structure computed from evolutionary sequence variation”. PLOS ONE 6 (12): e28766. Bibcode: 2011PLoSO...628766M. doi:10.1371/journal.pone.0028766. PMC 3233603. PMID 22163331.
- ^ Burger L, van Nimwegen E (January 2010). “Disentangling direct from indirect co-evolution of residues in protein alignments”. PLOS Computational Biology 6 (1): e1000633. Bibcode: 2010PLSCB...6E0633B. doi:10.1371/journal.pcbi.1000633. PMC 2793430. PMID 20052271.
- ^ Morcos F, Pagnani A, Lunt B, Bertolino A, Marks DS, Sander C, Zecchina R, Onuchic JN, Hwa T, Weigt M (December 2011). “Direct-coupling analysis of residue coevolution captures native contacts across many protein families”. Proceedings of the National Academy of Sciences of the United States of America 108 (49): E1293-301. arXiv:1110.5223. Bibcode: 2011PNAS..108E1293M. doi:10.1073/pnas.1111471108. PMC 3241805. PMID 22106262.
- ^ Nugent T, Jones DT (June 2012). “Accurate de novo structure prediction of large transmembrane protein domains using fragment-assembly and correlated mutation analysis”. Proceedings of the National Academy of Sciences of the United States of America 109 (24): E1540-7. Bibcode: 2012PNAS..109E1540N. doi:10.1073/pnas.1120036109. PMC 3386101. PMID 22645369.
- ^ Hopf TA, Colwell LJ, Sheridan R, Rost B, Sander C, Marks DS (June 2012). “Three-dimensional structures of membrane proteins from genomic sequencing”. Cell 149 (7): 1607–21. doi:10.1016/j.cell.2012.04.012. PMC 3641781. PMID 22579045.
- ^ Jin, Shikai; Chen, Mingchen; Chen, Xun; Bueno, Carlos; Lu, Wei; Schafer, Nicholas P.; Lin, Xingcheng; Onuchic, José N. et al. (9 June 2020). “Protein Structure Prediction in CASP13 Using AWSEM-Suite”. Journal of Chemical Theory and Computation 16 (6): 3977–3988. doi:10.1021/acs.jctc.0c00188. PMID 32396727.
- ^ Zhang Y, Skolnick J (January 2005). “The protein structure prediction problem could be solved using the current PDB library”. Proceedings of the National Academy of Sciences of the United States of America 102 (4): 1029–34. Bibcode: 2005PNAS..102.1029Z. doi:10.1073/pnas.0407152101. PMC 545829. PMID 15653774.
- ^ Bowie JU, Lüthy R, Eisenberg D (July 1991). “A method to identify protein sequences that fold into a known three-dimensional structure”. Science 253 (5016): 164–70. Bibcode: 1991Sci...253..164B. doi:10.1126/science.1853201. PMID 1853201.
- ^ Dunbrack RL (August 2002). “Rotamer libraries in the 21st century”. Current Opinion in Structural Biology 12 (4): 431–40. doi:10.1016/S0959-440X(02)00344-5. PMID 12163064.
- ^ Ponder JW, Richards FM (February 1987). “Tertiary templates for proteins. Use of packing criteria in the enumeration of allowed sequences for different structural classes”. Journal of Molecular Biology 193 (4): 775–91. doi:10.1016/0022-2836(87)90358-5. PMID 2441069.
- ^ Lovell SC, Word JM, Richardson JS, Richardson DC (August 2000). “The penultimate rotamer library”. Proteins 40 (3): 389–408. doi:10.1002/1097-0134(20000815)40:3<389::AID-PROT50>3.0.CO;2-2. PMID 10861930.
- ^ Shapovalov MV, Dunbrack RL (June 2011). “A smoothed backbone-dependent rotamer library for proteins derived from adaptive kernel density estimates and regressions”. Structure 19 (6): 844–58. doi:10.1016/j.str.2011.03.019. PMC 3118414. PMID 21645855.
- ^ Chen VB, Arendall WB, Headd JJ, Keedy DA, Immormino RM, Kapral GJ, Murray LW, Richardson JS, Richardson DC (January 2010). “MolProbity: all-atom structure validation for macromolecular crystallography”. Acta Crystallographica. Section D, Biological Crystallography 66 (Pt 1): 12–21. doi:10.1107/S0907444909042073. PMC 2803126. PMID 20057044.
- ^ Bower MJ, Cohen FE, Dunbrack RL (April 1997). “Prediction of protein side-chain rotamers from a backbone-dependent rotamer library: a new homology modeling tool”. Journal of Molecular Biology 267 (5): 1268–82. doi:10.1006/jmbi.1997.0926. PMID 9150411.
- ^ Voigt CA, Gordon DB, Mayo SL (June 2000). “Trading accuracy for speed: A quantitative comparison of search algorithms in protein sequence design”. Journal of Molecular Biology 299 (3): 789–803. doi:10.1006/jmbi.2000.3758. PMID 10835284.
- ^ Krivov GG, Shapovalov MV, Dunbrack RL (December 2009). “Improved prediction of protein side-chain conformations with SCWRL4”. Proteins 77 (4): 778–95. doi:10.1002/prot.22488. PMC 2885146. PMID 19603484.
- ^ Battey JN, Kopp J, Bordoli L, Read RJ, Clarke ND, Schwede T (2007). “Automated server predictions in CASP7”. Proteins 69 Suppl 8 (Suppl 8): 68–82. doi:10.1002/prot.21761. PMID 17894354.
推薦 文献 [編集 ]
- Majorek K, Kozlowski L, Jakalski M, Bujnicki JM (December 18, 2008). “Chapter 2: First Steps of Protein Structure Prediction”. In Bujnicki, J. Prediction of Protein Structures, Functions, and Interactions. John Wiley & Sons, Ltd.. pp. 39–62. doi:10.1002/9780470741894.ch2. ISBN 9780470517673
- Baker D, Sali A (October 2001). “Protein structure prediction and structural genomics”. Science 294 (5540): 93–6. Bibcode: 2001Sci...294...93B. doi:10.1126/science.1065659. PMID 11588250.
- Kelley LA, Sternberg MJ (2009). “Protein structure prediction on the Web: a case study using the Phyre server”. Nature Protocols 4 (3): 363-371. doi:10.1038/nprot.2009.2. hdl:10044/1/18157. PMID 19247286.
- Kryshtafovych A, Fidelis K (April 2009). “Protein structure prediction and model quality assessment”. Drug Discovery Today 14 (7–8): 386-393. doi:10.1016/j.drudis.2008.11.010. PMC 2808711. PMID 19100336.
- Qu X, Swanson R, Day R, Tsai J (June 2009). “A guide to template based structure prediction”. Current Protein & Peptide Science 10 (3): 270-285. doi:10.2174/138920309788452182. PMID 19519455.
- Daga PR, Patel RY, Doerksen RJ (2010). “Template-based protein modeling: recent methodological advances”. Current Topics in Medicinal Chemistry 10 (1): 84–94. doi:10.2174/156802610790232314. PMC 5943704. PMID 19929829.
- Fiser, A. (2010). “Template-based protein structure modeling”. Computational Biology. Methods in Molecular Biology. 673. pp. 73–94. doi:10.1007/978-1-60761-842-3_6. ISBN 978-1-60761-841-6. PMC 4108304. PMID 20835794
- Cozzetto D, Tramontano A (December 2008). “Advances and pitfalls in protein structure prediction”. Current Protein & Peptide Science 9 (6): 567–77. doi:10.2174/138920308786733958. PMID 19075747.
- Nayeem A, Sitkoff D, Krystek S (April 2006). “A comparative study of available software for high-accuracy homology modeling: from sequence alignments to structural models”. Protein Science 15 (4): 808–24. doi:10.1110/ps.051892906. PMC 2242473. PMID 16600967.
外部 リンク[編集 ]
- CASP experiments home page
- ExPASy Proteomics tools -
予測 ツールとサーバの一覧
