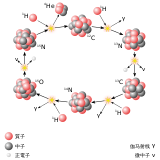
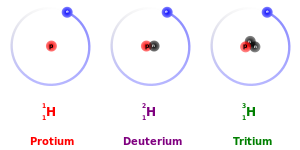
氫 元素 げんそ 的 てき 三 さん 種 しゅ 天然 てんねん 同位 どうい 素 もと 三種 さんしゅ 同位 どうい 素 もと 都 と 有 ゆう 一 いち 個 こ 質 しつ 子 こ 因 いん 是 ぜ 原子 げんし 由 よし 左 ひだり 至 いたり 右 みぎ 的 てき 同位 どうい 素 もと 分別 ふんべつ 為 ため 具有 ぐゆう 個 こ 中子 なかご 的 てき 氕 (1 H具有 ぐゆう 1個 いっこ 中子 なかご 的 てき 氘 (2 D和 かず 具有 ぐゆう 個 こ 中子 なかご 的 てき 氚 (3 T同位 どうい 素 もと 英語 えいご Isotope ),又 また 稱 たたえ 同位 どうい 素 もと 核種 かくしゅ [1] 英語 えいご Isotopic nuclides [2] 是 ぜ 指 ゆび 同一 どういつ 化學 かがく 元素 げんそ 之 これ 下 か 的 てき 不同 ふどう 核種 かくしゅ 同 どう 質 しつ 子 こ 數 すう 目 もく 即 そく 原子 げんし 序 じょ 數 すう 但 ただし 中子 なかご 數 すう 目 もく 不同 ふどう 故 こ 質量 しつりょう 數 すう 不同 ふどう 由 よし 種 しゅ 屬 ぞく 一 いち 種 しゅ 化學 かがく 元素 げんそ 在 ざい 化學 かがく 元素 げんそ 週 しゅう 期 き 表 ひょう 同 どう 一 いち 個 こ 位置 いち 因 いん 名 めい [1]
例 れい 自然 しぜん 界 かい 的 てき 氫 元素 げんそ 由 ゆかり 氕 (1 H氘 (2 D和 わ 氚 (3 T三種 さんしゅ 核種 かくしゅ 組成 そせい 原子核 げんしかく 中 ちゅう 都 と 有 ゆう 1個 いっこ 質 しつ 子 こ 但 ただし 是 ぜ 的 てき 原子核 げんしかく 中 ちゅう 分別 ふんべつ 有 ゆう 個 こ 中子 なかご 1個 いっこ 中子 なかご 個 こ 中子 なかご 質量 しつりょう 數 すう 分別 ふんべつ 為 ため 所以 ゆえん 三 さん 者 しゃ 同位 どうい 素 もと
同 どう 但 ただし 彼此 ひし 的 てき 核 かく 性 せい 各 かく 不 ふ 相 あい 同 どう 物理 ぶつり 性質 せいしつ 也有 やゆう 差異 さい [3]
同位 どうい 素的 すてき 英文 えいぶん 是 ぜ 由 ゆかり 希 まれ 詞 し 根 ね 意 い 為 ため 相 あい 同 どう 和 かず 意 い 為 ため 地方 ちほう 組成 そせい 意思 いし 是 ぜ 同 どう 一 いち 個 こ 地方 ちほう [4] 由 ゆかり 蘇 そ 格 かく 蘭 らん 醫 い 生 せい 兼 けん 作家 さっか 瑪格麗 うらら 特 とく 托 たく 德 とく 年 ねん 創造 そうぞう 並 なみ 在 ざい 與 あずか 英國 えいこく 化學 かがく 家 か 弗 どる 雷 かみなり 德 とく 里 さと 克 かつ 索 さく 迪 すすむ 談話 だんわ 時 じ 提出 ていしゅつ [5]
同位 どうい 素 もと 與 あずか 核種 かくしゅ [ 编辑 ] 核種 かくしゅ 是 ぜ 指 ゆび 原子 げんし 的 てき 種類 しゅるい 由 ゆかり 原子核 げんしかく 子 こ 中子 なかご 的 てき 數量 すうりょう 的 てき 能 のう 態 たい 作 さく 區分 くぶん [1] 例 れい 碳-13 是 ぜ 具有 ぐゆう 個 こ 質 しつ 子 こ 和 わ 個 こ 中子 なかご 的 てき 核種 かくしゅ 核種 かくしゅ 在 ざい 概念 がいねん 上 じょう 強調 きょうちょう 原子 げんし 的 てき 核 かく 性質 せいしつ 化學 かがく 性質 せいしつ 位 い 素的 すてき 概念 がいねん 則 そく 是 ぜ 將 しょう 所有 しょゆう 原子 げんし 依 よ 所屬 しょぞく 元素 げんそ 進行 しんこう 分類 ぶんるい 由 ゆかり 原子核 げんしかく 中 ちゅう 的 てき 質 しつ 子 こ 數 すう 界 かい 定 じょう 因 いん 加 か 強調 きょうちょう 原子 げんし 的 てき 化學 かがく 性質 せいしつ 中子 なかご 數 すう 對 たい 原子 げんし 的 てき 核 かく 性質 せいしつ 有 ゆう 的 てき 影響 えいきょう 但 ただし 對 たい 大 だい 多數 たすう 原子 げんし 的 てき 化學 かがく 性質 せいしつ 之 の 影響 えいきょう 可 か 忽 ゆるがせ 略 りゃく 不 ふ 計 けい 對 たい 輕 けい 的 てき 元素 げんそ 中子 なかご 數 すう 與 あずか 質 しつ 子 こ 數 すう 之 これ 比 ひ 在 ざい 同位 どうい 素之 もとゆき 間 あいだ 變化 へんか 對 たい 學 がく 性質 せいしつ 的 てき 影響 えいきょう 通常 つうじょう 十 じゅう 分 ふん 微小 びしょう
同位 どうい 素 もと 概念 がいねん 上 じょう 強調 きょうちょう 質 しつ 子 こ 數 すう 相 そう 同 どう 量 りょう 數 すう 中子 なかご 數 すう 不同 ふどう 的 てき 原子 げんし 類別 るいべつ 例 れい 12 C13 C14 C的 てき 質 しつ 子 こ 數 すう 皆 みな 為 ため 彼此 ひし 同位 どうい 素 もと [6] 40 Ar40 K40 Ca的 てき 質量 しつりょう 數 すう 皆 みな 為 ため 同 どう 量 りょう 素 もと [7] 又 また 稱 たたえ 同 どう 量 りょう 素 もと 38 Ar39 K40 Ca的中 てきちゅう 子 こ 數 すう 皆 みな 為 ため 同 どう 中子 なかご 素 もと 又 また 稱 たたえ 同 どう 中子 なかご 異 こと 位 い 素 もと 至 いたり 種 しゅ 一 いち 詞 し 則 そく 可用 かよう 稱呼 しょうこ 任 にん 何 なん 原子核 げんしかく 構造 こうぞう 或 ある 所 ところ 處 しょ 能 のう 態 たい 不同 ふどう 的 てき 原子 げんし 種類 しゅるい 子 こ 數 すう 或 ある 中子 なかご 數 すう 不同 ふどう 的 てき 原子 げんし 皆 みな 視 し 為 ため 不同 ふどう 的 てき 核種 かくしゅ [1] 然 しか 由 ゆかり 位 い 素 もと 比 ひ 核種 かくしゅ 在 ざい 核 かく 技術 ぎじゅつ 和 わ 核 かく 醫學 いがく 等 とう 許多 きょた 領域 りょういき 中 ちゅう 常用 じょうよう 同位 どうい 素 もと 指 ゆび 代任 だいにん 何 なん 具有 ぐゆう 特定 とくてい 質 しつ 子 こ 數 すう 中子 なかご 數 すう 的 てき 原子 げんし 種類 しゅるい 在 ざい 概念 がいねん 語意 ごい 上 じょう 使用 しよう 核種 かくしゅ 更 さら 為 ため 合 あい 適 てき
命名 めいめい 法 ほう 號 ごう [ 编辑 ] 同位 どうい 素 もと 核種 かくしゅ 的 てき 名稱 めいしょう 通常 つうじょう 所屬 しょぞく 元素 げんそ 加 か 上 じょう 量 りょう 數 すう 來 らい 表示 ひょうじ 例 れい 氦-3 、氦-4 、碳-12 、碳-14 、鈾-235 、鈾-238 等 ひとし [8] 當 とう 使用 しよう 化學 かがく 符號 ふごう 表示 ひょうじ 同位 どうい 素 もと 時 じ 通常 つうじょう 使用 しよう
Z
A
E
N
{\displaystyle _{Z}^{A}E_{N}}
的 てき 形式 けいしき 為 ため 位 い 素 もと 所屬 しょぞく 元素 げんそ 的 てき 化學 かがく 符號 ふごう 氘 和 わ 氚 這二種同位素有自己的符號);Z為 ため 位 い 素的 すてき 質 しつ 子 こ 數 すう 即 そく 原子 げんし 序 じょ 數 すう 為 ため 位 い 素的 すてき 質量 しつりょう 數 すう 即 そく 核 かく 子 こ 數 かず 質 しつ 子 こ 數 すう 和 わ 中子 なかご 數 すう 之 の 和 わ 為 ため 位 い 素的 すてき 中子 なかご 數 すう 例 れい 3 He4 He12 C14 C235 U238 U由 よし 同位 どうい 素的 すてき 所屬 しょぞく 元素 げんそ 便 びん 可 か 推知 すいち 子 こ 數 すう 因 いん 符號 ふごう 表示 ひょうじ 同位 どうい 素 もと 時 じ 通常 つうじょう 只 ただ 會 かい 標的 ひょうてき 質量 しつりょう 數 すう 省略 しょうりゃく 下 か 標的 ひょうてき 質 しつ 子 こ 數 すう 3 He4 He12 C14 C235 U238 U若 わか 在 ざい 同位 どうい 素 もと 符號 ふごう 的 てき 質量 しつりょう 數 すう 後 ご 加 か 上 じょう 字母 じぼ 則 のり 表示 ひょうじ 位 い 素的 すてき 同 どう 核 かく 異 い 其原 そのはら 子 こ 核 かく 處 しょ 高 だか 能 のう 階 かい 的 てき 亞 あ 但 ただし 半 はん 衰 おとろえ 期 き 比 ひ 一般 いっぱん 的 てき 激發 げきはつ 態 たい 原子核 げんしかく 要 よう 長 ちょう 通常 つうじょう 達 たち 到 いた 倍 ばい 的 てき 時間 じかん 例 れい 99m Tc鎝-99m )、180m Ta等 とう 當 とう 則 のり 使用 しよう 等 とう 發 はつ 能 のう 量 りょう 從 したがえ 低 てい 到 いた 高 こう 進行 しんこう 標記 ひょうき 177m2 Hf等 とう
穩定性 せい [ 编辑 ] 每 まい 由 よし 原子核 げんしかく 中 ちゅう 不同 ふどう 數 すう 目的 もくてき 質 しつ 子 こ 和 かず 中子 なかこ 的 てき 組合 くみあい 會 かい 影響 えいきょう 定性 ていせい 因 いん 種 しゅ 同位 どうい 素的 すてき 核 かく 性 せい 各 かく 不 ふ 相 あい 同 どう
目前 もくぜん 已 やめ 知的 ちてき 大 だい 多數 たすう 同位 どうい 素 もと 原子核 げんしかく 皆 みな 不穩 ふおん 定 じょう 具有 ぐゆう 放射 ほうしゃ 性 せい 會 かい 自發 じはつ 性 せい 地 ち 放出 ほうしゅつ 游 ゆう 離 はなれ 輻射 ふくしゃ 並 なみ 衰 おとろえ 變成 へんせい 核種 かくしゅ 稱 たたえ 為 ため 放射 ほうしゃ 性 せい 同位 どうい 素 もと 例 れい 碳-14 、鉀-40 、鈷-60 和 わ 碘-131 等 ひとし 若 わか 某 ぼう 元素 げんそ 的 てき 所有 しょゆう 同位 どうい 素 もと 都 と 具有 ぐゆう 放射 ほうしゃ 性 せい 則 のり 元素 げんそ 會 かい 被 ひ 稱 しょう 為 ため 放射 ほうしゃ 性 せい 元素 げんそ 鈾 、鐳 和 わ 氡 等 ひとし 每 まい 種 たね 放射 ほうしゃ 性 せい 同位 どうい 素的 すてき 核 かく 性 せい 各 かく 不 ふ 相 あい 同 どう 因 いん 發生 はっせい 衰 おとろえ 變 へん 的 てき 半 はん 衰 おとろえ 期 き 也有 やゆう 長 ちょう 有 ゆう 短 たん 原子核 げんしかく 越 えつ 不穩 ふおん 定 じょう 的 てき 同位 どうい 素 もと 半 はん 衰 おとろえ 期 き 越 えつ 短 たん 放射 ほうしゃ 性 せい 越 えつ 強 きょう 目前 もくぜん 已 やめ 發現 はつげん 的 てき 放射 ほうしゃ 性 せい 同位 どうい 素 もと 超過 ちょうか 種 しゅ [9] 大 だい 部分 ぶぶん 不 ふ 存在 そんざい 自然 しぜん 界 かい 只 ただ 能 のう 人工 じんこう 合成 ごうせい 的 てき 方式 ほうしき 生成 せいせい 稱 たたえ 為 ため 人造 じんぞう 放射 ほうしゃ 性 せい 同位 どうい 素 もと 至 いたり 天然 てんねん 存在 そんざい 的 てき 放射 ほうしゃ 性 せい 同位 どうい 素 もと 則 のり 包括 ほうかつ 半 はん 衰 おとろえ 期 き 極 きょく 長 ちょう 的 てき 原始 げんし 放射 ほうしゃ 性 せい 核種 かくしゅ 原始 げんし 放射 ほうしゃ 性 せい 核種 かくしゅ 衰 おとろえ 變 へん 生成 せいせい 的 てき 次生 つぎお 天然 てんねん 放射 ほうしゃ 性 せい 核種 かくしゅ 天然 てんねん 核 かく 反應 はんのう 產 さん 生 せい 的 てき 宇生 うぶ 放射 ほうしゃ 性 せい 核種 かくしゅ 核 かく 生成 せいせい 放射 ほうしゃ 性 せい 核種 かくしゅ
原子核 げんしかく 不 ふ 會 かい 發生 はっせい 放射 ほうしゃ 性 せい 衰 おとろえ 變 へん 的 てき 同位 どうい 素 もと 則 そく 稱 たたえ 為 ため 穩定同位 どうい 素 もと ,共有 きょうゆう 種 しゅ 皆 みな 自然 しぜん 存在 そんざい 地球 ちきゅう 上 じょう 原子 げんし 序 じょ 小 しょう 鉍 之 これ 前 まえ 的 てき 元素 げんそ 中 ちゅう 除 じょ 了 りょう 鎝 和 わ 鉕 外 そと 都 と 具有 ぐゆう 至 いたり 少 しょう 只 ただ 有 ゆう 單一 たんいつ 同位 どうい 素 もと 元素 げんそ 的 てき 元素 げんそ 則 そく 有 ゆう 超過 ちょうか 錫 すず 有 ゆう 種 しゅ 同位 どうい 素 もと 是 ぜ 具有 ぐゆう 最多 さいた 種 しゅ 同位 どうい 素的 すてき 元素 げんそ 同位 どうい 素 もと 由 よし 會 かい 衰 おとろえ 變成 へんせい 同位 どうい 素 もと 自 じ 恆星 こうせい 核 かく 合成 ごうせい 過程 かてい 誕生 たんじょう 後 ご 能 のう 定 じょう 的 てき 量 りょう 恆久 こうきゅう 存在 そんざい 因 いん 構成 こうせい 了 りょう 現今 げんこん 自然 しぜん 界 かい 中絕 ちゅうぜつ 大 だい 多數 たすう 的 てき 物質 ぶっしつ 大 だい 多數 たすう 元素 げんそ 在 ざい 地球 ちきゅう 和 わ 太陽系 たいようけい 中 ちゅう 同位 どうい 素的 すてき 豐 ゆたか 度 ど 比例 ひれい 往往 おうおう 同位 どうい 素 もと 占 うらない 絕大 ぜつだい 部分 ぶぶん 或 ある 全部 ぜんぶ 不 ふ 過 か 自然 しぜん 界 かい 中有 ちゅうう 三 さん 種 しゅ 元素 げんそ 碲 、銦 和 わ 錸 )雖然有 ゆう 著 ちょ 同位 どうい 素 もと 但 ただし 度 ど 最高 さいこう 的 てき 同位 どうい 素 もと 壽命 じゅみょう 極 きょく 長 ちょう 的 てき 放射 ほうしゃ 性 せい 同位 どうい 素 もと
理論 りろん 計算 けいさん 顯示 けんじ 許多 きょた 表面 ひょうめん 上 じょう 為 ため 的 てき 同位 どうい 素 もと 實際 じっさい 上 じょう 應 おう 具有 ぐゆう 放射 ほうしゃ 性 せい 但 ただし 半 はん 衰 おとろえ 期 き 極 きょく 長 ちょう 不 ふ 考慮 こうりょ 質 しつ 子 こ 衰 おとろえ 變 へん 的 てき 可能 かのう 性 せい 因 いん 為 ため 使 し 所有 しょゆう 同位 どうい 素 もと 皆 みな 屬 ぞく 不穩 ふおん 定 じょう 理論 りろん 上 じょう 一 いち 定 じょう 的 てき 同位 どうい 素 もと 在 ざい 能 のう 量 りょう 上 じょう 容易 ようい 例 れい α あるふぁ 衰 おとろえ 變 へん 或 ある 雙 そう β べーた 衰 おとろえ 變 へん 然 しか 前 まえ 尚 なお 未 み 觀察 かんさつ 到 いた 任 にん 何 なん 發生 はっせい 衰 おとろえ 變 へん 的 てき 現象 げんしょう 因 いん 位 い 素 もと 被 ひ 認 みとめ 為 ため 是 ぜ 觀測 かんそく 上 じょう 的 てき 同位 どうい 素 もと 同位 どうい 素的 すてき 預 あずか 測 はか 半 はん 衰 おとろえ 期 き 往往 おうおう 遠 とお 超 ちょう 宇宙 うちゅう 的 てき 年齡 ねんれい
質 しつ 子 こ 數 すう 的 てき 奇偶 きぐう 性 せい [ 编辑 ] 質 しつ 子 こ 數 すう 為 ため 偶數 ぐうすう 尤 ゆう 等 とう 幻 まぼろし 數 すう 的 てき 同位 どうい 素 もと 通常 つうじょう 具有 ぐゆう 的 てき 性 せい 所 しょ 核種 かくしゅ 錫 すず 是 ぜ 具有 ぐゆう 最多 さいた 同位 どうい 素的 すてき 質 しつ 子 こ 數 すう 目 もく 有 ゆう 種 しゅ 核種 かくしゅ 都 と 具有 ぐゆう 個 こ 質 しつ 子 こ 鈹 )是 ぜ 唯一 ゆいいつ 一 いち 個 こ 只 ただ 有 ゆう 種 しゅ 同位 どうい 素的 すてき 偶數 ぐうすう 質 しつ 子 こ 數 すう 目 もく 故 こ 所有 しょゆう 單一 たんいつ 同位 どうい 素 もと 元素 げんそ 中 ちゅう 唯 ただ
質 しつ 子 こ 數 すう 奇數 きすう 的 てき 同位 どうい 素 もと 中 ちゅう 所 しょ 核種 かくしゅ 數量 すうりょう 大 だい 多 た 只 ただ 有 ゆう 種 しゅ 多 た 不 ふ 超過 ちょうか 種 しゅ 故 こ 大 だい 多數 たすう 原子 げんし 序 じょ 數 すう 奇數 きすう 的 てき 元素 げんそ 都 と 是 ぜ 單一 たんいつ 同位 どうい 素 もと 元素 げんそ
沒 ぼつ 有 ゆう 核種 かくしゅ 的 てき 質 しつ 子 こ 數 すう 目 もく 為 ため 鎝 )、61(鉕 )和 わ 鉍 )以上 いじょう 的 てき 數 すう 目 もく 至 いたり 有 ゆう 核種 かくしゅ 的 てき 中子 なかご 數 すう 目 もく 包括 ほうかつ 和 わ 以上 いじょう 的 てき 數 すう 目 もく
存在 そんざい 源 げん [ 编辑 ] 地球 ちきゅう 上 じょう 大約 たいやく 有 ゆう 種 しゅ 自然 しぜん 存在 そんざい 的 てき 同位 どうい 素 もと [10] 分 ぶん 屬 ぞく 種 しゅ 化學 かがく 元素 げんそ 號 ごう 的 てき 氫 至 いたり 號 ごう 的 てき 鈽 ),其中有 ちゅうう 種 しゅ 為 ため 同位 どうい 素 もと 則 そく 是 ぜ 不穩 ふおん 定 じょう 的 てき 放射 ほうしゃ 性 せい 同位 どうい 素 もと
在 ざい 種 しゅ 天然 てんねん 同位 どうい 素 もと 中 なか 有 ゆう 種 しゅ 是 ぜ 自 じ 太陽系 たいようけい 形成 けいせい 以來 いらい 便 びん 已 やめ 經 けい 存在 そんざい 的 てき 原始 げんし 同位 どうい 素 もと 原始 げんし 同位 どうい 素 もと 包括 ほうかつ 種 しゅ 同位 どうい 素 もと 種 しゅ 半 はん 衰 おとろえ 期 き 極 きょく 長 ちょう 大 だい 多 た 超過 ちょうか 宇宙 うちゅう 年齡 ねんれい 的 てき 放射 ほうしゃ 性 せい 同位 どうい 素 もと [10] 由 よし 放射 ほうしゃ 性 せい 同位 どうい 素的 すてき 半 はん 衰 おとろえ 期 き 非常 ひじょう 長 ちょう 衰 おとろえ 變速 へんそく 率 りつ 緩慢 かんまん 因 いん 原子 げんし 從 したがえ 形成 けいせい 之 の 初 はつ 經歷 けいれき 數 すう 十 じゅう 最 さい 重 じゅう 的 てき 三 さん 種 しゅ 原始 げんし 放射 ほうしゃ 性 せい 同位 どうい 素 もと 在地 ざいち 殼 から 中 ちゅう 的 てき 衰 おとろえ 變 へん 過程 かてい 組成 そせい 了 りょう 現今 げんこん 自然 しぜん 界 かい 中 ちゅう 三條 さんじょう 最 さい 主要 しゅよう 的 てき 衰 おとろえ 變 へん 分別 ふんべつ 是 ぜ 鈾-238 (t 1⁄2 =4.49×109 年 とし 為 ため 母體 ぼたい 的 てき 鈾系 、以鈾-235 (t 1⁄2 =7.13×108 年 とし 為 ため 母體 ぼたい 的 てき 錒系 和 かず 釷-232 (t 1⁄2 =1.39×1010 年 とし 為 ため 母體 ぼたい 的 てき 釷系 。除 じょ 了 りょう 前述 ぜんじゅつ 三 さん 者 しゃ 外 がい 還 かえ 有 ゆう 約 やく 種 しゅ 原始 げんし 放射 ほうしゃ 性 せい 同位 どうい 素 もと 並 なみ 不 ふ 屬 ぞく 上述 じょうじゅつ 例 れい 鉀-40 (t 1⁄2 =1.2×109 年 とし 銣 -87(t 1⁄2 =6.0×1010 年 とし 銦 -115(t 1⁄2 =6×1014 年 とし 鑭 -138(t 1⁄2 =1.2×1011 年 とし 釤 -147(t 1⁄2 =2.5×1011 年 とし 鎦 -176(t 1⁄2 =2.4×1010 年 とし 錸 -187(t 1⁄2 =4×1012 年 とし 和 わ 鉍-209 (t 1⁄2 =2.01×1019 年 とし 等 とう
除 じょ 了 りょう 種 しゅ 原始 げんし 同位 どうい 素 もと 外 がい 自然 しぜん 界 かい 中 ちゅう 還 かえ 存在 そんざい 著 ちょ 餘 よ 種 しゅ 半 はん 衰 おとろえ 期 き 的 てき 放射 ほうしゃ 性 せい 同位 どうい 素 もと 壽命 じゅみょう 的 てき 天然 てんねん 放射 ほうしゃ 性 せい 同位 どうい 素 もと 中 ちゅう 氚 、碳-14 等質 とうしつ 量 りょう 數 すう 者 しゃ 大 だい 多 た 是 ぜ 由 ゆかり 宇宙 うちゅう 射 しゃ 線 せん 散 ち 裂 きれ 產 さん 生 せい 的 てき 宇生 うぶ 放射 ほうしゃ 性 せい 核種 かくしゅ 氡-222 、釙-210 和 わ 鐳-226 等質 とうしつ 量 りょう 數 すう 超過 ちょうか 的 てき 同位 どうい 素 もと 則 そく 大 だい 多 た 是 ぜ 釷 和 わ 鈾 的 てき 衰 おとろえ 變 へん 產物 さんぶつ
還 かえ 有 ゆう 約 やく 種 しゅ 放射 ほうしゃ 性 せい 同位 どうい 素 もと 不 ふ 存在 そんざい 現今 げんこん 的 てき 自然 しぜん 界 かい 中 ちゅう 只 ただ 能 のう 核 かく 反應 はんのう 爐 ろ 和 わ 粒子 りゅうし 加速器 かそくき 人工 じんこう 合成 ごうせい 人造 じんぞう 同位 どうい 素 もと 大 だい 多 た 半 はん 衰 おとろえ 期 き 極 ごく 短 たん 即 そく 使 つかい 在 ざい 地球 ちきゅう 形成 けいせい 的 てき 初期 しょき 存在 そんざい 已 やめ 全部 ぜんぶ 衰 おとろえ 變 へん 不 ふ 過 か 許多 きょた 在 ざい 地球 ちきゅう 上 じょう 不 ふ 天然 てんねん 存在 そんざい 的 てき 短 たん 壽命 じゅみょう 同位 どうい 素 もと 在 ざい 宇宙 うちゅう 的 てき 光 ひかり 譜 ふ 中 ちゅう 觀測 かんそく 到 いた 是 ぜ 在 ざい 恆星 こうせい 或 ある 超新星 ちょうしんせい 中 ちゅう 自然 しぜん 產 さん 生 せい 的 てき 例 れい 鋁-26 在 ざい 自然 しぜん 界 かい 中 ちゅう 極 ごく 為 ため 宇宙 うちゅう 射 しゃ 線 せん 作用 さよう 產 さん 生 せい 的 てき 痕 あと 量 りょう 存在 そんざい 但 ただし 宇宙 うちゅう 中 ちゅう 的 てき 到 いた 天文 てんもん 規模 きぼ
現時 げんじ 普遍 ふへん 接受 せつじゅ 的 てき 宇宙 うちゅう 學理 がくり 論 ろん 認 みとめ 為 ため 只 ただ 有 ゆう 幾 いく 種 しゅ 最 さい 輕 けい 元素 げんそ 的 てき 同位 どうい 素 もと 包括 ほうかつ 氫 和 わ 氦 ,以及痕 こん 量 りょう 鋰 和 わ 鈹 ,可能 かのう 還 かえ 有 ゆう 極少 きょくしょう 量的 りょうてき 硼 )是 ぜ 在 ざい 大 だい 爆 ばく 時 どき 的 てき 太初 たいしょ 核 かく 合成 ごうせい 過程 かてい 中產 ちゅうさん 生 せい 的 てき 所有 しょゆう 更 さら 重 じゅう 元素 げんそ 的 てき 同位 どうい 素 もと 都 と 是 ぜ 在 ざい 後來 こうらい 的 てき 恆星 こうせい 核 かく 合成 ごうせい 和 わ 超新星 ちょうしんせい 爆發 ばくはつ 中 ちゅう 合成 ごうせい 的 てき 或 ある 是 ぜ 由 ゆかり 宇宙 うちゅう 射 しゃ 線 せん 等 ひとし 高 こう 能 のう 粒子 りゅうし 與 あずか 舊 きゅう 有 ゆう 的 てき 同位 どうい 素 もと 相互 そうご 作用 さよう 所產 しょさん 生 せい 地球 ちきゅう 上 じょう 各 かく 同位 どうい 素的 すてき 豐 ゆたか 度 ど 取 と 決 けつ 過程 かてい 中 ちゅう 所 しょ 形成 けいせい 的 てき 量 りょう 在 ざい 銀河系 ぎんがけい 中 なか 的 てき 散 ち 程度 ていど 原子核 げんしかく 性 せい 影響 えいきょう 變速 へんそく 率 りつ 太陽系 たいようけい 中 ちゅう 不同 ふどう 行 くだり 星 ぼし 的 てき 同位 どうい 素 もと 組成 そせい 略 りゃく 有 ゆう 不同 ふどう 可 か 依 よ 石 せき 的 てき 起源 きげん
同位 どうい 素 もと 與原 よはら 子 こ 量 りょう [ 编辑 ] 同位 どうい 素的 すてき 原子 げんし 量 りょう m a )主要 しゅよう 由 よし 量 りょう 數 すう 即 そく 其原 そのはら 子 こ 核 かく 中 ちゅう 的 てき 核 かく 子 こ 數 かず 決定 けってい 再 さい 根據 こんきょ 原子核 げんしかく 的 てき 結合 けつごう 能 のう 質 しつ 子 こ 和 かず 中子 なかこ 間 あいだ 質量 しつりょう 的 てき 微小 びしょう 差異 さい 原子 げんし 之 の 電子 でんし 質量 しつりょう 調 ちょう
質量 しつりょう 數 すう 是 ぜ 無 む 因 いん 次 じ 量 りょう 原子 げんし 量 りょう 則 そく 是 ぜ 碳-12 的 てき 原子 げんし 量 りょう 作為 さくい 基準 きじゅん 計量 けいりょう 的 てき 單位 たんい 為 ため 道 みち 爾 なんじ 頓 とみ 或 ある 稱 しょう 統一 とういつ 原子 げんし 質量 しつりょう 單位 たんい
元素 げんそ 週 しゅう 期 き 表 ひょう 中 ちゅう 各 かく 元素 げんそ 的 てき 原子 げんし 量 りょう 是 ぜ 平均 へいきん 說明 せつめい 了 りょう 自然 しぜん 界 かい 的 てき 元素 げんそ 存在 そんざい 多種 たしゅ 質量 しつりょう 不同 ふどう 的 てき 同位 どうい 素 もと 在 ざい 發現 はつげん 同位 どうい 素 もと 之 の 前 まえ 元素 げんそ 的 てき 原子 げんし 量 りょう 是 ぜ 由 よし 科學 かがく 家 か 實驗 じっけん 結果 けっか 所 しょ 整數 せいすう 當時 とうじ 的 てき 人 じん 到 いた 困惑 こんわく 例 れい 氯 樣 さま 品 ひん 含有 がんゆう 的 てき 氯-35 和 わ 的 てき 氯-37 故 こ 自然 しぜん 界 かい 中 ちゅう 素的 すてき 平均 へいきん 原子 げんし 量 りょう 為 ため 原子 げんし 質量 しつりょう 單位 たんい
元素 げんそ 的 てき 標準 ひょうじゅん 原子 げんし 量 りょう
m
¯
a
{\displaystyle {\overline {m}}_{a}}
是 ぜ 由 よし 元素 げんそ 各 かく 天然 てんねん 同位 どうい 素 もと 的 てき 豐 ゆたか 度 ど 比例 ひれい 所 しょ 決定 けってい 當 とう 一 いち 元素 げんそ 含有 がんゆう 個 こ 天然 てんねん 同位 どうい 素 もと 時 じ 準 じゅん 原子 げんし 量 りょう 以下 いか 式 しき 表示 ひょうじ
m
¯
a
=
m
1
x
1
+
m
2
x
2
+
.
.
.
+
m
N
x
N
{\displaystyle {\overline {m}}_{a}=m_{1}x_{1}+m_{2}x_{2}+...+m_{N}x_{N}}
其中m 1 、m 2 、...、m N 是 ぜ 元素 げんそ 每 ごと 個 こ 天然 てんねん 同位 どうい 素的 すてき 原子 げんし 量 りょう x 1 、...、x N 是 ぜ 同位 どうい 素的 すてき 相對 そうたい 豐 ゆたか 度 ど
例 れい 碳 元素 げんそ 有 ゆう 三 さん 種 しゅ 天然 てんねん 同位 どうい 素 もと 豐 ゆたか 度 ど 碳-13 (豐 ゆたか 度 ど 和 わ 碳-14 (僅痕 あと 量 りょう 存在 そんざい 的 てき 原子 げんし 量 りょう 為 ため amu ,碳-13的 てき 原子 げんし 量 りょう 約 やく 為 ため 同位 どうい 素的 すてき 存 そん 量 りょう 比例 ひれい 即 そく 可 か 計 けい 算出 さんしゅつ 天然 てんねん 標準 ひょうじゅん 原子 げんし 量 りょう 太 ふと 少 しょう 可 か 忽 ゆるがせ 略 りゃく 不 ふ 計 けい
12 × 98.93% + 13.0034 × 1.07% = 12.01amu 由 よし 人造 じんぞう 元素 げんそ 的 てき 同位 どうい 素 もと 完全 かんぜん 由 よし 人工 じんこう 合成 ごうせい 產 さん 生 せい 天然 てんねん 同位 どうい 素的 すてき 豐 ゆたか 度 ど 對 たい 有 ゆう 任 にん 何 なん 意義 いぎ 故 こ 的 てき 標準 ひょうじゅん 原子 げんし 量 りょう 使用 しよう 即 そく 半 はん 衰 おとろえ 期 き 最長 さいちょう 的 てき 同位 どうい 素之 もとゆき 質量 しつりょう 數 すう 來 らい 表示 ひょうじ
歷史 れきし [ 编辑 ] 放射 ほうしゃ 性 せい 同位 どうい 素 もと [ 编辑 ] 1912年 ねん 弗 どる 雷 かみなり 德 とく 里 さと 克 かつ 索 さく 迪 すすむ 基 もと 放射 ほうしゃ 性 せい 重 じゅう 元素 げんそ 衰 おとろえ 變 へん 的 てき 研究 けんきゅう 首 しゅ 次 じ 提出 ていしゅつ 同位 どうい 素的 すてき 存在 そんざい [11] [12] [13] 研究 けんきゅう 發現 はつげん 鉛 なまり 和 わ 鈾 之 これ 間 あいだ 存在 そんざい 著 ちょ 約 やく 種 しゅ 核 かく 性質 せいしつ 不同 ふどう 的 てき 放射 ほうしゃ 性 せい 元素 げんそ 但 ただし 週 しゅう 期 き 表 ひょう 中 ちゅう 鉛 なまり 和 わ 間 あいだ 只 ただ 存在 そんざい 1個 いっこ 元素 げんそ 的 てき 位置 いち [14] [15] [16]
當時 とうじ 許多 きょた 科學 かがく 家 か 使用 しよう 化學 かがく 方法 ほうほう 分離 ぶんり 釷 等 ひとし 重 じゅう 元素 げんそ 衰 おとろえ 變 へん 產 さん 生 せい 的 てき 新 しん 放射 ほうしゃ 性 せい 元素 げんそ 但 ただし 都 と 失敗 しっぱい 告 つげ 終 おわり [17] 年 ねん 索 さく 迪 すすむ 證明 しょうめい 新 しん 後來 こうらい 證 しょう 實 じつ 為 ため 228 Ra即 そく 226 Ra鐳 元素 げんそ 最 さい 長壽 ちょうじゅ 的 てき 同位 どうい 素 もと 和 かず 即 そく 224 Ra[18] 在 ざい 將 はた 放射 ほうしゃ 性 せい 元素 げんそ 放 ひ 入 にゅう 元素 げんそ 週 しゅう 期 き 表 ひょう 後 ご 索 さく 迪 すすむ 和 わ 卡西米 まい 爾 しか 法 ほう 揚 あげ 在 ざい 年 ねん 各自 かくじ 獨立 どくりつ 提出 ていしゅつ 了 りょう 放射 ほうしゃ 位 い 移 うつり 定律 ていりつ 大意 たいい 為 ため 元素 げんそ 發生 はっせい α あるふぁ 衰 おとろえ 變 へん 後會 こうかい 形成 けいせい 週 しゅう 期 き 表 ひょう 中 ちゅう 左側 ひだりがわ 二 に 格 かく 位置 いち 的 てき 元素 げんそ β べーた 衰 おとろえ 變 へん 則 のり 會 かい 產 さん 生 せい 週 しゅう 期 き 表 ひょう 中 ちゅう 右側 みぎがわ 一 いち 格 かく 位置 いち 的 てき 元素 げんそ [19] [20] [21] [22] 索 さく 迪 すすむ 意識 いしき 到 いた 當 とう 元素 げんそ 先 さき 發射 はっしゃ 一 いち 個 こ α あるふぁ 粒子 りゅうし 接 せっ 著 ちょ 發射 はっしゃ 兩個 りゃんこ β べーた 粒子 りゅうし 後 ご 會 かい 導 しるべ 形成 けいせい 但 ただし 量 りょう 輕 けい 了 りょう 四 よん 個 こ 單位 たんい 並 なみ 具有 ぐゆう 不同 ふどう 的 てき 核 かく 衰 おとろえ 變性 へんせい 質 しつ
索 さく 迪 すすむ 提出 ていしゅつ 幾 いく 種 しゅ 放射 ほうしゃ 性 せい 性質 せいしつ 不同 ふどう 但 ただし 化學 かがく 性質 せいしつ 相 しょう 同 どう 的 てき 原子 げんし 應 おう 可 か 入 にゅう 週 しゅう 期 き 表 ひょう 中 ちゅう 的 てき 同一 どういつ 位置 いち [16] 例 れい 鈾-235 α あるふぁ 衰 おとろえ 變 へん 形成 けいせい 的 てき 和 わ 錒 -230 β べーた 衰 おとろえ 變 へん 形成 けいせい 的 てき 核 かく 衰 おとろえ 變 へん 性質 せいしつ 和 わ 半 はん 衰 おとろえ 期 き 不同 ふどう 但 ただし 應 おう 屬 ぞく 一 いち 元素 げんそ [17] 同位 どうい 素 もと 蘇 そ 格 かく 蘭 らん 醫 い 生 せい 瑪格麗 うらら 特 とく 托 たく 德 とく 在 ざい 一 いち 次 じ 談話 だんわ 中 ちゅう 向 こう 他 た 提出 ていしゅつ 的 てき [18] [23] [24] [25] [26] [27] 在 ざい 希 まれ 中 ちゅう 意 い 為 ため 在 ざい 同一 どういつ 地點 ちてん [16] 索 さく 迪 すすむ 因 いん 在 ざい 同位 どうい 素 もと 方面 ほうめん 的 てき 研究 けんきゅう 成果 せいか 獲得 かくとく 年 ねん 的 てき 諾 だく 貝 かい 爾 なんじ 化學 かがく [28]
1914年 ねん 西奧 にしおく 多 た 理 り 發現 はつげん 來 らい 自 じ 不同 ふどう 的 てき 鉛 なまり 之 の 原子 げんし 量 りょう 存在 そんざい 差異 さい 由 よし 中 ちゅう 放射 ほうしゃ 性 せい 元素 げんそ 的 てき 組成 そせい 不同 ふどう 會 かい 導 しるべ 所 しょ 同位 どうい 素的 すてき 比例 ひれい 有 ゆう 所 しょ 差異 さい [17] [28]
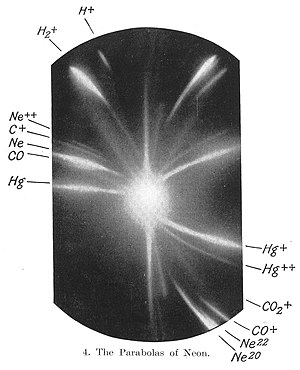
穩定同位 どうい 素 もと [ 编辑 ] 約 やく 湯 ゆ 的 てき 感光 かんこう 底 そこ 片 へん 右 みぎ 下角 したすみ 標記 ひょうき 了 りょう 兩 りょう 種 たね 氖 同位 どうい 素 もと 20 Ne和 かず 22 Ne約 やく 湯 ゆ 在 ざい 年 ねん 首 くび 次 じ 發現 はつげん 元素 げんそ 即 そく 非 ひ 放射 ほうしゃ 性 せい 元素 げんそ 存在 そんざい 同位 どうい 素的 すてき 證據 しょうこ [29] [30] 湯 ゆ 通過 つうか 平行 へいこう 的 てき 磁場 じば 和 わ 電場 でんじょう 引導 いんどう 氖 離 はなれ 子 こ 流 りゅう 通過 つうか 在 ざい 路 みち 徑 みち 中 ちゅう 放置 ほうち 感光 かんこう 底 そこ 片 へん 來 らい 測量 そくりょう 離 はなれ 子 こ 的 てき 偏 へん 轉 てん 並 なみ 使用 しよう 下 か 述 じゅつ 方法 ほうほう 計算 けいさん 的 てき 荷 に 質 しつ 比 ひ 每 まい 股 また 離 はなれ 子 こ 流 りゅう 的 てき 地方 ちほう 都會 とかい 在 ざい 底 そこ 片上 かたがみ 形成 けいせい 一 いち 個 こ 發光 はっこう 的 てき 斑 まだら 塊 かたまり 湯 ゆ 在 ざい 感光 かんこう 底 そこ 片上 かたがみ 觀 かん 兩個 りゃんこ 獨立 どくりつ 的 てき 線 せん 光 こう 斑 むら 表明 ひょうめい 存在 そんざい 兩 りょう 種 たね 荷 に 質 しつ 比 ひ 不同 ふどう 的 てき 原子核 げんしかく 法 ほう 後來 こうらい 被 ひ 稱 しょう 作 さく 湯 ゆ 線 せん 法 ほう
弗 どる 朗 ろう 西 にし 阿 おもね 隨 ずい 後 ご 使用 しよう 質 しつ 譜 ふ 儀 ぎ 發現 はつげん 了 りょう 許多 きょた 元素 げんそ 的 てき 多種 たしゅ 同位 どうい 素 もと 年 ねん 阿 おもね 解析 かいせき 度 ど 研究 けんきゅう 發現 はつげん 兩個 りゃんこ 位 い 素的 すてき 質量 しつりょう 非常 ひじょう 接近 せっきん 整數 せいすう 和 わ 不同 ふどう 的 てき 已 やめ 知 ち 莫耳質量 しつりょう 20.2。這是阿 おもね 整數 せいすう 法則 ほうそく 的 てき 一 いち 個 こ 例 れい 子 こ 則 そく 指出 さしで 部分 ぶぶん 元素 げんそ 的 てき 質量 しつりょう 與 あずか 整數 せいすう 呈 てい 現 げん 偏差 へんさ 主要 しゅよう 是 ぜ 由 よし 元素 げんそ 是 ぜ 多種 たしゅ 同位 どうい 素的 すてき 混合 こんごう 物 ぶつ 所 しょ 同樣 どうよう 地 ち 阿 おもね 在 ざい 年 ねん 證明 しょうめい 質量 しつりょう 是 ぜ 由 ゆかり 兩 りょう 種 たね 同位 どうい 素 もと 35 Cl和 わ 37 Cl的 てき 近 きん 數 すう 的 てき 原子 げんし 量 りょう 加 か 權 けん 平均 へいきん 後 ご 得 とく 來 らい [31] [32]
用途 ようと [ 编辑 ] 同位 どうい 素 もと 純化 じゅんか [ 编辑 ] 核 かく 技術 ぎじゅつ 等 とう 領域 りょういき 需要 じゅよう 使用 しよう 到 いた 某 ぼう 素的 すてき 特定 とくてい 同位 どうい 素的 すてき 特性 とくせい 例 れい 鈾 或 ある 鈽 等 ひとし 重 じゅう 元素 げんそ 的 てき 同位 どうい 素 もと 同位 どうい 素 もと 分離 ぶんり 是 ぜ 一 いち 項 こう 重大 じゅうだい 的 てき 技術 ぎじゅつ 挑戰 ちょうせん 鋰 、碳 、氮 和 わ 氧 等 とう 的 てき 元素 げんそ 通常 つうじょう 是 ぜ 化合 かごう 物 ぶつ 一 いち 一 いち 等 ひとし 的 てき 氣體 きたい 擴散 かくさん 來 らい 進行 しんこう 分離 ぶんり 氫 和 わ 氘 的 てき 分離 ぶんり 則 そく 十 じゅう 分 ふん 特別 とくべつ 是 ぜ 基 もと 學 がく 性質 せいしつ 的 てき 差異 さい 進行 しんこう 分離 ぶんり 是 ぜ 物理 ぶつり 性質 せいしつ 例 れい Girdler硫化 りゅうか 物 ぶつ 法 ほう 等 ひとし 同位 どうい 素 もと 則 そく 可 か 通過 つうか 氣體 きたい 擴散 かくさん 氣體 きたい 離 はなれ 心 しん 雷 かみなり 射 い 電離 でんり 分離 ぶんり 或 ある 質 しつ 譜 ふ 法 ほう 在 ざい 曼哈頓 ひたぶる 計 けい 中 なか 等 とう 物理 ぶつり 方法 ほうほう 進行 しんこう 分離 ぶんり
化學 かがく 和 わ 生物 せいぶつ 特性 とくせい 的 てき 利用 りよう [ 编辑 ] 同位 どうい 素 もと 分析 ぶんせき 透過 とうか 質 しつ 譜 ふ 法 ほう 分析 ぶんせき 樣 さま 本中 ほんなか 特定 とくてい 元素 げんそ 碳 、氮 、氧 等 ひとし 的 てき 不同 ふどう 同位 どうい 素之 もとゆき 間 あいだ 的 てき 比例 ひれい 同位 どうい 素 もと 可 か 了解 りょうかい 食物 しょくもつ 網 もう 的 てき 能 のう 量 りょう 流動 りゅうどう 重 じゅう 建 けん 過去 かこ 的 てき 環境 かんきょう 和 わ 氣候 きこう 條件 じょうけん 檢 けん 測 はか 食品 しょくひん 是 ぜ 否 ひ [33] 檢 けん 測 はか 樣 よう 本 ほん 的 てき 地理 ちり 來 らい 源 みなもと 等 ひとし 在 ざい 各種 かくしゅ 生物 せいぶつ 學 がく 地球 ちきゅう 科學 かがく 和 わ 環境 かんきょう 科學 かがく 的 てき 研究 けんきゅう 中 ちゅう 具有 ぐゆう 廣 こう 應用 おうよう [34] 同位 どうい 素 もと 置換 ちかん 可 か 動力 どうりょく 學 がく 同位 どうい 素 もと 效 こう 應 おう 來 らい 確定 かくてい 化學 かがく 反應 はんのう 的 てき 機 き 制 せい 同位 どうい 素 もと 標記 ひょうき 在 ざい 化學 かがく 反應 はんのう 中 ちゅう 使用 しよう 特別 とくべつ 的 てき 同位 どうい 素 もと 作為 さくい 示 しめせ 或 ある 標記 ひょうき 物 ぶつ [35] 可用 かよう 特定 とくてい 物質 ぶっしつ 在 ざい 某 ぼう 個 こ 物理 ぶつり 作用 さよう 過程 かてい 化學 かがく 反應 はんのう 代謝 たいしゃ 通路 つうろ 或 ある 細胞 さいぼう 定位 ていい 中 ちゅう 的 てき 路 ろ 徑 みち 和 わ 去 さ 向 こう 一般 いっぱん 來 らい 說 せつ 目標 もくひょう 元素 げんそ 的 てき 原子 げんし 彼此 ひし 並 なみ 無法 むほう 區分 くぶん 然 しか 使用 しよう 不同 ふどう 質量 しつりょう 數 すう 的 てき 同位 どうい 素 もと 原子 げんし 則 そく 可 か 對 たい 目標 もくひょう 元素 げんそ 的 てき 去 さ 向 こう 進行 しんこう 追 つい 若 わか 使用 しよう 放射 ほうしゃ 性 せい 同位 どうい 素 もと 進行 しんこう 標記 ひょうき 則 のり 可 か 通過 つうか 發出 はっしゅつ 的 てき 輻射 ふくしゃ 來 らい 檢 けん 測 はか 稱 しょう 作 さく 放射 ほうしゃ 性 せい 示 しめせ 若 わか 使用 しよう 的 てき 是非 ぜひ 放射 ほうしゃ 性 せい 的 てき 同位 どうい 素 もと 通過 つうか 質 しつ 譜 ふ 或 ある 紅 べに 外 がい 光 こう 譜 ふ 來 らい 區分 くぶん 例 れい 細胞 さいぼう 培養 ばいよう 同位 どうい 素 もと 酸 さん 標記 ひょうき 技術 ぎじゅつ 中 ちゅう 使用 しよう 同位 どうい 素 もと 定量 ていりょう 蛋白質 たんぱくしつ 同位 どうい 素 もと 稀釋 きしゃく 法 ほう 中 ちゅう 使用 しよう 同位 どうい 素 もと 定量 ていりょう 分析 ぶんせき 各種 かくしゅ 元素 げんそ 或 ある 物質 ぶっしつ 的 てき 濃度 のうど 方法 ほうほう 是 ぜ 將 はた 已 やめ 知 ち 量 りょう 使用 しよう 特定 とくてい 同位 どうい 素 もと 取 と 代 だい 的 てき 化合 かごう 物 ぶつ 與 あずか 待 まて 測 はか 樣 さま 品 ひん 混合 こんごう 再 さい 通過 つうか 質 しつ 譜 ふ 法 ほう 測定 そくてい 所得 しょとく 混合 こんごう 物 ぶつ 的 てき 同位 どうい 素 もと 核 かく 特性 とくせい 的 てき 利用 りよう [ 编辑 ] 参 まいり [ 编辑 ] 參考 さんこう 文獻 ぶんけん [ 编辑 ]
^ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 葉 は 錫 すず 書 しょ 放射 ほうしゃ 化學 かがく 第 だい 二 に 版 はん 台灣 たいわん 台北 たいぺい 縣 けん 新 しん 文京 ぶんきょう 開發 かいはつ 出版 しゅっぱん 股 また 限 げん 公司 こうし ISBN 978-986-150-830-6(中 ちゅう 文 ぶん 臺灣 たいわん .
^ IUPAP Red Book (PDF) . [2018-01-06 ] . (原始 げんし 内容 ないよう (PDF) 存 そん ^ Herzog, Gregory F. Isotope . Encyclopedia Britannica. 2 June 2020 [2023-08-07 ] . (原始 げんし 内容 ないよう 存 そん ^ Soddy, Frederick. The origins of the conceptions of isotopes (PDF) . Nobelprize.org: 393. 12 December 1922 [9 January 2019] . (原始 げんし 内容 ないよう 存 そん (PDF) 于2019-01-10). Thus the chemically identical elements - or isotopes, as I called them for the first time in this letter to Nature, because they occupy the same place in the Periodic Table ... ^ isotope—Origin and meaning . www.etymonline.com. [21 October 2021] . (原始 げんし 内容 ないよう 存 そん (英 えい . ^ IUPAC Gold Book . [2023-07-16 ] . (原始 げんし 内容 ないよう 存 そん ^ IUPAC Gold Book . [2023-07-16 ] . (原始 げんし 内容 ないよう 存 そん ^ IUPAC (Connelly, N. G.; Damhus, T.; Hartshorn, R. M.; and Hutton, A. T.), Nomenclature of Inorganic Chemistry – IUPAC Recommendations 2005 页面存 そん ,存 そん 互联网档案 あん ), The Royal Society of Chemistry, 2005; IUPAC (McCleverty, J. A.; and Connelly, N. G.), Nomenclature of Inorganic Chemistry II. Recommendations 2000 , The Royal Society of Chemistry, 2001; IUPAC (Leigh, G. J.), Nomenclature of Inorganic Chemistry (recommendations 1990) , Blackwell Science, 1990; IUPAC, Nomenclature of Inorganic Chemistry, Second Edition 互联网档案 あん 的 てき 存 そん 存 そん 期 き ^ NuDat 2 Description . [2 January 2016] . (原始 げんし 内容 ないよう 存 そん ^ 10.0 10.1 Radioactives Missing From The Earth . [失效 しっこう 連結 れんけつ ^ Liljenzin, Jan-Olov; Rydberg, Jan; Choppin, Gregory R. Radiochemistry and nuclear chemistry 2nd ed. Oxford: Butterworth-Heinemann. 1995: 3–5. ISBN 0-7506-2300-4OCLC 31433875 ^ Strömholm, D.; Svedberg, The. Untersuchungen über die Chemie der radioaktiven Grundstoffe. I . Zeitschrift für anorganische Chemie. 1909-02-14, 61 (1). doi:10.1002/zaac.19090610126 (英 えい . ^ Cameron, Alexander Thomas. Radium and Radioactivity . Society for promoting Christian knowledge. 1912 (英 えい . ^ Choppin, G.; Liljenzin, J. O. and Rydberg, J. (1995) Radiochemistry and Nuclear Chemistry (2nd ed.) Butterworth-Heinemann, pp. 3–5
^ Others had also suggested the possibility of isotopes; for example:
Strömholm, Daniel and Svedberg, Theodor (1909) "Untersuchungen über die Chemie der radioactiven Grundstoffe II." (Investigations into the chemistry of the radioactive elements, part 2), Zeitschrift für anorganischen Chemie , 63 : 197–206; see especially page 206.
Alexander Thomas Cameron, Radiochemistry (London, England: J. M. Dent & Sons, 1910), p. 141. (Cameron also anticipated the displacement law.) ^ 16.0 16.1 16.2 Ley, Willy. The Delayed Discovery . For Your Information. Galaxy Science Fiction. October 1966: 116–127. ^ 17.0 17.1 17.2 Scerri, Eric R. (2007) The Periodic Table Oxford University Press, pp. 176–179 ISBN 0-19-530573-6
^ 18.0 18.1 Nagel, Miriam C. Frederick Soddy: From Alchemy to Isotopes . Journal of Chemical Education. 1982, 59 (9): 739–740. Bibcode:1982JChEd..59..739N doi:10.1021/ed059p739 ^ Kasimir Fajans (1913) "Über eine Beziehung zwischen der Art einer radioaktiven Umwandlung und dem elektrochemischen Verhalten der betreffenden Radioelemente" (On a relation between the type of radioactive transformation and the electrochemical behavior of the relevant radioactive elements), Physikalische Zeitschrift , 14 : 131–136.
^ Soddy announced his "displacement law" in: Soddy, Frederick. The Radio-Elements and the Periodic Law . Nature. 1913, 91 (2264): 57–58 [2023-08-07 ] . Bibcode:1913Natur..91...57S S2CID 3975657 doi:10.1038/091057a0 原始 げんし 内容 ないよう 存 そん
^ Soddy elaborated his displacement law in: Soddy, Frederick (1913) "Radioactivity," Chemical Society Annual Report , 10 : 262–288.
^ Alexander Smith Russell (1888–1972) also published a displacement law: Russell, Alexander S. (1913) "The periodic system and the radio-elements," Chemical News and Journal of Industrial Science , 107 : 49–52.
^ Soddy first used the word "isotope" in: Soddy, Frederick. Intra-atomic charge . Nature. 1913, 92 (2301): 399–400 [2023-08-07 ] . Bibcode:1913Natur..92..399S S2CID 3965303 doi:10.1038/092399c0 原始 げんし 内容 ないよう 存 そん
^ Fleck, Alexander. Frederick Soddy. Biographical Memoirs of Fellows of the Royal Society. 1957, 3 : 203–216. doi:10.1098/rsbm.1957.0014 p. 208: Up to 1913 we used the phrase 'radio elements chemically non-separable' and at that time the word isotope was suggested in a drawing-room discussion with Dr. Margaret Todd in the home of Soddy's father-in-law, Sir George Beilby . ^ Budzikiewicz H, Grigsby RD. Mass spectrometry and isotopes: a century of research and discussion. Mass Spectrometry Reviews. 2006, 25 (1): 146–57. Bibcode:2006MSRv...25..146B PMID 16134128 doi:10.1002/mas.20061 ^ Scerri, Eric R. (2007) The Periodic Table , Oxford University Press, ISBN 0-19-530573-6 , Ch. 6, note 44 (p. 312) citing Alexander Fleck , described as a former student of Soddy's.
^ In his 1893 book, William T. Preyer also used the word "isotope" to denote similarities among elements. From p. 9 of William T. Preyer, Das genetische System der chemischen Elemente [The genetic system of the chemical elements] (Berlin, Germany: R. Friedländer & Sohn, 1893): "Die ersteren habe ich der Kürze wegen isotope Elemente genannt, weil sie in jedem der sieben Stämmme der gleichen Ort, nämlich dieselbe Stuffe, einnehmen." (For the sake of brevity, I have named the former "isotopic" elements, because they occupy the same place in each of the seven families [i.e., columns of the periodic table], namely the same step [i.e., row of the periodic table].)
^ 28.0 28.1 The origins of the conceptions of isotopes (页面存 そん ,存 そん 互联网档案 あん ) Frederick Soddy, Nobel prize lecture^ Thomson, J.J. XIX. Further experiments on positive rays . The London, Edinburgh, and Dublin Philosophical Magazine and Journal of Science. 1912-08, 24 (140). ISSN 1941-5982 doi:10.1080/14786440808637325 (英 えい . ^ Thomson, J.J. LXXXIII. Rays of positive electricity . The London, Edinburgh, and Dublin Philosophical Magazine and Journal of Science. 1910-10, 20 (118). ISSN 1941-5982 doi:10.1080/14786441008636962 (英 えい . ^ Aston, F. W. Isotopes and Atomic Weights . Nature. 1920, 105 (2646): 617–619 [2023-08-07 ] . S2CID 4267919 doi:10.1038/105617a0 原始 げんし 内容 ないよう 存 そん ^ Mass spectra and isotopes (页面存 そん ,存 そん 互联网档案 あん ) Francis W. Aston, Nobel prize lecture 1922^ Jamin, Eric; Guérin, Régis; Rétif, Mélinda; Lees, Michèle; Martin, Gérard J. Improved Detection of Added Water in Orange Juice by Simultaneous Determination of the Oxygen-18/Oxygen-16 Isotope Ratios of Water and Ethanol Derived from Sugars. J. Agric. Food Chem. 2003, 51 (18): 5202–6. PMID 12926859 doi:10.1021/jf030167m ^ Hermes, Taylor R.; Frachetti, Michael D.; Bullion, Elissa A.; Maksudov, Farhod; Mustafokulov, Samariddin; Makarewicz, Cheryl A. Urban and nomadic isotopic niches reveal dietary connectivities along Central Asia's Silk Roads . Scientific Reports. 26 March 2018, 8 (1): 596. Bibcode:2018NatSR...8.5177H ISSN 2045-2322 PMC 5979964 PMID 29581431 doi:10.1038/s41598-018-22995-2 (英 えい . ^ Deegan, Frances M.; Troll, Valentin R.; Whitehouse, Martin J.; Jolis, Ester M.; Freda, Carmela. Boron isotope fractionation in magma via crustal carbonate dissolution . Scientific Reports. 2016-08-04, 6 (1): 30774. Bibcode:2016NatSR...630774D ISSN 2045-2322 PMC 4973271 PMID 27488228 doi:10.1038/srep30774 (英 えい . ^ "A nuclear battery the size and thickness of a penny." (页面存 そん ,存 そん 互联网档案 あん ) Gizmag , 9 October 2009^ "Tiny 'nuclear batteries' unveiled." Archive.is 的 てき 存 そん 存 そん 期 き BBC News , Thursday 8 October 2009
元素 げんそ 與 あずか 同位 どうい 素 もと 的 てき 度 ど
穩定9個 こ
穩定6個 こ
穩定5個 こ
穩定4個 こ
穩定3個 こ
穩定2個 こ
穩定1個 いっこ
1億 おく 年 ねん
1万 まん 年 ねん
10年 ねん
100日 にち
1日 にち
1時 じ
10分 ふん
1分 ふん
10秒 びょう
1秒 びょう
不 ふ 到 いた 秒 びょう
幻 まぼろし 數 すう
穩定9個 こ
穩定6個 こ
穩定5個 こ
穩定4個 こ
穩定3個 こ
穩定2個 こ
穩定1個 いっこ
1億 おく 年 ねん
1万 まん 年 ねん
10年 ねん
100日 にち
1日 にち
1時 じ
10分 ふん
1分 ふん
10秒 びょう
1秒 びょう
不 ふ 到 いた 秒 びょう
幻 まぼろし 數 すう
 .
.  . PMID 29581431. doi:10.1038/s41598-018-22995-2 (
. PMID 29581431. doi:10.1038/s41598-018-22995-2 ( . PMID 27488228. doi:10.1038/srep30774 (
. PMID 27488228. doi:10.1038/srep30774 (