| 1-βουτανόλη
|
|

|
|
| Γενικά
|
| Όνομα IUPAC |
1-βουτανόλη
|
| Άλλες ονομασίες |
Βουτυρική αλκοόλη
1-υδροξυβουτάνιο
1-οξαπεντάνιο
|
| Χημικά αναγνωριστικά
|
| Χημικός τύπος |
C4H10O
|
| Μοριακή μάζα |
74,12 amu
|
Σύντομος
συντακτικός τύπος |
C4H9OH
|
| Συντομογραφίες |
BuOH
|
| Αριθμός CAS |
71-36-3
|
| SMILES |
CCCCO
|
| InChI |
1S/C4H10O/c1-2-3-4-5/h5H,2-4H2,1H3
|
| Αριθμός EINECS |
200-751-6
|
| Αριθμός RTECS |
EO1400000
|
| Αριθμός UN |
1120
|
| PubChem CID |
263
|
| ChemSpider ID |
258
|
| Δομή
|
| Διπολική ροπή |
1,66 D
|
| Ισομέρεια
|
| Ισομερή θέσης |
6
|
| Φυσικές ιδιότητες
|
| Σημείο τήξης |
−90 °C
|
| Σημείο βρασμού |
118 °C
|
| Πυκνότητα |
810 kg/m3
|
Διαλυτότητα
στο νερό |
73 kg/m3
|
| Ιξώδες |
3 cP
|
Δείκτης διάθλασης ,
nD |
1,399 (20 °C)
|
| Εμφάνιση |
Άχρωμο υγρό
|
| Χημικές ιδιότητες
|
Ελάχιστη θερμοκρασία
ανάφλεξης |
35 °C
|
| Σημείο αυτανάφλεξης |
343 °C
|
| Επικινδυνότητα
|
|
|

|
| Βλαβερή (Xn)
|
| Φράσεις κινδύνου |
R10, R22, R37/38, R41, R67
|
| Φράσεις ασφαλείας |
(S2), S7/9, S13, S26, S37/39, S46
|
| LD50 |
790 mg/kg[1]
|
Κίνδυνοι κατά
NFPA 704 |
|
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa).
|
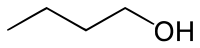
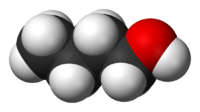
Η 1-βουτανόλη[2] είναι οργανική χημική ένωση, που περιέχει άνθρακα, υδρογόνο και οξυγόνο, με χημικό τύπο C4H10O, αν και παριστάνεται συχνά και με τους τύπους C4H9OH, CH3CH2CH2CH2OH και BuOH. Είναι μια πρωτοταγής αλκοόλη με τέσσερα (4) άτομα άνθρακα ανά μόριο. Με βάση το χημικό τύπο της, C4H10O, έχει τα ακόλουθα 6 ισομερή θέσης
(+ 1 οπτικό = 7 συνολικά ισομερή):
- 2-βουτανόλη ή δευτεροταγής βουτανόλη, με σύντομο συντακτικό τύπο: CH3CH2CH(OH)CH3, σε δύο (2) οπτικά ισομερή.
- Μεθυλο-1-προπανόλη ή ισοβουτανόλη, με σύντομο συντακτικό τύπο: (CH3)2CHCH2OH.
- Μεθυλο-2-προπανόλη ή τριτοταγής βουτανόλη, με σύντομο συντακτικό τύπο: (CH3)3COH.
- 1-μεθοξυπροπάνιο ή μεθυλοπροπυλαιθέρας, με σύντομο συντακτικό τύπο: CH3CH2CH2ΟCH3.
- 2-μεθοξυπροπάνιο ή ισοπροπυλομεθυλαιθέρας, με σύντομο συντακτικό τύπο: (CH3)2CHΟCH3.
- Αιθυοξυαιθάνιο ή διαιθυλαιθέρας, με σύντομο συντακτικό τύπο: CH3CH2ΟCH2CH3.
Η βουτανόλη ανήκει στην ομάδα των ζυμελαίων (αγγλόφωνος όρος: fusel alcohols, γερμανόφωνος όρος:
bad likör), δηλαδή των αλκοολών που έχουν περισσότερων από δύο (2) άτομα άνθρακα ανά μόριο και έχουν σημαντική διαλυτότητα στο νερό.
Η βουτανόλη βρίσκεται φυσικά ως ένα παραπροϊόν της αλκοολικής ζύμωσης ζάχαρης και άλλων σακχάρων[3]. Γι' αυτό είναι φυσικά παρούσα σε πολλά τρόφιμα και ποτά[4][5]. Είναι επίσης επιτρεπτό τεχνητό αρωματικό πρόσθετο στις ΗΠΑ[6], που χρησιμοποιήθηκε στο βούτυρο, σε κρέμες, σε φρούτα, σε ρούμι, σε ουΐσκι, σε παγωτά, σε γρανίτες, σε ζαχαρώδη, σε αρτοσκευάσματα, σε λικέρ[7], καθώς και σε μεγάλο εύρος άλλων καταναλωτικών προϊόντων[4].
Η μεγαλύτερη χρήση της βουτανόλης είναι ως ένα βιομηχανικό ενδιάμεσο, ειδικότερα για την παραγωγή αιθανικού βουτυλεστέρα, που χρησιμοποιείται ως τεχνητό αρωματικό πρόσθετο και ως βιομηχανικός διαλύτης. Η βουτανόλη είναι είναι πετροχημικό προϊόν, παραγώμενο από το προπένιο και συνήθως χρησιμοποιείται κοντά στη μονάδα παραγωγής της. Η εκτιμώμενη ετήσια παραγωγή της ήταν το 1997 784.000 τόννοι από τις ΗΠΑ, 575.000 τόννοι από τη Δυτική Ευρώπη και 225.000 τόννοι από την Ιαπωνία[5].
Η ονομασία «1-βουτανόλη» προέρχεται από την ονοματολογία κατά IUPAC. Συγκεκριμένα, το πρόθεμα «βουτ-» δηλώνει την παρουσία τεσσάρων (4) ατόμων άνθρακα ανά μόριο της ένωσης, το ενδιάμεσο «-αν-» δείχνει την παρουσία μόνο απλών δεσμών μεταξύ ατόμων άνθρακα στο μόριο και η κατάληξη «-όλη» φανερώνει ότι περιέχει ένα υδροξύλιο ως κύρια χαρακτηριστική ομάδα, δηλαδή ότι πρόκειται για αλκοόλη. Τέλος, στην αρχή τοποθετείται ο αριθμός θέσης του ατόμου άνθρακα στο οποίο συνδέεται το υδροξύλιο (1-), ώστε να υπάρχει διαχωρισμός των ισομερών προπανολών.
| Δεσμοί[8]
|
| Δεσμός |
τύπος δεσμού |
ηλεκτρονική δομή |
Μήκος δεσμού |
Ιονισμός
|
| C-H |
σ |
2sp3-1s |
109 pm |
3% C- H+
|
| C-C |
σ |
2sp3-2sp3 |
154 pm |
|
| C-O |
σ |
2sp3-2sp3 |
150 pm |
19% C+ O-
|
| O-H |
σ |
2sp3-1s |
96 pm |
32% H+ O-
|
Κατανομή φορτίων
σε ουδέτερο μόριο
|
| O |
-0,51
|
| C#4 |
-0,09
|
| C#2-#3 |
-0,06
|
| Η (C-H) |
+0,03
|
| C#1 |
+0,13
|
| Η (O-H) |
+0,32
|
Κάποιες φερμομόνες κινδύνου που ανακαλύφθηκαν από τον αδένα μελιού Koschevnikov των μελισσών περιέχουν 1-βουτανόλη.
Η 1-βουτανόλη υπάρχει φυσικά ως ένα παραπροϊόν της ζύμφωσης σακχάρων σε έναν αριθμό οινοπνευματωδών ποτών, που περιλαμβάνουν τη μπύρα[9], το κονιάκ[10], το κρασί[11] και το ουΐσκυ[12]. Ακόμη έχει ανιχνευθεί σε αναθυμιάσεις του λυκίσκου[13], κάποιους καρπούς[14], γάλακτος θερμικής επεξεργασίας[15] musk melon,[16], μοσχοπέπονων[16], τυριών[17], μπιζέλια[18] και μαγιρευμένου ρυζιού[19] n-Butanol is also formed during deep frying of corn oil, cottonseed oil, trilinolein, and triolein.[20]. Ακόμη, η 1-βουτανόλη σχηματίζεται στα ακόλουθα έλαια κατά το τηγάνισμα: καλαμποκελαιο, βαμβακέλαιο, τριλινολεΐνη και τριολεΐνη[20].
Η 1-βουτανόλη χρησιμοποιήθηκε ακόμη ως συστατικό σε επεξεργασμένες και τεχνητές αρωματικές ουσίες[21], για την εκχύλιση αποβουτυρωμένης πρωτεΐνης από κρόκο αυγού, φυσικών αρωματικών υλικών, φυτικών ελαίων, μπυρομαγιάς, καθώς και ως ένας διαλύτης για αφαίρεση χρωστικών ουσιών από υγρό στρώμα πρωτεΐνης από πηγμένο γάλα για τυρί[22].
Η 1-βουτανόλη παράγεται βιομηχανικά από το προπένιο, που είναι μια πετροχημική πρώτη ύλη . Το προπένιο αρχικά υδροφορμυλιώνεται (με προσθήκη μονοξειδίου του άνθρακα και υδρογόνου), παρουσία ενός ομογενούς καταλύτη με βάση το ρόδιο, παράγοντας βουτανάλη. Στη συνέχεια, η παραγώμενη βουτανάλη υδρογονώνεται σχηματίζοντας 1-βουτανόλη[5]:


- Οι παρακάτω μέθοδοι πρακτικά δεν εφαρμόζονται, παρά μόνο για την ακαδημαϊκή μελέτη τους:
Από το 1-βουτένιο (παράγωγο του πετρελαίου) με υδροβορίωση και στη υδρόλυση παράγεται 1-βουτανόλη[23]:

- Προσθήκη διβορανίου έχει το ίδιο αποτέλεσμα.
1. Με υδρόλυση βουτυλαγολογονιδίων (CH3CH2CH2CH2X) παράγεται 1-βουτανόλη[24]:

2. Με επίδραση καρβοξυλικών αλάτων (RCOONa) παράγονται αρχικά καρβοξυλικοί βουτυλεστέρες (RCOOCH2CH2CH2CH3), που υδρολόνται προς προπανόλη-1[25]:

Με υδρόλυση βουτυλεστέρων (RCOOCH2CH2CH2CH3) παράγεται 1-βουτανόλη[26]:

Με αναγωγή βουτανάλης (CH3CH2CH2CHO) παράγεται 1-βουτανόλη:
1. Με καταλυτική υδρογόνωση[27]:

2. Με λιθιοαργιλιοϋδρίδιο (LiAlH4)[28]:
![{\displaystyle \mathrm {4CH_{3}CH_{2}CH_{2}CHO+LiAlH_{4}{\xrightarrow {}}Li[Al(CH_{3}CH_{2}CH_{2}CH_{2}O)_{4}]{\xrightarrow {+2H_{2}O}}4CH_{3}CH_{2}CH_{2}CH_{2}OH+LiAlO_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/8aebe507f4e696889bb95e9cfa035abb3f2013a3)
Με αναγωγή βουτανικού οξέος με LiAlH4[28] παράγεται 1-βουτανόλη:

Ο βουτανικός βουτυλεστέρας δίνει αντιδράσεις οξειδοαναγωγής, σχηματίζοντας 1-βουτανόλη[29]:
1. Με νάτριο (Na) και αιθανόλη (CH3CH2OH):

2. Με διυδρογόνο (H2) και νικέλιο (Ni):

3. Με λιθιοαργιλιοτετραϋδρίδιο (LiAlH4):

Με επίδραση νιτρώδους οξέος (ΗΝΟ2) σε 1-βουταναμίνη παράγεται 1-βουτανόλη:[30]:

Αρχίζει με την παραγωγή μεθυλοϊωδίδιου και μετά, με επίδραση οξετανίου σε μεθυλομαγνησιοϊωδίδιο, παράγεται 1-βουτανόλη[31]:
Αρχίζει με την παραγωγή βρωμαιθάνιου και μετά, με επίδραση οξιρανίου σε αιθυλομαγνησιοϊωδίδιο, παράγεται 1-βουτανόλη[31]:
Υπάρχουν δύο (2) μέθοδοι για ανοικοδόμηση 1-προπανόλης προς 1-βουτανόλη[31]:
Αρχίζουν και οι δύο με την παραγωγή 1-βρωμοπροπάνιου και μετά βουτανονιτρίλιου:


1. Υδρόλυση βουτανονιτριλίου προς βουτανικό οξύ και μετά αναγωγή προς 1-βουτανόλη:


2. Αναγωγή προς 1-βουταναμίνη και μετατροπή της τελευταίας σε 1-βουτανόλη:


Με αποικοδόμιση της ανθρακικής αλυσίδας της 1-πεντανόλης προς 1-βουτανόλη[31]:
1. Αντίδραση με αλκαλιμέταλλα[32]:

2. Αντίδραση με αμίδια μετάλλων[33]::

3. Αντίδραση με αιθινικά μέταλλα[34]::

4. Αντίδραση με αντιδραστήρια Grignard[35]::

- Ενδεικτική σειρά οξύτητας ορισμένων ενώσεων: νερό (H2O) > 1-βουτανόλη (CH3CH2CH2CH2OH) > αιθίνιο (HC ≡ CH) > αμμωνία (NH3) > μεθάνιο (CH4).
1. Αντίδραση με υδροϊώδιο[36]:

2. Αντίδραση με άλλα υδραλογόνα (X: F, Cl, Br)[37]:

3. Αντίδραση με ισχυρά χλωριωτικά μέσα[38]:
- 1. Με PCl5:

- 2. Με PCl3[39]:

- Η συγκεκριμένη μέθοδος εφαρμόζεται επίσης για την παραγωγή 1-βρωμοβουτάνιου από 1-βουτανόλη, με την ανάλογη χρήση του τριβρωμιούχου φωσφόρου.
- 3. Με SOCl2[40]:

Με ενδομοριακή αφυδάτωση 1-βουτανόλης παράγεται 1-βουτένιο. Η αντίδραση ευνοείται σε σχετικά υψηλές θερμοκρασίες, >150 °C. Σε χαμηλότερες ευνοείται η διαμοριακή αφυδάτωση που δίνει διβουτυλαιθέρα, ενώ χωρίς καθόλου θέρμανση παράγεται ο όξινος θειικός βουτυλεστέρας (CH3CH2CH2CH2OSO3H), που αποτελεί την ενδιάμεση ένωση για τις αφυδατώσεις.[41]:
![{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}OH{\xrightarrow[{>150^{o}C}]{\pi .H_{2}SO_{4}}}CH_{3}CH_{2}CH=CH_{2}+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/ec6594b1383ef610f259b439c46d772d6ae5bf0f)
Παραγωγή διβουτυλαιθέρα[42]:
![{\displaystyle \mathrm {2CH_{3}CH_{2}CH_{2}CH_{2}OH{\xrightarrow[{<140^{o}C}]{H_{2}SO_{4}}}CH_{3}CH_{2}CH_{2}CH_{2}OCH_{2}CH_{2}CH_{2}CH_{3}+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/38e67d399ba210fead8276daadac4446b360d97c)
Αντίδραση με ακυλιωτικά μέσα:
1. Εστεροποίηση με καρβοξυλικό οξύ[43]:

2. Εστεροποίηση με ανυδρίτη καρβοξυλικού οξέος[44]:

3. Εστεροποίηση με ακυλαλογονίδιο[45]:

1. Με υπερμαγγανικό κάλιο (KMnO4). Παράγεται βουτανικό οξύ[46]:

2. Με τριοξείδιο του χρωμίου (CrO3). Παράγεται αρχικά βουτανάλη και στη συνέχεια, με περίσσεια τριοξειδίου του χρωμίου, βουτανικό οξύ[47]:

- Η διαφορά είναι ότι στην περίπτωση #2, η οξείδωση μπορεί να σταματήσει στην βουτανάλη.
Με αποικοδόμηση της ανθρακικής αλυσίδας της αιθανόλης παράγεται 1-προπανόλη[31]::
Υπάρχουν δύο (2) μέθοδοι για ανοικοδόμηση 1-βουτανόλης προς 1-πεντανόλη[31]:
Αρχίζουν και οι δύο με την παραγωγή 1-ιωδοβουτάνιου και μετά πεντανονιτρίλιου:


1. Υδρόλυση πεντανονιτριλίου προς πεντανικό οξύ και μετά αναγωγή προς 1-πεντανόλη:


2. Αναγωγή προς 1-πενταναμίνη και μετατροπή της τελευταίας σε 1-πεντανόλη:


Αρχίζει με την παραγωγή 1-ιωδοβουτάνιου και μετά, με επίδραση οξιρανίου σε βουτυλομαγνησιοϊωδίδιο, παράγεται 1-εξανόλη[31]:
Με επίδραση σε εποξυαιθάνιο παράγεται 2-βουτοξυαιθανόλη[48]:


Παρεμβολή καρβενίων, π.χ. με μεθυλενίου παράγονται 1-πεντανόλη, 2-πεντανόλη, 2-μεθυλο-1-βουτανόλη, 3-μεθυλο-1-βουτανόλη και βουτυλομεθυλαιθέρας[49]:

Η 1-βουτανόλη είναι ένα βιομηχανικό ενδιάμεσο για την παραγωγή προπενικού βουτυλεστέρα, σιθανικού βουτυλεστέρα, φθαλικού διβουτυλοδιεστέρα, σεβακικού διβουτυλοδιεστέρα[21][50] , καθώς και άλλων χρήσιμων βουτυλεστέρων και βουτυλαιθέρων. Άλλες βιομηχανικές χρήσεις της 1-βουτανόλης περιλαμβάνουν την παραγωγή φαρμακευτικών, πολυμερών, ζιζανιοκτόνων[51], καθώς και κάποιων ρητινών[5].
Η 1-βουτανόλη χρησιμοποιήθηκε ως ένα συστατικό σε αρώματα και ως ένας διαλύτης για την εκχύλιση αιθέριων ελαίων[21]. Χρησιμοποιήθηκε ακόμη ως ένας εκχυλιστής στην παραγωγή αντιβιοτικών, ορμονών και βιταμινών[21][50]. Χρησιμοποιήθηκε ακόμη ως διαλύτης για μπογιές, επιστρώσεις, φυσικές ρητίνες, μαστίχες, συνθετικές ρητίνες, βερνίκια, αλκαλοειδή και καμφορά[21][50]. Διάφορες άλλες εφαρμογές της 1-βουτανόλης είναι ως μέσο διόγκωσης σε υφάσματα, ως συστατικό του υγρού φρένων, ως συστατικό καθαριστικών, απογρασωτικών, εντομοαπωθητικών[4], μέσων επίπλευσης μεταλλευμάτων[51] και ξυλοθεραπευτικών συστημάτων[52].
Η 1-βουτανόλη προτάθηκε ως ένα υποκατάστατο ντίζελ και βενζίνης. Παράγεται σε μικρές ποσότητες ως παραπροϊόν σχεδόν σε όλες τις ζυμώσεις, αλλά κάποια είδη του κλωστρίδιου (Clostridium) την παράγουν σε υψηλότερες αποδόσεις, ενώ υπάρχουν σε εξέλιξη έρευνες για ακόμη μεγαλύτερη παραγωγή βιο-1-βουτανόλης από βιομάζα.
Η παραγωγή ή η χρήση κάποιων από τα ακόλουθα προϊόντα μπορεί να έχει ως αποτέλεσμα στην έκθεση σε 1-βουτανόλη: τεχνητό δέρμα, βουτυστέρες, «λαστιχένιο τσιμέντο», βερνίκια, εκχυλίσματα φρούτων, λικέρ, κινηματογραφικές ταινίες, φωτογραφικά φιλμ, αδιάβροχα, αρώματα, τεχνητό μετάξι, γυαλιά ασφάλειας, γομαλάκα βερνίκια και αδιάβροχα ρούχα[4].
Η 1-βουτανόλη απορροφάται γρήγορα μέσω της πεπτικής οδού και των πνευμόνων, καθώς επίσης και από κάποια επαφή από το δέρμα[53]. Μεταβολίζεται τελείως στα σπονδυλωτά παρόμοια με την αιθανόλη: Η αλκοολική δεϋδρογονάση μετατρέπει την 1-βουταβόλη σε βουτανάλη. Αυτή μετατρέπεται σε βουτανικό οξύ από τη δεϋδρογονάση της αιθανάλης. Το παραγώμενο βουτανικό οξύ μπορεί να μεταβολιστεί πλήρω; σε διοξείδιο του άνθρακα και νερό από την μεταβολική οδό της β-οξείδωσης, της οποίας άλλωστε αποτελεί το προτελευταίο στάδιο. Πειράματα που έγιναν σε ποντίκια έδειξαν ότι μόλις το 0,03% μιας δόσης 2 g/kg 1-βουτανόλης αποβλήθηκε ανέπαφο από τα ούρα τους[54].
Η ακριβής τοξικότητα της 1-βουτανόλης είναι σχετικά χαμηλή, με την LD50 να κυμαίνεται από 2290 – 4360 mg/kg, δηλαδή συγκρίσιμη μ' αυτήν της αιθανόλης, που αντίστοιχα είναι 7000–15000 mg/kg.[5][55]. Δεν αναφέρθηκε κανένας θάνατος μετά από εισπνοή 1-βουτανόλης με συφκέντρωση 8000 ppm επί τετράωρο από ποντίκια. Σε δόσεις μικρότερες από τη θανατηφόρα, η 1-βουτανόλη δρα με παρόμοιο δυσάρεστο τρόπο στο κεντρικό νευρικό σύστημα. Μια σχετική έρευνα σε ποντίκια έδειξε ότι η μέθη από 1-βουτανόλη είναι εξαπλάσια από αυτήν από αιθανόλη, πιθανότατα γιατί η εξουδετέρωσή της από την αλκοολική δεϋδρογονάση είναι πιο αργή[56].
Η 1-βουτανόλη είναι ένα φυσικό συστατικό σε πολλά οινοπνευματώδη ποτά, αν και σε χαμηλές αλλά κυμαινόμενες συγκεντρώσεις[57][58]. Μαζί με άλλα παρόμοια ζυμέλαια είναι υπεύθυνη για σοβαρές περιπτώσεις μέθης, αν και πειράματα σε ζώα δεν έδωσαν ενδείξεις γι' αυτό[59].
Η υγρή 1-βουτανόλη είναι, όπως είναι πολύ συνηθισμένο με τους περισσότερους οργανικούς διαλύτες, είναι εξαιρετικά ερεθιστική για τα μάτια, αλλά επαναλαμβανόμενη επαφή μπορεί να προκαλέσει ερεθισμό και στο δέρμα[5]. Αυτό πιστεύεται ότι είναι το γενικό αποτέλεσμα από την αφαίρεση του υποδόρειου λίπους. Ωστόσο, δεν έχει παρατηρηθεί ευαισθητοποίηση του δέρματος. Ο ερεθισμός στις αναπνευστικές οδούς συμβαίνει μόνο σε πολύ υψηλές συγκεντρώσεις (>2400 ppm).[60].
Έχοντας ως ελάχιστη θερμοκρασία ανάφλεξης τους 29 °C, η 1-βουτανόλη παρουσιάζει ένα μέτριο κίνδυνο ανάφλεξης. Είναι λίγο πιο εύφλεκτη από την κηροζίνη ή το ντίζελ, αλλά λιγότερο εύφλεκτη από τους περισσότερους άλλους οργανικούς διαλύτες. Η δυσάρεστη επίδραση της 1-βουτανόλης στον εγκέφαλο (παρόμοια με τη μέθη από την αιθανόλη) είναι ένας δυνητικός κίνδυνος όταν κάποιοι εργάζονται χρησιμοποιώντας 1-βουτανόλη σε κλειστούς χώρους, αν και το κατώφλι όσφρησης για την 1-βουτανόλη (0,2–30 ppm) είναι πολύ χαμηλότερο από τις συγκεντρώσεις με κάποιο νευρολογικό αποτέλεσμα[60][61].
Η 1-βουτανόλη έχει (σχετικά) χαμηλή τοξικότητα για την υδάτινη χλωρίδα και πανίδα. Βιοαποικοδομείται γρήγορα στο νερό, ενώ στον αέρα δημιουργεί ελεύθερες ρίζες υδροξυλίου με ημιζωή 1,2 - 2,3 ημέρες. Επίσης έχει χαμηλό δυναμικό βιοσυσσώρευσης[5]. Ένας δυνητικός κίνδυνος που δημιουργεί η παρουσία της σε υδάτινα περιβάλλοντα είναι η αυξημένη χημική απαίτηση οξυγόνου (C.O.D.) που σχετίζεται με τη βιοαποικοδόμησή της.
- ↑ http://chem.sis.nlm.nih.gov/chemidplus/
- ↑ Για εναλλακτικές ονομασίες δείτε τον πίνακα πληροφοριών.
- ↑ Hazelwood, Lucie A.; Daran, Jean-Marc; van Maris, Antonius J. A.; Pronk, Jack T.; Dickinson, J. Richard (2008), "The Ehrlich pathway for fusel alcohol production: a century of research on Saccharomyces cerevisiae metabolism", Appl. Environ. Microbiol. 74 (8): 2259–66, doi:10.1128/AEM.02625-07, PMC 2293160, PMID 18281432.
- ↑ 4,0 4,1 4,2 4,3 Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9.
- ↑ 5,0 5,1 5,2 5,3 5,4 5,5 5,6 n-Butanol, SIDS Initial Assessment Report, Geneva: United Nations Environment Programme, April 2005.
- ↑ 21 C.F.R. § 172.515; 42 FR 14491, Mar. 15, 1977, as amended.
- ↑ Hall, R. L.; Oser, B. L. (1965), "Recent progress in the consideration of flavouring ingredients under the food additives amendement. III. Gras substances", Food Technol.: 151, cited in Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9.
- ↑ Τα δεδομένα προέρχονται εν μέρει από το «Table of periodic properties of the Ellements», Sagrent-Welch Scientidic Company και Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, Σελ. 34.
- ↑ Bonte, W. (1979), «Congener substances in German and foreign beers», Blutalkohol 16: 108–24 , cited in Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9, http://www.inchem.org/documents/ehc/ehc/ehc65 [νεκρός σύνδεσμος].
- ↑ Schreier, Peter; Drawert, Friedrich; Winkler, Friedrich (1979), «Composition of neutral volatile constituents in grape brandies», J. Agric. Food Chem. 27 (2): 365–72, doi:10.1021/jf60222a031 .
- ↑ Bonte, W. (1978), «Congener content of wine and similar beverages», Blutalkohol 15: 392–404 , cited in Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9, http://www.inchem.org/documents/ehc/ehc/ehc65 [νεκρός σύνδεσμος].
- ↑ Postel, W.; Adam, L. (1978), «Gas chromatographic characterization of whiskey. III. Irish whiskey», Branntweinwirtschaft 118: 404–7 , cited in Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9, http://www.inchem.org/documents/ehc/ehc/ehc65 [νεκρός σύνδεσμος].
- ↑ Tressl, Roland; Friese, Lothar; Fendesack, Friedrich; Koeppler, Hans (1978), «Studies of the volatile composition of hops during storage», J. Agric. Food Chem. 26 (6): 1426–30, doi:10.1021/jf60220a036 .
- ↑ Swords, G.; Bobbio, P. A.; Hunter, G. L. K. (1978), «Volatile constituents of jack fruit (Arthocarpus heterophyllus)», J. Food Sci. 43 (2): 639–40, doi:10.1111/j.1365-2621.1978.tb02375.x .
- ↑ Jaddou, Haytham A.; Pavey, John A.; Manning, Donald J. (1978), «Chemical analysis of flavor volatiles in heat-treated milks», J. Dairy Res. 45 (3): 391–403, doi:10.1017/S0022029900016617 .
- ↑ 16,0 16,1 Yabumoto, K.; Yamaguchi, M.; Jennings, W. G. (1978), «Production of volatile compounds by Muskmelon, Cucumis melo», Food Chem. 3 (1): 7–16, doi:10.1016/0308-8146(78)90042-0 .
- ↑ Dumont, Jean Pierre; Adda, Jacques (1978), «Occurrence of sesquiterpones in mountain cheese volatiles», J. Agric. Food Chem. 26 (2): 364–67, doi:10.1021/jf60216a037 .
- ↑ Fisher, Gordon S.; Legendre, Michael G.; Lovgren, Norman V.; Schuller, Walter H.; Wells, John A. (1979), «Volatile constituents of southernpea seed [Vigna unguiculata (L.) Walp.]», J. Agric. Food Chem. 27 (1): 7–11, doi:10.1021/jf60221a040 .
- ↑ Yajima, Izumi; Yanai, Tetsuya; Nakamura, Mikio; Sakakibara, Hidemasa; Habu, Tsutomu (1978), «Volatile flavor components of cooked rice», Agric. Biol. Chem. 42 (6): 1229–33, http://www.journalarchive.jst.go.jp/jnlpdf.php?cdjournal=bbb1961&cdvol=42&noissue=6&startpage=1229&lang=en&from=jnlabstract [νεκρός σύνδεσμος].
- ↑ 20,0 20,1 Chang, S. S.; Peterson, K. J.; Ho, C. (1978), «Chemical reactions involved in the deep-fat frying of foods», J. Am. Oil Chem. Soc.: 718–27 , cited in Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9, http://www.inchem.org/documents/ehc/ehc/ehc65 [νεκρός σύνδεσμος].
- ↑ 21,0 21,1 21,2 21,3 21,4 Mellan, I. (1950), Industrial Solvents, New York: Van Nostrand Reinhold, σελ. 482–88 , cited in Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9, http://www.inchem.org/documents/ehc/ehc/ehc65 [νεκρός σύνδεσμος].
- ↑ Bray, Walter J.; Humphries, Catherine (1978), «Solvent fractionation of leaf juice to prepare green and white protein products», J. Sci. Food Agric. 29 (10): 839–46, doi:10.1002/jsfa.2740291003 .
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 156, §6.8.5.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.197, §8.2.3α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.197, §8.2.3β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.198, §8.2.5.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 218, §9.2.2.
- ↑ 28,0 28,1 Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 197, §8.2.2α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 307, §13.7.5.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.198, §8.2.6.
- ↑ 31,0 31,1 31,2 31,3 31,4 31,5 31,6 Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.198, §8.2.7.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.2.4α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.2.4β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.2.4γ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.2.4δ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.4.2β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.4.2γ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.4.3α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.4.3β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.4.3γ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.153, §6.3.3.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.4.5β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.4.4α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.4.4β.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.199, §8.4.4γ.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.200, §8.4.6α.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.200, §8.4.6β.
- ↑ Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §2.1., σελ. 16-17, εφαρμογή γενικής αντίδρασης για Nu = CH3CH2CH2CH2O-.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 155, §6.7.3.
- ↑ 50,0 50,1 50,2 Doolittle, A. K. (1954), The Technology of Solvents and Plasticizers, New York: Wiley, σελ. 644–45 , cited in Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9, http://www.inchem.org/documents/ehc/ehc/ehc65 [νεκρός σύνδεσμος].
- ↑ 51,0 51,1 Monich, J. A. (1968), Alcohols: Their Chemistry, Properties, and Manufacture, New York: Chapman and Reinhold , cited in Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9, http://www.inchem.org/documents/ehc/ehc/ehc65 [νεκρός σύνδεσμος].
- ↑ ZA 7801031, Amundsen, J.; R. J. Goodwin & W. H. Wetzel, "Water-soluble pentachlorophenol and tetrachlorophenol wood-treating systems", published 28 Feb. 1979.
- ↑ Theorell, Hugo; Bonnichsen, Roger; Holtermann, Hugo; Sörensen, JöRgine Stene; Sörensen, Nils Andreas (1951), «Studies on Liver Alcohol Dehydrogenase I. Equilibria and Initial Reaction Velocities», Acta. Chem. Scand. 5: 1105–26, doi:10.3891/acta.chem.scand.05-1105, http://actachemscand.dk/pdf/acta_vol_05_p1105-1126.pdf, ανακτήθηκε στις 2013-01-22 . Winer, Alfred D.; Nurmikko, V.; Hartiala, K.; Hartiala, K.; Veige, S.; Diczfalusy, E. (1958), «A Note of the Substrate Specificity of Horse Liver Alcohol Dehydrogenase», Acta. Chem. Scand. 12: 1695–96, doi:10.3891/acta.chem.scand.12-1695, http://actachemscand.dk/pdf/acta_vol_12_p1695-1696.pdf, ανακτήθηκε στις 2013-01-22 . Merritt, A. Donald; Tomkins, Gordon M. (1959), «Reversible Oxidation of Cyclic Secondary Alcohols by Liver Alcohol Degydrogenase», J. Biol. Chem. 234 (10): 2778–82, http://www.jbc.org/cgi/reprint/234/10/2778, ανακτήθηκε στις 2013-01-22 . von Wartburg, Jean-Pierre; Bethane, J. L.; Vallee, B. L. (1964), «Human Liver Alcohol Dehydrogenase: Kinetic and Physiochemical Properties», Biochemistry 3 (11): 1775–82, doi:10.1021/bi00899a033 .
- ↑ Gaillard, D.; Derache, R. (1965), «Métabilisation de différents alcools présents dans les biossons alcooliques chez le rat», Trav. Soc. Pharmacol. Montpellier 25: 541–62 , cited in Butanols: four isomers, Environmental Health Criteria monograph No. 65, Geneva: World Health Organization, 1987, ISBN 92-4-154265-9, http://www.inchem.org/documents/ehc/ehc/ehc65 [νεκρός σύνδεσμος].
- ↑ Ethanol (PDF), SIDS Initial Assessment Report, Geneva: United Nations Environment Programme, August 2005
- ↑ McCreery, N. J.; Hunt, W. A. (1978), «Physico-chemical correlates of alcohol intoxication», Neuropharmacology 17 (7): 451–61, doi:10.1016/0028-3908(78)90050-3, PMID 567755 .
- ↑ Woo, Kang-Lyung (2005), «Determination of low molecular weight alcohols including fusel oil in various samples by diethyl ether extraction and capillary gas chromatography», J. AOAC Int. 88 (5): 1419–27, doi:10.5555/jaoi.2005.88.5.1419, PMID 16385992 .
- ↑ Lachenmeier, Dirk W.; Haupt, Simone; Schulz, Katja (2008), «Defining maximum levels of higher alcohols in alcoholic beverages and surrogate alcohol products», Regulat. Toxicol. Pharmacol. 50 (3): 313–21, doi:10.1016/j.yrtph.2007.12.008, PMID 18295386 .
- ↑ Hori, Hisako; Fujii, Wataru; Hatanaka, Yutaka; Suwa, Yoshihide (2003), «Effects of fusel oil on animal hangover models», Alcohol Clin. Exp. Res. 27 (8 Suppl): 37S–41S, doi:10.1097/01.ALC.0000078828.49740.48, PMID 12960505 .
- ↑ 60,0 60,1 Wysocki, C. J.; Dalton, P. (1996), Odor and Irritation Thresholds for 1-Butanol in Humans, Philadelphia: Monell Chemical Senses Center , cited in n-Butanol (PDF), SIDS Initial Assessment Report, Geneva: United Nations Environment Programme, April 2005.
- ↑ Cometto-Muñiz, J. Enrique; Cain, William S. (1998), «Trigeminal and Olfactory Sensitivity: Comparison of Modalities and Methods of Measurement», Int. Arch. Occup. Environ. Health 71 (2): 105–10, doi:10.1007/s004200050256, PMID 9580447 .
- Βάρβογλης Α. "Χημεία Οργανικών Ενώσεων", Θεσσαλονίκη 1986.
- Μανωλκίδης Κ., Μπέζας Κ. "Στοιχεία οργανικής χημείας", Έκδοση 13η, Αθήνα 1985.
- Αλεξάνδρου Ν. Ε. "Γενική Οργανική Χημεία, Δομή-Φάσματα-Μηχανισμοί", Τόμοι 1ος και 2ος, Θεσσαλονίκη 1985.
- Τσακιστράκης Α. "Οργανική Χημεία", Αθήνα 1993
- Κεχαγιόγλου Α. Χ. "Βιομηχανική Οργανική Χημεία", Θεσσαλονίκη 1989.
- Morrison R. T., Boyd R. N. "Οργανική Χημεία" Τόμοι 1ος,2ος,3ος, Μετάφραση:Σακαρέλλος-Πηλίδης-Γεροθανάσης, Ιωάννινα 1991.
- Meislich H., Nechamkin H., Sharefkin J. "Οργανική Χημεία", Μετάφραση:Βάρβογλης Α., Αθήνα 1983.
- Ιακώβου Π. "Οργανική Χημεία. Σύγχρονη Θεωρία και Ασκήσεις", Θεσσαλονίκη 1995.
- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- Δημήτριου Ν. Νικολαΐδη: Ειδικά μαθήματα Οργανικής Χημείας, Θεσσαλονίκη 1983.
- Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985
| π • σ • ε
Αλκοόλες |
|---|
| | Αλκανόλες | | | | Αλκενόλες | | | | Κυκλοαλκανόλες | | | | Αλαλκοόλες | | | | Αλκινόλες | | | | Αλκανοδιόλες | | | | Αλκενοδιόλες | | | | Αλκοξυαλκανοδιόλες | | | | Αλκανοτριόλες | | | | Αλκανοτετρόλες | | | | Αρωματικές αλκοόλες | | | | Ετεροκυκλικές αλκοόλες | | | | Ετεροαρωματικές αλκοόλες | | |
Μερικές αλκενόλες, αλκινόλες και αλκανοδιόλες είναι ασταθείς. Οι αρωματικές αλκοόλες με υδροξύλιο απευθείας ενωμένο με το αρωμστικό σύστημα βενζολίου ή παραγώγων του αποκαλούνται αρενόλες, υποσύνολο των οποίων αποτελούν οι φαινόλες. |
|











![{\displaystyle \mathrm {4CH_{3}CH_{2}CH_{2}CHO+LiAlH_{4}{\xrightarrow {}}Li[Al(CH_{3}CH_{2}CH_{2}CH_{2}O)_{4}]{\xrightarrow {+2H_{2}O}}4CH_{3}CH_{2}CH_{2}CH_{2}OH+LiAlO_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/8aebe507f4e696889bb95e9cfa035abb3f2013a3)
































![{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}OH{\xrightarrow[{>150^{o}C}]{\pi .H_{2}SO_{4}}}CH_{3}CH_{2}CH=CH_{2}+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/ec6594b1383ef610f259b439c46d772d6ae5bf0f)
![{\displaystyle \mathrm {2CH_{3}CH_{2}CH_{2}CH_{2}OH{\xrightarrow[{<140^{o}C}]{H_{2}SO_{4}}}CH_{3}CH_{2}CH_{2}CH_{2}OCH_{2}CH_{2}CH_{2}CH_{3}+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/38e67d399ba210fead8276daadac4446b360d97c)



















