セレギリン
IUPAC命名 めいめい 法 ほう による物質 ぶっしつ 名 めい
(R )-N -methyl-N -(1-pheny
lpropan-2-yl)prop-3-yn-1-amine 臨床 りんしょう 発音 はつおん
sə-LEJ -i-leen 販売 はんばい 名 めい
Eldepryl, Jumex, Zelapar, Emsam, others[ 1] Drugs.com
monograph MedlinePlus
a697046 ライセンス
US FDA :リンク 胎児 たいじ 危険 きけん 度 ど 分類 ぶんるい
法的 ほうてき 規制 きせい
投与 とうよ 経路 けいろ
By mouth , transdermal (patch ) 薬物 やくぶつ 動態 どうたい 生物 せいぶつ 学 がく 的 てき 利用 りよう 能 のう 10% (oral), 73% (patch) 血漿 けっしょう 結合 けつごう 94% 代謝 たいしゃ Intestines and liver 代謝 たいしゃ 物質 ぶっしつ N -Desmethylselegiline, L -amphetamineL -methamphetamine半減 はんげん 期 き 10 hours (oral)[要 よう 出典 しゅってん , 18–25 hours[要 よう 出典 しゅってん (transdermal) 排泄 はいせつ Urine 識別 しきべつ CAS番号 ばんごう
14611-51-9 14611-52-0 (HCl ) ATCコード
N04BD01 (WHO QN06AX90 (WHO PubChem
CID: 26757 IUPHAR/BPS
6639 DrugBank
DB01037 ChemSpider
24930 UNII
2K1V7GP655 KEGG
D03731 ChEBI
CHEBI:9086 ChEMBL
CHEMBL972 別名 べつめい
L -Deprenyl; (R )-(–)-N ,α あるふぁ N -2-propynylphenethylamine; (R )-(–)-N -Methyl-N -2-propynylamphetamine; (R )-(–)-N -2-propynylmethamphetamine 化学 かがく 的 てき 化学 かがく 式 しき C 13 H 17 N 分子 ぶんし 量 りょう 187.281
C#CCN([C@@H](Cc1ccccc1)C)C
InChI=1S/C13H17N/c1-4-10-14(3)12(2)11-13-8-6-5-7-9-13/h1,5-9,12H,10-11H2,2-3H3/t12-/m1/s1 Key:MEZLKOACVSPNER-GFCCVEGCSA-N テンプレートを表示 ひょうじ
セレギリン (英 えい Selegiline )は、パーキンソン病 びょう および大 だい 病 びょう 性 せい 障害 しょうがい 治療 ちりょう 使用 しよう 薬 くすり [ 1] L -deprenyl知 し 名 めい エフピー 、Eldepryl 、Emsamの下 した 販売 はんばい 病 びょう 経口 けいこう 摂取 せっしゅ 錠剤 じょうざい 形 かたち 病 びょう 皮膚 ひふ 適用 てきよう パッチ として提供 ていきょう 日本 にっぽん 経口 けいこう 投与 とうよ 錠剤 じょうざい 後述 こうじゅつ
セレギリンはモノアミンオキシダーゼ阻害 そがい 剤 ざい として作用 さよう 脳 のう 内 ない モノアミン神経 しんけい 伝達 でんたつ 物質 ぶっしつ のレベルを増加 ぞうか 典型 てんけい 的 てき 臨床 りんしょう 用量 ようりょう 選択 せんたく 的 てき 不 ふ 可逆 かぎゃく 的 てき モノアミンオキシダーゼB (MAO-B)の阻害 そがい 剤 ざい 脳 のう 内 ない ドーパミン のレベルを増加 ぞうか 高 こう 用量 ようりょう 特異 とくい 性 せい 失 うしな MAO-A も阻害 そがい 脳 のう 内 ない セロトニン 、ノルエピネフリン 、およびドーパミンのレベルを増加 ぞうか
錠剤 じょうざい 形 かたち パーキンソン病 びょう の症状 しょうじょう 治療 ちりょう 使用 しよう [ 2] 単 たん 剤 ざい 療法 りょうほう 適応 てきおう 外 がい 使用 しよう レボドパ (L -DOPA)などの薬物 やくぶつ 補助 ほじょ 剤 ざい 最 もっと 使用 しよう [ 3] [ 4] 追加 ついか 理論 りろん 的 てき 根拠 こんきょ 必要 ひつよう 用量 ようりょう 減 へ 療法 りょうほう 運動 うんどう 合併症 がっぺいしょう 減 へ [ 5] 治療 ちりょう 必要 ひつよう 時点 じてん 診断 しんだん 後 ご 約 やく 月 げつ 約 やく 月 げつ 遅 おく [ 6] 神経 しんけい 保護 ほご 剤 ざい 作用 さよう 疾患 しっかん 進行 しんこう 速度 そくど 低下 ていか 議論 ぎろん
セレギリンはまた、アルツハイマー病 びょう における認知 にんち 症 しょう 緩和 かんわ 治療 ちりょう 適応 てきおう 外 がい 使用 しよう [ 4]
日本 にっぽん 病 びょう 治療 ちりょう 剤 ざい 選択 せんたく 的 てき 阻害 そがい 剤 ざい 塩酸 えんさん 塩 しお 錠剤 じょうざい 医薬品 いやくひん 先発 せんぱつ 品 ひん 錠 じょう 口腔 こうくう 内 ない 崩壊 ほうかい 錠 じょう 錠 じょう
セレギリンはまた、大 だい 病 びょう 性 せい 障害 しょうがい 治療 ちりょう 経 けい 皮 がわ 投与 とうよ [ 7] [ 8]
2015年 ねん 発表 はっぴょう 量的 りょうてき 重要 じゅうよう 試験 しけん 結果 けっか 症状 しょうじょう 軽減 けいげん 治療 ちりょう 必要 ひつよう 数 すう 効果 こうか 大 おお 兆候 ちょうこう 数 かず 少 すく 方 ほう 良 よ 寛解 かんかい [ 8] 害 がい 及 およ 必要 ひつよう 数 かず 逆数 ぎゃくすう 高 たか 数 かず 望 のぞ 性的 せいてき 副作用 ふくさよう 適用 てきよう 部位 ぶい 反応 はんのう 範囲 はんい 救 すく 害 がい 受 う 可能 かのう 性 せい 関 かん 分析 ぶんせき 寛解 かんかい 可能 かのう 性 せい 副作用 ふくさよう 中止 ちゅうし 可能 かのう 性 せい 倍 ばい 高 たか 示 しめ 寛解 かんかい 不眠症 ふみんしょう 発生 はっせい 率 りつ 寛解 かんかい 不眠症 ふみんしょう 中止 ちゅうし 寛解 かんかい 不眠症 ふみんしょう 性 せい 機能 きのう 障害 しょうがい 非常 ひじょう 低 ひく
日本 にっぽん 剤 ざい 販売 はんばい
注意 ちゅうい 欠陥 けっかん 多 た 動 どう 性 せい 障害 しょうがい [ 編集 へんしゅう ] 一部 いちぶ 研究 けんきゅう 子供 こども [ 9] [ 10] [ 11] 成人 せいじん 両方 りょうほう 注意 ちゅうい 欠陥 けっかん 多 た 動 どう 性 せい 障害 しょうがい 治療 ちりょう メチルフェニデート と同 おな 効果 こうか 的 てき 副作用 ふくさよう 特 とく 食欲 しょくよく 抑制 よくせい 不安 ふあん 頭痛 ずつう 睡眠 すいみん 妨害 ぼうがい 少 すく [ 12] [ 13] パーキンソン病 びょう の治療 ちりょう 使用 しよう MAO-B阻害 そがい 剤 ざい であるセレギリンは、チトクロームP450 によってL- デスメチルセレギリン、L- アンフェタミン、およびL- メタンフェタミンに代謝 たいしゃ [ 14] [ 15]
ヒトへのすべての用途 ようと 剤 ざい 型 がた 妊娠 にんしん 妊娠 にんしん 実験 じっけん 動物 どうぶつ 用 もち 研究 けんきゅう 胎児 たいじ 悪影響 あくえいきょう 示 しめ 対象 たいしょう 適切 てきせつ 研究 けんきゅう 無 な [ 2] [ 7]
レボドパ と併用 へいよう 錠剤 じょうざい 副作用 ふくさよう 頻度 ひんど 高 たか 順 じゅん 吐 は 気 け 幻覚 げんかく 錯乱 さくらん うつ病 びょう 、バランスの喪失 そうしつ 、不眠症 ふみんしょう 不 ふ 随意 ずいい 運動 うんどう 増加 ぞうか 興奮 こうふん 徐 じょ 脈 みゃく 不整脈 ふせいみゃく 妄想 もうそう 高血圧 こうけつあつ 狭心症 きょうしんしょう 発症 はっしょう 増加 ぞうか 失神 しっしん [ 2] 副作用 ふくさよう 高 こう 伝達 でんたつ 原因 げんいん 用量 ようりょう 減 へ 緩和 かんわ [ 1]
うつ病 びょう 剤 ざい 主 おも 副作用 ふくさよう 貼付 ちょうふ 部位 ぶい 反応 はんのう 不眠症 ふみんしょう 下痢 げり 喉 のど 痛 いた [ 7] 特 とく 若 わか 人 ひと 対 たい 自殺 じさつ 企図 きと 上昇 じょうしょう 可能 かのう 性 せい 黒枠 くろわく 警告 けいこく 年 ねん 以降 いこう 抗 こう 薬 やく 同様 どうよう [ 16]
経口 けいこう 剤 ざい 剤 ざい 両方 りょうほう セロトニン症候群 しょうこうぐん を引 ひ 起 お 可能 かのう 性 せい 薬物 やくぶつ SSRI や咳 せき 止 と 薬 やく デキストロメトルファン など)を組 く 合 あ 対 たい 強 つよ 警告 けいこく 表示 ひょうじ [ 2] [ 7] [ 17] 鎮痛 ちんつう 薬 やく ペチジン の併用 へいよう 深刻 しんこく 副作用 ふくさよう 引 ひ 起 お 可能 かのう 性 せい 推奨 すいしょう トラマドール やメタドン などのいくつかの他 ほか 合成 ごうせい トリプタン は 、セロトニン症候群 しょうこうぐん 可能 かのう 性 せい 禁忌 きんき [ 18] [ 19]
エチニルエストラジオールとプロゲスチンを含 ふく 経口 けいこう 避妊 ひにん 薬 やく バイオアベイラビリティ を10倍 ばい 倍 ばい 増加 ぞうか [ 20] 血 ち 中 ちゅう 濃度 のうど 上 あ 選択 せんたく 性 せい 喪失 そうしつ 可能 かのう 性 せい 同様 どうよう 阻害 そがい 始 はじ 可能 かのう 性 せい 作動 さどう 薬 やく 組 く 合 あ チラミン 誘発 ゆうはつ 性 せい 高 だか 血圧 けつあつ 発症 はっしょう 毒性 どくせい 非 ひ 選択 せんたく 的 てき MAOI の副作用 ふくさよう 対 たい 感受性 かんじゅせい 高 たか
経口 けいこう 錠剤 じょうざい 剤 ざい 阻害 そがい 剤 ざい 関連 かんれん 高血圧 こうけつあつ 危機 きき 回避 かいひ 食事 しょくじ 制限 せいげん [ 2] [ 7] 剤 ざい 開発 かいはつ 際 さい 食事 しょくじ 制限 せいげん 克服 こくふく 目的 もくてき 臨床 りんしょう 試験 しけん 成功 せいこう 示 しめ 年 ねん 月 がつ 年 ねん 月 がつ 市販 しはん 後 ご 調査 ちょうさ 回 かい 薬物 やくぶつ 曝露 ばくろ 高血圧 こうけつあつ 高血圧 こうけつあつ 可能 かのう 性 せい 自己 じこ 報告 ほうこく 件 けん 客観 きゃっかん 的 てき 臨床 りんしょう 伴 ともな 無 な [ 8] 薬物 やくぶつ 送達 そうたつ 法 ほう 最低 さいてい 用量 ようりょう 時 じ 間 あいだ 食事 しょくじ 制限 せいげん 必要 ひつよう [ 21] 古 ふる 非 ひ 選択 せんたく 的 てき 組 く 合 あ 可逆 かぎゃく 的 てき 阻害 そがい 剤 ざい モクロベミド との組 く 合 あ 経口 けいこう 製剤 せいざい 高 こう 用量 ようりょう 低 ひく チラミン 食 しょく 必要 ひつよう [ 17]
セレギリンはMAO-Bの選択 せんたく 的 てき 阻害 そがい 剤 ざい 共有 きょうゆう 結合 けつごう 不 ふ 可逆 かぎゃく 的 てき 阻害 そがい [ 1] [ 22] 分解 ぶんかい 効果 こうか 発揮 はっき 活性 かっせい 増加 ぞうか [ 23] 神経 しんけい 保護 ほご 特性 とくせい 可能 かのう 性 せい 作動 さどう 放出 ほうしゅつ 遊離 ゆうり 酸素 さんそ 近 ちか 保護 ほご 高 こう 用量 ようりょう 対 たい 選択 せんたく 性 せい 失 うしな 阻害 そがい
セレギリンはCYP2A6も阻害 そがい 結果 けっか ニコチン の効果 こうか 高 たか [ 24] σ しぐま 1 受容 じゅよう 体 たい 活性 かっせい 化 か 受容 じゅよう 体 たい 対 たい 比較的 ひかくてき 高 たか 親和 しんわ 性 せい 有 ゆう 約 やく [ 25] [ 26]
セレギリンの経口 けいこう バイオアベイラビリティ は約 やく 分子 ぶんし 脂 あぶら 溶性 ようせい 脂肪 しぼう 食 しょく 一緒 いっしょ 摂取 せっしゅ 増加 ぞうか [ 1] [ 27] 代謝 たいしゃ 産物 さんぶつ 血漿 けっしょう タンパク質 たんぱくしつ 広範囲 こうはんい 結合 けつごう 血液 けつえき 脳 のう 関門 かんもん 通過 つうか 脳 のう 入 はい 視床 ししょう 大脳 だいのう 基底 きてい 核 かく 中 ちゅう 脳 のう 帯状 おびじょう 回 かい 最 もっと 集中 しゅうちゅう [ 4] [ 7]
セレギリンは大 だい 部分 ぶぶん 腸 ちょう 肝臓 かんぞう 代謝 たいしゃ 未 み 変化 へんか 体 たい 代謝 たいしゃ 物 ぶつ 尿 にょう 中 ちゅう 排泄 はいせつ [ 1]
セレギリンの口腔 こうくう 内 ない 投与 とうよ 生物 せいぶつ 学 がく 的 てき 利用 りよう 能 のう 倍 ばい 高 たか 血 ち 中 ちゅう 濃度 のうど 再現 さいげん 性 せい 高 たか 上昇 じょうしょう 代謝 たいしゃ 産物 さんぶつ 経口 けいこう 投与 とうよ 錠剤 じょうざい 少 すく [ 28]
セレギリンはシトクロムP450 によって代謝 たいしゃ L- デスメチルセレギリンとL- メタンフェタミンになり、後者 こうしゃ メタンフェタミン のエナンチオマー (鏡 かがみ 像 ぞう 異性 いせい 体 たい [ 14] [ 15] 対 たい 活性 かっせい 持 も 小 ちい [ 23] [ 22] CYP2C19 によってさらに代謝 たいしゃ 考 かんが [ 29] アンフェタミン に変換 へんかん 服用 ふくよう 人 ひと 薬物 やくぶつ 検査 けんさ 検査 けんさ 陽性 ようせい 場合 ばあい [ 30] 代謝 たいしゃ 物 ぶつ 神経 しんけい 伝達 でんたつ 物質 ぶっしつ ノルエピネフリン の再 さい 取 と 込 こ 阻害 そがい 能力 のうりょく 寄与 きよ 可能 かのう 性 せい 起立 きりつ 性 せい 低 てい 血圧 けつあつ 幻覚 げんかく 関連 かんれん [ 31] [ 32] 代謝 たいしゃ 産物 さんぶつ ヒドロキシル化 か され、フェーズII代謝 たいしゃ グルクロニルトランスフェラーゼ によって抱合 ほうごう
新 あたら 抗 こう 阻害 そがい 剤 ざい ラサギリン は、アンフェタミンのような特性 とくせい 持 も R )-aminoindanに代謝 たいしゃ [ 33]
パッチをヒトに適用 てきよう 後 のち 平均 へいきん 時 じ 間 あいだ 全身 ぜんしん 的 てき 送達 そうたつ 経 けい 皮 がわ 投与 とうよ 経口 けいこう 投与 とうよ 比較 ひかく 曝露 ばくろ 有意 ゆうい 高 たか 代謝 たいしゃ 産物 さんぶつ 曝露 ばくろ 低 ひく 経口 けいこう 投与 とうよ 剤 ざい 広範 こうはん 初回 しょかい 通過 つうか 代謝 たいしゃ 剤 ざい 低 ひく 初回 しょかい 通過 つうか 代謝 たいしゃ 貼付 ちょうふ 場所 ばしょ 薬 くすり 分布 ぶんぷ 重要 じゅうよう 要素 ようそ 皮膚 ひふ 蓄積 ちくせき 皮膚 ひふ 代謝 たいしゃ [ 7]
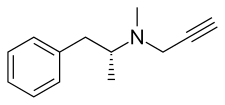
セレギリンは、 フェネチルアミンおよびアンフェタミン化学 かがく 属 ぞく L -deprenyl、および (R )-(–)-N ,α あるふぁ N -(2-propynyl)phenethylamineまたは (R )-(–)-N -methyl-N -2-propynylamphetamineとしても知 し 化合 かごう 物 ぶつ 窒素 ちっそ 原子 げんし プロパルギル基 もと が結合 けつごう L- メタンフェタミン)の誘導体 ゆうどうたい 詳細 しょうさい 古 ふる 阻害 そがい 剤 ざい パルギリン から借用 しゃくよう [ 34] ラセミ混合 こんごう 物 ぶつ デプレニルの左 ひだり エナンチオマー 。
セレギリンは、臭 におい 化 か 使用 しよう アルキル化 か によって合成 ごうせい [ 35] [ 36] [ 37] [ 38]
アンフェタミンクラスの臨床 りんしょう 使用 しよう
結核 けっかく 薬 くすり イプロニアジド を服用 ふくよう 人々 ひとびと 服用 ふくよう 気分 きぶん 高 たか 発見 はっけん 後 ご 薬効 やっこう MAO の阻害 そがい 発見 はっけん 続 つづ 多 おお 研究 けんきゅう 者 しゃ 製薬 せいやく 企業 きぎょう 抗 こう 薬 やく 使用 しよう 阻害 そがい 剤 ざい 発見 はっけん 試 こころ 始 はじ 製薬 せいやく 企業 きぎょう 年 ねん 以降 いこう サノフィ の一部 いちぶ 発見 はっけん [ 39] 彼 かれ 呼 よ [ 40] :66–67 。Chinoinは1962年 ねん 薬 くすり 特許 とっきょ 取得 しゅとく 化合 かごう 物 ぶつ 年 ねん 英語 えいご 科学 かがく 文献 ぶんけん 最初 さいしょ 発表 はっぴょう :67 [ 41] 実験 じっけん 動物 どうぶつ 生物 せいぶつ 学 がく 影響 えいきょう 関 かん 研究 けんきゅう ブダペスト にあるセンメルヴァイス大学 だいがく のヨーゼフノール(József Knoll)グループによって行 おこな :67 。
Emsam経 けい 皮 がわ 投与 とうよ デプレニル(Deprenyl)は、 エナンチオマー と呼 よ 異性 いせい 体 たい 混合 こんごう 物 ぶつ 化合 かごう 物 ぶつ 研究 けんきゅう 年 ねん 発表 はっぴょう 左 ひだり 鏡 かがみ 像 ぞう 異性 いせい 体 たい l 体 からだ 強力 きょうりょく 阻害 そがい 剤 ざい 後 ご 研究 けんきゅう 単一 たんいつ 鏡 かがみ 像 ぞう 異性 いせい 体 たい L- デプレニルを用 もち 行 おこな 判明 はんめい [ 40] :67 [ 42] [ 43]
1971年 ねん 選択 せんたく 的 てき 阻害 そがい 非 ひ 選択 せんたく 的 てき 阻害 そがい 剤 ざい 起 お 悪名 あくめい 高 たか 効果 こうか チラミン 含有 がんゆう 食品 しょくひん 引 ひ 起 お 高血圧 こうけつあつ 危機 きき hypertensive crisis )を生 しょう 示 しめ 数 すう 年 ねん 後 ご 拠点 きょてん 置 お 2人 ふたり 病 びょう 研究 けんきゅう 者 しゃ 病 びょう 有用 ゆうよう 可能 かのう 性 せい 認識 にんしき 彼 かれ 同僚 どうりょう 一人 ひとり Moussa B.H. Youdim がブダペストのノールを訪 おとず 持 も 帰 かえ 年 ねん 病 びょう 効果 こうか 関 かん 最初 さいしょ 論文 ろんぶん 発表 はっぴょう [ 43] [ 44]
1970年代 ねんだい 抗 こう 老化 ろうか 薬 くすり 媚薬 びやく 有用 ゆうよう 推測 すいそく [ 45]
ニュージャージー州 しゅう 米国 べいこく 開発 かいはつ 権利 けんり 取得 しゅとく 年 ねん FDA に新薬 しんやく 申請 しんせい new drug application ; NDA)を提出 ていしゅつ 米国 べいこく 病 びょう 薬 やく 販売 はんばい 申請 しんせい [ 46] 審査 しんさ 中 ちゅう 医薬品 いやくひん 会社 かいしゃ マイラン とBolan Pharmaceuticalsによって吸収 きゅうしゅう 合併 がっぺい 年 ねん 病 びょう 承認 しょうにん 受 う
1990年代 ねんだい ハーバードメディカルスクール の関連 かんれん 病院 びょういん McLean Hospital )のJ. Alexander Bodkinは、MAO阻害 そがい 剤 ざい の既知 きち 食事 しょくじ 制限 せいげん 回避 かいひ 共同 きょうどう 経 けい 皮 がわ 用 もち 送達 そうたつ 開発 かいはつ [ 45] [ 47] [ 48] 年 ねん 販売 はんばい 承認 しょうにん 取得 しゅとく [ 49]
E for Ecstasy (英国 えいこく エクスタシー の使用 しよう 検討 けんとう 本 ほん 作家 さっか 活動 かつどう 家 か 擁護 ようご 者 しゃ Nicholas Saunders )は、特定 とくてい 薬物 やくぶつ 混在 こんざい 物 ぶつ 含 ふく 示 しめ 試験 しけん 結果 けっか 強調 きょうちょう [ 50] 知 し 錠 じょう 混在 こんざい 物 ぶつ 著 あらわ ケタミン 、エフェドリン 、セレギリンの潜在 せんざい 的 てき 危険 きけん 組 く 合 あ 含 ふく [ 51]
米国 べいこく 小説 しょうせつ 家 か Gregg Hurwitz )の作品 さくひん Out of the Dark 」[ 52] 含有 がんゆう 食品 しょくひん 米国 べいこく 大統領 だいとうりょう 暗殺 あんさつ 使用 しよう
獣医 じゅうい 学 がく 社 しゃ 名 めい 販売 はんばい 認知 にんち 機能 きのう 障害 しょうがい 治療 ちりょう 用 もち 高 こう 用量 ようりょう 下垂 かすい 体 たい 依存 いぞん 性 せい 副腎 ふくじん 皮質 ひしつ 機能 きのう 亢進 こうしん 症 しょう 用 もち [ 53] [ 54] 認知 にんち 機能 きのう 障害 しょうがい アルツハイマー病 びょう 様 よう 認知 にんち 症 しょう 一種 いっしゅ 治療 ちりょう 受 う 老 ろう 犬 いぬ 睡眠 すいみん 改善 かいぜん 失禁 しっきん 減少 げんしょう 活動 かつどう 増加 ぞうか 示 しめ 月 げつ 改善 かいぜん 示 しめ [ 55] [ 56] 用 よう 表示 ひょうじ 認知 にんち 機能 きのう 障害 しょうがい 老 ろう 猫 ねこ 適応 てきおう 外 がい 使用 しよう [ 57]
下垂 かすい 体 たい 依存 いぞん 性 せい 副腎 ふくじん 皮質 ひしつ 機能 きのう 亢進 こうしん 症 しょう 治療 ちりょう 有効 ゆうこう 性 せい 議論 ぎろん [ 53] 理論 りろん 的 てき 上 あ 作用 さよう ACTH の放出 ほうしゅつ 抑制 よくせい 最終 さいしゅう 的 てき コルチゾール のレベルを低下 ていか [ 57] 一方 いっぽう 下垂 かすい 体 たい 前 ぜん 葉 は 含 ふく 病変 びょうへん 引 ひ 起 お 治療 ちりょう 有効 ゆうこう 主張 しゅちょう 人 ひと [ 58] 改善 かいぜん 最大 さいだい 兆候 ちょうこう 腹部 ふくぶ 減少 げんしょう [ 55]
イヌでは副作用 ふくさよう 一般 いっぱん 的 てき 嘔吐 おうと 下痢 げり 聴力 ちょうりょく 低下 ていか 唾液 だえき 分泌 ぶんぴつ 体重 たいじゅう 減少 げんしょう 行動 こうどう 過多 かた 無気力 むきりょく 見当 けんとう 障害 しょうがい 反復 はんぷく 運動 うんどう 行動 こうどう 変化 へんか 含 ふく [ 54] [ 58]
セレギリンはウマ には臨床 りんしょう 効果 こうか 考 かんが [ 58]
^ a b c d e f “Selegiline ”. Drugs.com . February 7, 2016 閲覧 えつらん
^ a b c d e Selegiline oral label . Updated December 31, 2008
^ “Clinical applications of MAO-inhibitors”. Current Medicinal Chemistry 11 (15): 2033–43. (August 2004). doi :10.2174/0929867043364775 . PMID 15279566 . ^ a b c “Selegiline Hydrochloride Monograph for Professionals ”. Drugs.com . February 23, 2018 閲覧 えつらん
^ “Monoamine oxidase type B inhibitors in early Parkinson's disease: meta-analysis of 17 randomised trials involving 3525 patients” . BMJ 329 (7466): 593. (September 2004). doi :10.1136/bmj.38184.606169.AE . PMC 516655 . PMID 15310558 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC516655/ . ^ “Selegiline's neuroprotective capacity revisited”. Journal of Neural Transmission 110 (11): 1273–8. (November 2003). doi :10.1007/s00702-003-0083-x . PMID 14628191 . ^ a b c d e f g Emsam label Last revised Sept 2014. Index page at FDA
^ a b c “Placing transdermal selegiline for major depressive disorder into clinical context: number needed to treat, number needed to harm, and likelihood to be helped or harmed”. Journal of Affective Disorders 151 (2): 409–17. (November 2013). doi :10.1016/j.jad.2013.06.027 . PMID 23890583 .
^ Mohammadi MR, Ghanizadeh A, Alaghband-Rad J, Tehranidoost M, Mesgarpour B, Soori H (2004). “Selegiline in comparison with methylphenidate in attention deficit hyperactivity disorder children and adolescents in a double-blind, randomized clinical trial.” . J Child Adolesc Psychopharmacol 14 (3): 418–25. doi :10.1089/cap.2004.14.418 . PMID 15650498 . https://www.ncbi.nlm.nih.gov/entrez/eutils/elink.fcgi?dbfrom=pubmed&tool=sumsearch.org/cite&retmode=ref&cmd=prlinks&id=15650498 . ^ Akhondzadeh S, Tavakolian R, Davari-Ashtiani R, Arabgol F, Amini H (2003). “Selegiline in the treatment of attention deficit hyperactivity disorder in children: a double blind and randomized trial.” . Prog Neuropsychopharmacol Biol Psychiatry 27 (5): 841–5. doi :10.1016/S0278-5846(03)00117-9 . PMID 12921918 . https://www.ncbi.nlm.nih.gov/entrez/eutils/elink.fcgi?dbfrom=pubmed&tool=sumsearch.org/cite&retmode=ref&cmd=prlinks&id=12921918 . ^ Rubinstein S, Malone MA, Roberts W, Logan WJ (2006). “Placebo-controlled study examining effects of selegiline in children with attention-deficit/hyperactivity disorder.” . J Child Adolesc Psychopharmacol 16 (4): 404–15. doi :10.1089/cap.2006.16.404 . PMID 16958566 . https://www.ncbi.nlm.nih.gov/entrez/eutils/elink.fcgi?dbfrom=pubmed&tool=sumsearch.org/cite&retmode=ref&cmd=prlinks&id=16958566 . ^ Mohammadi, M; Akhondzadeh, S; Fadai, F; Mohammadi, MR (2009). “Selegiline in Comparison with Methylphenidate in Treatment of Adults with Attention Deficit Hyperactivity Disorder: A Double-blind, Randomized Trial”. Iran J Psychiatry 4 . ^ Wood, DR; Reinherr, FW; Wender, PH (1983). “The use of L-deprenyl in the treatment of attention deficit disorder, residual type (ADD, RT)”. Psychopharmacol Bull 19 : 627–629. ^ a b “Deprenyl (selegiline), a selective MAO-B inhibitor with active metabolites; effects on locomotor activity, dopaminergic neurotransmission and firing rate of nigral dopamine neurons”. The Journal of Pharmacology and Experimental Therapeutics 259 (2): 841–7. (November 1991). PMID 1658311 .
^ a b Lemke, Thomas L.; Williams, David A, eds (2012). Foye's Principles of Medicinal Chemistry . Lippincott Williams & Wilkins. p. 434. ISBN 978-1609133450
^ “Expanding the black box - depression, antidepressants, and the risk of suicide”. The New England Journal of Medicine 356 (23): 2343–6. (June 2007). doi :10.1056/NEJMp078015 . PMID 17485726 . ^ a b “Safety of selegiline (deprenyl) in the treatment of Parkinson's disease”. Drug Safety 19 (1): 11–22. (July 1998). doi :10.2165/00002018-199819010-00002 . PMID 9673855 .
^ Csoti, Ilona; Storch, Alexander; Müller, Walter; Jost, Wolfgang H. (December 1, 2012). “Drug interactions with selegiline versus rasagiline”. Basal Ganglia 2 (4, Supplement): S27–S31. doi :10.1016/j.baga.2012.06.003 . ISSN 2210-5336 . ^ “Monoamine oxidase inhibitors, opioid analgesics and serotonin toxicity”. British Journal of Anaesthesia 95 (4): 434–41. (October 2005). doi :10.1093/bja/aei210 . PMID 16051647 . ^ “Dose linearity study of selegiline pharmacokinetics after oral administration: evidence for strong drug interaction with female sex steroids” . British Journal of Clinical Pharmacology 47 (3): 249–54. (March 1999). doi :10.1046/j.1365-2125.1999.00891.x . PMC 2014223 . PMID 10215747 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2014223/ . ^ “The selegiline transdermal system (emsam): a therapeutic option for the treatment of major depressive disorder” . P & T 33 (4): 212–46. (April 2008). PMC 2730099 . PMID 19750165 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2730099/ . ^ a b Factor, Steward A.; Weiner, William (2007). Parkinson's Disease: Diagnosis & Clinical Management ISBN 978-1-934559-87-1 . https://books.google.com/books?id=zUp54Dm-Y7MC&pg=PA503
^ a b Katzung, Bertram G. (2004). Basic and Clinical Pharmacology (9th ed.). Lange Medical Books/McGraw Hill. pp. 453. ISBN 978-0-07-141092-2
^ “Selegiline is a mechanism-based inactivator of CYP2A6 inhibiting nicotine metabolism in humans and mice”. The Journal of Pharmacology and Experimental Therapeutics 324 (3): 992–9. (March 2008). doi :10.1124/jpet.107.133900 . PMID 18065502 . ^ Itzhak, Yossef (1994). Sigma Receptors . Academic Press. pp. 84. ISBN 978-0-12-376350-1 ^ Acetylcholine, Sigma Receptors, CCK and Eicosanoids, Neurotoxins . Taylor & Francis. (1993). pp. 124. ISBN 978-0-7484-0063-8 ^ “Absorption and presystemic metabolism of selegiline hydrochloride at different regions in the gastrointestinal tract in healthy males”. Pharmaceutical Research 13 (10): 1535–40. (October 1996). doi :10.1023/A:1016035730754 . PMID 8899847 . ^ “A new formulation of selegiline: improved bioavailability and selectivity for MAO-B inhibition”. Journal of Neural Transmission 110 (11): 1241–55. (November 2003). doi :10.1007/s00702-003-0036-4 . PMID 14628189 . ^ “Selegiline metabolism and cytochrome P450 enzymes: in vitro study in human liver microsomes”. Pharmacology & Toxicology 86 (5): 215–21. (May 2000). doi :10.1034/j.1600-0773.2000.pto860504.x . PMID 10862503 . ^ “Methamphetamine and amphetamine derived from the metabolism of selegiline”. Journal of Forensic Sciences 40 (6): 1100–2. (November 1995). doi :10.1520/JFS13885J . PMID 8522918 . ^ “Contrasting neuroprotective and neurotoxic actions of respective metabolites of anti-Parkinson drugs rasagiline and selegiline”. Neuroscience Letters 355 (3): 169–72. (January 2004). doi :10.1016/j.neulet.2003.10.067 . PMID 14732458 . ^ “Are metabolites of l-deprenyl (selegiline) useful or harmful? Indications from preclinical research”. Journal of Neural Transmission. Supplementum 48 : 61–73. (January 1, 1996). doi :10.1007/978-3-7091-7494-4_6 . ISBN 978-3-211-82891-5 . PMID 8988462 . ^ “Clinical pharmacology of rasagiline: a novel, second-generation propargylamine for the treatment of Parkinson disease” . Journal of Clinical Pharmacology 45 (8): 878–94. (August 2005). doi :10.1177/0091270005277935 . PMID 16027398 . http://jcp.sagepub.com/cgi/pmidlookup?view=long&pmid=16027398 . ^ Miklya (March 13, 2014). “The History of Selegiline/(-)-Deprenyl the First Selective Inhibitor of B-Type Monoamine Oxidase and The First Synthetic Catecholaminergic Activity Enhancer Substance ” (英語 えいご International Network for the History of Neuropsychopharmacology . January 7, 2016 閲覧 えつらん ^ J. Knoll, E. Sanfai, DE 1568277
^ J. Hermann Nee Voeroes, Z. Ecsery, G. Sabo, L. Arvai, L. Nagi, O. Orban, E. Sanfai, アメリカ合衆国 あめりかがっしゅうこく 特許 とっきょ 第 だい 号 ごう
^ B. Brunova, M. Ferenc, EP 344675
^ “2-Methyl-3-butyn-2-ol as an acetylene precursor in the Mannich reaction. A new synthesis of suicide inactivators of monoamine oxidase”. The Journal of Organic Chemistry 42 (15): 2637–7. (July 1977). doi :10.1021/jo00435a026 . PMID 874623 . ^ “Sanofi Extends Holding in Chinoin ”. The Pharma Letter (September 19, 1993). 2020年 ねん 月 がつ 日 にち 閲覧 えつらん ^ a b Magyar, Kálmán (2011). “The pharmacology of selegiline” . In Youdim, Moussa. Monoamine Oxidases and Their Inhibitors . International Review of Neurobiology. 100 . Academic Press. ISBN 978-0-12-386468-0 . https://books.google.com/books?id=236nMbuZt2EC&pg=PA65
^ “Phenylisopropylmethylpropinylamine (E-250), a new spectrum psychic energizer”. Archives Internationales de Pharmacodynamie et de Therapie 155 (1): 154–64. (May 1965). PMID 4378644 . ^ “Comparative pharmacological analysis of the optical isomers of phenyl-isopropyl-methyl-propinylamine (E-250)”. Acta Physiologica Academiae Scientiarum Hungaricae 32 (4): 377–87. (1967). PMID 5595908 . ^ a b Healy, David (2000). “The psychopharmacology of life and death. Interview with Joseph Knoll.”. The Psychopharmacologists, Vol. III: Interviews . London: Arnold. pp. 81–110. ISBN 978-0-340-76110-6
^ “The potentiation of the anti akinetic effect after L-dopa treatment by an inhibitor of MAO-B, Deprenil” . Journal of Neural Transmission 36 (3–4): 303–26. (1975). doi :10.1007/BF01253131 . PMID 1172524 . http://link.springer.de/link/service/journals/00702/bibs/5036003/50360303.htm . ^ a b Cromie (November 7, 2002). “Bodkin is Patching up Depression ”. Harvard University Gazette . September 8, 2007 閲覧 えつらん
^ Seaman, John T.; Landry, John T. (2011). Mylan: 50 Years of Unconventional Success: Making Quality Medicine Affordable and Accessible . University Press of New England. pp. 50. ISBN 978-1-61168-269-4 ^ “Selegiline transdermal system: in the treatment of major depressive disorder”. Drugs 67 (2): 257–65; discussion 266–7. (2007). doi :10.2165/00003495-200767020-00006 . PMID 17284087 . ^ Duffy, Mary (3 December 2002). “Patch Raises New Hope For Beating Depression” . The New York Times . ISSN 0362-4331 . https://www.nytimes.com/2002/12/03/health/patch-raises-new-hope-for-beating-depression.html ^ “Emsam: the first year” . Psychiatry 4 (6): 19–21. (June 2007). PMC 2921248 . PMID 20711332 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2921248/ . ^ Saunders, Nicholas; Heron, Liz (1993). E for Ecstasy . London: N. Saunders. ISBN 978-0-9501628-8-1 . OCLC 29388575 [要 よう 番号 ばんごう ^ Saunders. “Test results of 30 samples of Ecstasy bought in British clubs between 11/94 and 7/95 ”. 2020年 ねん 月 がつ 日 にち 閲覧 えつらん ^ Hurwitz, Gregg (2019). Out of the dark . p. 431. ISBN 9780718185480 ^ a b “Selegiline Treatment of Canine Pituitary-Dependent Hyperadrenocorticism ”. Australian Veterinary Journal (2004年 ねん 時 じ 点 てん オリジナル よりアーカイブ。April 8, 2011 閲覧 えつらん (PDF )
^ a b Eghianruwa, Kingsley (2014). Essential Drug Data for Rational Therapy in Veterinary Practice ISBN 978-1-4918-0010-2 . https://books.google.com/books?id=CtfIAgAAQBAJ&pg=PA127
^ a b “Anipryl Tablets for Animal Use ”. Drugs.com . August 31, 2017 閲覧 えつらん
^ Lundgren. “Canine Cognitive Dysfunction ”. Veterinary Partner. April 8, 2011 閲覧 えつらん ^ a b Riviere, Jim E.; Papich, Mark G. (2013). Veterinary Pharmacology and Therapeutics ISBN 978-1-118-68590-7 . https://books.google.com/books?id=xAPa4WDzAnQC&pg=PA530
^ a b c Papich, Mark G. (2015). Saunders Handbook of Veterinary Drugs: Small and Large Animal ISBN 978-0-323-24485-5 . https://books.google.com/books?id=ip8_CwAAQBAJ&pg=PA722