出典: フリー百科事典『ウィキペディア(Wikipedia)』
| この 記事で 示されている 出典について、 該当する 記述が 具体的にその文献の何ページあるいはどの章節にあるのか、特定が求められています。 ご存知の方は加筆をお願いします。(2023年2月) |
| 硫酸アンモニウム鉄(II)
|

|
|

|
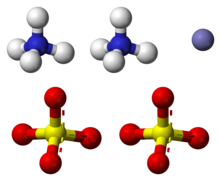
Ammonium iron(II) sulfate
硫酸アンモニウム鉄(II) |
別称 硫酸鉄(II)アンモニウム
硫酸第一鉄アンモニウム
モール塩 |
| 識別情報
|
| CAS登録番号
|
10045-89-3  , (無水物) , (無水物)
7783-85-9 (六水和物)
|
| PubChem
|
24863
|
| ChemSpider
|
23246 
|
| EC番号
|
233-151-8
|
[Fe+2].[O-]S(=O)(=O)[O-].[O-]S([O-])(=O)=O.[NH4+].[NH4+]
|
InChI=1S/Fe.2H3N.2H2O4S/c;;;2*1-5(2,3)4/h;2*1H3;2*(H2,1,2,3,4)/q+2;;;;/p-2  Key: IMBKASBLAKCLEM-UHFFFAOYSA-L  InChI=1/Fe.2H3N.2H2O4S/c;;;2*1-5(2,3)4/h;2*1H3;2*(H2,1,2,3,4)/q+2;;;;/p-2 Key: IMBKASBLAKCLEM-NUQVWONBAX
|
| 特性
|
| 化学式
|
(NH4)2Fe(SO4)2·6H2O
|
| モル質量
|
284.05 g mol−1 (無水物)
392.14 g mol−1 (六水和物)
|
| 危険性
|
| 安全データシート(外部リンク)
|
Fisher MSDS
|
| 主な危険性
|
刺激性 (Xi)
|
| Rフレーズ
|
R36/37/38
|
| Sフレーズ
|
S24/25
|
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。
|
硫酸アンモニウム鉄(II)(りゅうさんアンモニウムてつに、ammonium iron(II) sulfate)またはモール塩(モールえん、Mohr's Salt)は化学式 (NH4)2Fe(SO4)2·6H2O で表される無機化合物である。Fe2+ と NH4+ の2種類のカチオンを含み、硫酸鉄(II)と硫酸アンモニウムの複塩である。研究室において頻繁に用いられる試薬である。ほかの硫酸鉄塩と同じく、水に溶けてアクア錯体(英語版) [Fe(H2O)6]2+ をつくる。これは水分子が正八面体方向に鉄原子に配位した構造を持つ[1]。
他の硫酸鉄(II)の塩に比べて、硫酸アンモニウム鉄(II)は鉄(III)に酸化されにくいので、分析化学において滴定によく用いられる。溶液中での鉄(II)イオンの酸化のされやすさは pH に強く依存していて、pH が高いほど酸化されやすい。モール塩の水溶液においては、アンモニウムイオンが溶液をわずかに酸性にするので、酸化プロセスが起こりにくい[1]。
モール塩の名はドイツ人化学者であるカール・フリードリヒ・モールにちなんでいる。19世紀、彼は滴定に関する多くの重要な方法論を発展させた。
 ウィキメディア・コモンズには、モール塩に関するカテゴリがあります。
ウィキメディア・コモンズには、モール塩に関するカテゴリがあります。



![]() ウィキメディア・コモンズには、モール
ウィキメディア・コモンズには、モール