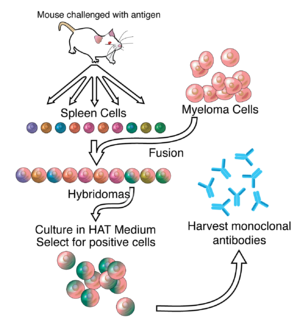
ハイブリドーマ技術 ぎじゅつ 抗体 こうたい 作成 さくせい 概要 がいよう 示 しめ 模 も 式 しき 図 ず [1] [2] 抗原 こうげん 誘発 ゆうはつ 脾臓 ひぞう 細胞 さいぼう 骨髄腫 こつづいしゅ 細胞 さいぼう 融合 ゆうごう 作成 さくせい 培地 ばいち 培養 ばいよう 優 すぐ 特性 とくせい 持 も 細胞 さいぼう 抗体 こうたい 採取 さいしゅ モノクローナル抗体 こうたい (モノクローナルこうたい、英 えい monoclonal antibody 、mAb またはmoAb )は、単一 たんいつ 抗体 こうたい 産 さん 生 せい 細胞 さいぼう クローニング して作 つく 抗体 こうたい 得 え 後続 こうぞく 抗体 こうたい 単一 たんいつ 親 しん 細胞 さいぼう
通常 つうじょう 抗体 こうたい ポリクローナル抗体 こうたい )は抗原 こうげん 免疫 めんえき 動物 どうぶつ 血清 けっせい 調製 ちょうせい 抗体 こうたい 分 ぶん 子種 こだね 混合 こんごう 物 ぶつ 抗体 こうたい 抗体 こうたい 分 ぶん 子種 こだね 均一 きんいつ 抗原 こうげん 複数 ふくすう エピトープ (抗原 こうげん 決定 けってい 基 もと 抗体 こうたい 認識 にんしき 抗原 こうげん 部分 ぶぶん 持 も 多 おお 抗体 こうたい 各々 おのおの 対 たい 抗体 こうたい 混合 こんごう 物 ぶつ 厳密 げんみつ 抗原 こうげん 特異 とくい 性 せい 互 たが 異 こと 抗体 こうたい 分子 ぶんし 含 ふく 対 たい 抗体 こうたい 用 もち 抗原 こうげん 単一 たんいつ 抗原 こうげん 特異 とくい 性 せい 単一 たんいつ 抗体 こうたい 治療 ちりょう 対象 たいしょう 増 ふ 二 に 重 じゅう 特異 とくい 性 せい 抗体 こうたい 設計 せっけい
通常 つうじょう 抗体 こうたい 産 さん 生 せい 細胞 さいぼう 骨髄腫 こつづいしゅ 細胞 さいぼう 細胞 さいぼう 融合 ゆうごう 自律 じりつ 増殖 ぞうしょく 能 のう 持 も 融合 ゆうごう 細胞 さいぼう ハイブリドーマ (hybridoma) を作成 さくせい 目的 もくてき 抗原 こうげん 特異 とくい 性 せい 融合 ゆうごう 細胞 さいぼう 選別 せんべつ 抗原 こうげん 細胞 さいぼう 抗原 こうげん 細胞 さいぼう 培養 ばいよう 分泌 ぶんぴつ 物 ぶつ 精製 せいせい 目的 もくてき 抗体 こうたい 作製 さくせい 事実 じじつ 上 じょう 適切 てきせつ 物質 ぶっしつ 特異 とくい 的 てき 結合 けつごう 抗体 こうたい 作製 さくせい 物質 ぶっしつ 検出 けんしゅつ 精製 せいせい 機能 きのう 生化学 せいかがく 分子生物学 ぶんしせいぶつがく 医学 いがく 分野 ぶんや 重要 じゅうよう
1900年代 ねんだい 免疫 めんえき 学者 がくしゃ パウル・エールリヒ は、病気 びょうき 原因 げんいん 生物 せいぶつ 選択 せんたく 的 てき 標的 ひょうてき 生物 せいぶつ 対 たい 毒素 どくそ 送達 そうたつ 化合 かごう 物 ぶつ 魔法 まほう 弾丸 だんがん Zauberkugel )のアイデアを提案 ていあん 抗体 こうたい 薬物 やくぶつ 複 ふく 合体 がったい 概念 がいねん 支持 しじ イリヤ・メチニコフ は、免疫 めんえき 学 がく 理論 りろん 的 てき 基礎 きそ 提供 ていきょう 年 ねん ノーベル生理学 せいりがく 医学 いがく 賞 しょう を受賞 じゅしょう
1970年代 ねんだい 単一 たんいつ 抗体 こうたい 産 さん 生 せい 球 だま B細胞 さいぼう の癌 がん 多発 たはつ 性 せい 骨髄腫 こつづいしゅ 形 かたち 知 し 異常 いじょう 抗体 こうたい パラプロテイン (英語 えいご 版 ばん 抗体 こうたい 構造 こうぞう 研究 けんきゅう 使用 しよう 特定 とくてい 抗原 こうげん 特異 とくい 的 てき 同一 どういつ 抗体 こうたい 作 つく [3] :324 。1973年 ねん Jerrold Schwaber は、ヒトとマウスのハイブリッド細胞 さいぼう 使用 しよう 抗体 こうたい 生産 せいさん 説明 せつめい [4] 研究 けんきゅう 由来 ゆらい ハイブリドーマ を使用 しよう 人々 ひとびと 間 あいだ 広 ひろ 引用 いんよう [5] 年 ねん ジョルジュ・ケーラー とセーサル・ミルスタイン は、骨髄腫 こつづいしゅ 細胞 さいぼう 株 かぶ 細胞 さいぼう 融合 ゆうごう 既知 きち 抗原 こうげん 特異 とくい 的 てき 不死 ふし 化 か 抗体 こうたい 産 さん 生 せい 作成 さくせい 成功 せいこう [6] 彼 かれ ニールス・カイ・イェルネ は、この発見 はっけん 年 ねん 生理学 せいりがく 医学 いがく 賞 しょう 受賞 じゅしょう [6]
1988年 ねん グレッグ・ウィンター と彼 かれ 抗体 こうたい ヒト化 か する技術 ぎじゅつ 開拓 かいたく [7] 多 おお 抗体 こうたい 一部 いちぶ 患者 かんじゃ 引 ひ 起 お 反応 はんのう 解消 かいしょう 年代 ねんだい 入 はい 抗体 こうたい 治療 ちりょう 用 もち 研究 けんきゅう 進展 しんてん 年 ねん 抑制 よくせい 性 せい 連鎖 れんさ 防 ふせ 抗体 こうたい 使用 しよう 負 まけ 免疫 めんえき 調節 ちょうせつ 阻害 そがい 癌 がん 治療 ちりょう 法 ほう 発見 はっけん ジェームズ・P・アリソン と本 ほん 生理学 せいりがく 医学 いがく 賞 しょう 受賞 じゅしょう [8]
モノクローナル抗体 こうたい 作 つく 細胞 さいぼう 培養 ばいよう 物 ぶつ 見 み 研究 けんきゅう 者 しゃ 実験 じっけん 室 しつ 培養 ばいよう 研究 けんきゅう 者 しゃ 中 なか 最 もっと 有望 ゆうぼう 選 えら 産物 さんぶつ 分析 ぶんせき モノクローナル抗体 こうたい 写真 しゃしん 示 しめ 無制限 むせいげん 増殖 ぞうしょく 検査 けんさ 技師 ぎし 研究 けんきゅう 用 よう 液体 えきたい ウェル に手 て 充填 じゅうてん 目的 もくてき 抗体 こうたい 産 さん 生 せい 大量 たいりょう 増殖 ぞうしょく 培養 ばいよう 液 えき 調整 ちょうせい 骨髄腫 こつづいしゅ 細胞 さいぼう リンパ球 だま を融合 ゆうごう 細胞 さいぼう ハイブリドーマ )を形成 けいせい 行 おこな 検査 けんさ 技師 ぎし 準備 じゅんび 溶液 ようえき 浸 ひた 技師 ぎし 研究 けんきゅう 者 しゃ 抗体 こうたい 作成 さくせい 示 しめ 細胞 さいぼう 乳癌 にゅうがん 標識 ひょうしき モノクローナル抗体 こうたい 作製 さくせい 背後 はいご 研究 けんきゅう 多 おお ハイブリドーマ の作製 さくせい 根 ね 作成 さくせい 目的 もくてき 抗原 こうげん 特異 とくい 的 てき 抗体 こうたい 産 さん 生 せい 抗原 こうげん 特異 とくい 的 てき 血漿 けっしょう 形質 けいしつ 芽 め 細胞 さいぼう 特定 とくてい 細胞 さいぼう 骨髄腫 こつづいしゅ 細胞 さいぼう 融合 ゆうごう 含 ふく [6] 細胞 さいぼう 使 つか ウサギ・ハイブリドーマ (英語 えいご 版 ばん 形成 けいせい 隣接 りんせつ 細胞 さいぼう 膜 まく 融合 ゆうごう ポリエチレングリコール [9] 用 もち 成功 せいこう 率 りつ 低 ひく 融合 ゆうごう 細胞 さいぼう 増殖 ぞうしょく 選択 せんたく 培地 ばいち 使用 しよう 可能 かのう 骨髄腫 こつづいしゅ 細胞 さいぼう 核酸 かくさん サルベージ合成 ごうせい に必要 ひつよう 酵素 こうそ ヒポキサンチン-グアニン-ホスホリボシルトランスフェラーゼ (HGPRT)を合成 ごうせい 能力 のうりょく 失 うしな 欠損 けっそん de novoプリン合成 ごうせい 経路 けいろ (英語 えいご 版 ばん 破壊 はかい 限 かぎ 細胞 さいぼう 問題 もんだい 細胞 さいぼう アミノプテリン (英語 えいご 版 ばん 葉酸 ようさん 類似 るいじ 物質 ぶっしつ ジヒドロ葉酸 ようさん 還元 かんげん 酵素 こうそ (DHFR)を阻害 そがい 細胞 さいぼう de novo 経路 けいろ 使用 しよう 核酸 かくさん 対 たい 完全 かんぜん 栄養 えいよう 要求 ようきゅう 性 せい 生 い 延 の 補給 ほきゅう 必要 ひつよう
選択 せんたく 培地 ばいち ヒポキサンチン 、アミノプテリン、チミジン を含 ふく HAT培地 ばいち (英語 えいご 版 ばん 呼 よ 培地 ばいち 融合 ゆうごう 細胞 さいぼう ハイブリドーマ )に選択 せんたく 的 てき 未 み 融合 ゆうごう 骨髄腫 こつづいしゅ 細胞 さいぼう 欠損 けっそん 複製 ふくせい 増殖 ぞうしょく 未 み 融合 ゆうごう 脾臓 ひぞう 細胞 さいぼう 寿命 じゅみょう 限 かぎ 無制限 むせいげん 増殖 ぞうしょく 呼 よ 融合 ゆうごう 細胞 さいぼう 培地 ばいち 中 ちゅう 無制限 むせいげん 増殖 ぞうしょく 理由 りゆう 脾臓 ひぞう 細胞 さいぼう 供給 きょうきゅう 骨髄腫 こつづいしゅ 細胞 さいぼう 不死 ふし 特性 とくせい 癌 がん 細胞 さいぼう 似 に 持 も
次 つぎ 細胞 さいぼう 混合 こんごう 物 ぶつ 希釈 きしゃく マイクロタイター ウェル上 じょう 単一 たんいつ 親 しん 細胞 さいぼう 増殖 ぞうしょく 後 ご 異 こと 分泌 ぶんぴつ 抗体 こうたい 抗原 こうげん 結合 けつごう 能力 のうりょく ELISA や抗原 こうげん マイクロアレイ アッセイなどの試験 しけん ドットブロット で評価 ひょうか 最 もっと 生産 せいさん 的 てき 安定 あんてい 将来 しょうらい 使用 しよう 選択 せんたく
このハイブリドーマは、適切 てきせつ 細胞 さいぼう 培養 ばいよう 培地 ばいち 無制限 むせいげん 増殖 ぞうしょく 注射 ちゅうしゃ 腸 ちょう 囲 かこ 腹膜 ふくまく 内 うち 腹水 ふくすい 呼 よ 抗体 こうたい 多 おお 含 ふく 液体 えきたい 分泌 ぶんぴつ 腫瘍 しゅよう 生成 せいせい
ハイブリドーマの増殖 ぞうしょく 促進 そくしん 器 うつわ 内 ない in vitro) での選択 せんたく 際 さい 培地 ばいち 濃縮 のうしゅく 繊維 せんい 細胞 さいぼう 層 そう 補助 ほじょ 媒体 ばいたい 使用 しよう 実施 じっし 調整 ちょうせい 培地 ばいち 使用 しよう 腹水 ふくすい 手法 しゅほう 動物 どうぶつ 苦痛 くつう 与 あた 通常 つうじょう 細胞 さいぼう 培養 ばいよう 製造 せいぞう 望 のぞ 代替 だいたい 技術 ぎじゅつ 存在 そんざい 場合 ばあい 腹水 ふくすい 非 ひ 倫理 りんり 的 てき 見 み [10]
抗体 こうたい 新規 しんき 開発 かいはつ 技術 ぎじゅつ [ 編集 へんしゅう ] 近年 きんねん ファージディスプレイ [11] 単一 たんいつ 細胞 さいぼう 培養 ばいよう [12] 細胞 さいぼう 集団 しゅうだん 単一 たんいつ 細胞 さいぼう 増幅 ぞうふく [13] [14] [15] [16] [17] 単一 たんいつ 形質 けいしつ 細胞 さいぼう 解析 かいせき 技術 ぎじゅつ 抗体 こうたい 技術 ぎじゅつ 開発 かいはつ [18] 従来 じゅうらい 技術 ぎじゅつ 異 こと 新 あたら 技術 ぎじゅつ 分子生物学 ぶんしせいぶつがく 的 てき 手法 しゅほう 用 もち 抗体 こうたい 遺伝子 いでんし 重 じゅう 鎖 くさり 軽 けい 鎖 くさり PCR で増幅 ぞうふく 組 くみ 換 か 技術 ぎじゅつ 細菌 さいきん 哺乳類 ほにゅうるい 系 けい 生産 せいさん 新 あたら 技術 ぎじゅつ 利点 りてん 一 ひと 他 た 実験 じっけん 室 しつ 一般 いっぱん 的 てき 実験 じっけん 動物 どうぶつ 複数 ふくすう 動物 どうぶつ 適用 てきよう
培養 ばいよう 培地 ばいち 腹水 ふくすい 液 えき 入手 にゅうしゅ 後 のち 目的 もくてき 抗体 こうたい 抽出 ちゅうしゅつ 必要 ひつよう 細胞 さいぼう 培養 ばいよう 液 えき 夾雑 きょうざつ 物 ぶつ 主 おも 成長 せいちょう 因子 いんし ホルモン 、トランスフェリン などの培地 ばいち 成分 せいぶん 構成 こうせい 一方 いっぽう 生体 せいたい 内 ない in vivo )サンプルには、宿主 しゅくしゅ 抗体 こうたい プロテアーゼ 、ヌクレアーゼ 、核酸 かくさん ウイルス が含 ふく 可能 かのう 性 せい 場合 ばあい サイトカイン のようなハイブリドーマによる他 た 分泌 ぶんぴつ 物 ぶつ 存在 そんざい 可能 かのう 性 せい 細菌 さいきん 汚染 おせん 結果 けっか 細菌 さいきん 分泌 ぶんぴつ 内 うち 毒素 どくそ 存在 そんざい 可能 かのう 性 せい 細胞 さいぼう 培養 ばいよう 必要 ひつよう 培地 ばいち 複雑 ふくざつ 混 こん 入物 いれもの 応 おう 一方 いっぽう 方法 ほうほう in vivo またはin vitro )が好 この 場合 ばあい
サンプルは、まず前 ぜん 処理 しょり 精製 せいせい 準備 じゅんび 最初 さいしょ 細胞 さいぼう 細胞 さいぼう 組織 そしき 片 へん 脂質 ししつ 凝固 ぎょうこ 物 ぶつ 通常 つうじょう 遠心 えんしん 分離 ぶんり 除去 じょきょ 後 ご ろ過 か する。これらの大 おお 粒子 りゅうし 後 ご 精製 せいせい 工程 こうてい 膜 まく (英語 えいご 版 ばん 呼 よ 現象 げんしょう 引 ひ 起 お 特 とく 分泌 ぶんぴつ 量 りょう 少 すく 細胞 さいぼう 株 かぶ 目的 もくてき 抗体 こうたい 作 つく 場合 ばあい 中 ちゅう 生成 せいせい 物 ぶつ 濃度 のうど 十分 じゅうぶん 可能 かのう 性 せい 限外 げんがい 濾過 ろか 透析 とうせき 濃縮 のうしゅく
帯電 たいでん 不純物 ふじゅんぶつ 多 おお 核酸 かくさん 陰 かげ イオン交換 こうかん によって分離 ぶんり [19] 目的 もくてき 抗体 こうたい 結合 けつごう 陰 かげ 流 なが 低 ひく 陽 ひ 交換 こうかん 使用 しよう 目的 もくてき 抗体 こうたい 結合 けつごう 流 なが 高 たか 陰 かげ 交換 こうかん (英語 えいご 版 ばん 使用 しよう タンパク質 たんぱくしつ 等 ひとし 電 でん 点 てん 基 もと 陰 かげ 分離 ぶんり タンパク質 たんぱくしつ 等 ひとし 電 でん 点 てん タンパク質 たんぱくしつ 正味 しょうみ 電荷 でんか 持 も 定義 ていぎ 場合 ばあい タンパク質 たんぱくしつ 正味 しょうみ 負 ふ 電荷 でんか 持 も 場合 ばあい タンパク質 たんぱくしつ 正味 しょうみ 正 せい 電荷 でんか 持 も アルブミン のpIは4.8であり、ほとんどのモノクローナル抗体 こうたい 比 くら 著 いちじる 低 ひく 間 あいだ 分子 ぶんし 平均 へいきん 電荷 でんか 負 まけ 可能 かのう 性 せい 高 たか 分子 ぶんし 正 まさ 帯電 たいでん 両者 りょうしゃ 分離 ぶんり 一方 いっぽう 方法 ほうほう 簡単 かんたん 分離 ぶんり 良好 りょうこう 分離 ぶんり 少 すく 差 さ 必要 ひつよう
その代 か サイズ排除 はいじょ によって除去 じょきょ 方法 ほうほう 信頼 しんらい 性 せい 高 たか 技術 ぎじゅつ 一 ひと タンパク質 たんぱくしつ 扱 あつか 電荷 でんか 親和 しんわ 性 せい 特性 とくせい 一貫 いっかん 分子 ぶんし 化 か 脱 だつ 化 か 変化 へんか 比較的 ひかくてき 一定 いってい 保 たも 低 てい 分解能 ぶんかいのう 低 てい 容量 ようりょう 低 ひく 溶出 ようしゅつ 時間 じかん 欠点 けってん
はるかに迅速 じんそく 単一 たんいつ 分離 ぶんり 方法 ほうほう プロテインA/G (英語 えいご 版 ばん アフィニティークロマトグラフィー がある。この抗体 こうたい 選択 せんたく 的 てき 結合 けつごう 高 こう 純度 じゅんど 通常 つうじょう 以上 いじょう 得 え 方法 ほうほう 一般 いっぱん 的 てき 過酷 かこく 条件 じょうけん 行 おこな 損傷 そんしょう 受 う 抗体 こうたい 問題 もんだい 可能 かのう 性 せい 低 ひく 結合 けつごう 切断 せつだん 抗体 こうたい 外 はず 製品 せいひん 影響 えいきょう 与 あた 可能 かのう 性 せい 加 くわ 低 ひく 自体 じたい 漏 も 出 だ 溶出 ようしゅつ 混入 こんにゅう 可能 かのう 性 せい 敏感 びんかん 抗体 こうたい 低 てい 防 ふせ 高塩 たかしお 濃度 のうど 採用 さいよう 穏 おだ 溶出 ようしゅつ 利用 りよう 固定 こてい 化 か 高価 こうか 樹脂 じゅし 方法 ほうほう 重要 じゅうよう 考慮 こうりょ 事項 じこう
単一 たんいつ 工程 こうてい 最大 さいだい 純度 じゅんど 達成 たっせい 抗体 こうたい 特異 とくい 性 せい 持 も 抗原 こうげん 使用 しよう 精製 せいせい 行 おこな 方法 ほうほう 抗体 こうたい 生成 せいせい 用 もち 抗原 こうげん アガロース 担体に共有 きょうゆう 結合 けつごう 抗原 こうげん ペプチド の場合 ばあい 一般 いっぱん 的 てき 末端 まったん システイン を持 も 合成 ごうせい 開発 かいはつ 時 じ KLH (英語 えいご 版 ばん タンパク質 たんぱくしつ 選択 せんたく 的 てき 結合 けつごう 精製 せいせい 保持 ほじ 後 ご 抗体 こうたい 含有 がんゆう 培地 ばいち 固定 こてい 化 か 抗原 こうげん 抗体 こうたい 式 しき 通過 つうか 選択 せんたく 的 てき 結合 けつごう 不純物 ふじゅんぶつ 洗 あら 流 なが 間 あいだ 保持 ほじ 後 ご 低 てい 穏 おだ 高塩 たかしお 濃度 のうど 溶出 ようしゅつ 溶出 ようしゅつ 精製 せいせい 抗体 こうたい 回収 かいしゅう
モノクローナル抗体 こうたい 他 た 組 くみ 換 か 生物 せいぶつ 学 がく 的 てき 製品 せいひん 製品 せいひん 不 ふ 均一 きんいつ 性 せい 普通 ふつう 見 み 一般 いっぱん 的 てき 発現 はつげん 時 じ 上流 じょうりゅう 側 がわ 製造 せいぞう 時 じ 下流 かりゅう 側 がわ [要 よう 出典 しゅってん 。
これらの変異 へんい 体 たい 典型 てんけい 的 てき 凝集 ぎょうしゅう 体 たい 脱 だつ 化 か 生成 せいせい 物 ぶつ グリコシル化 か 変異 へんい 体 たい アミノ酸 あみのさん 側 がわ 鎖 くさり 酸化 さんか 物 ぶつ 末 まつ 端 はし アミノ酸 あみのさん 付加 ふか 物 ぶつ [20] 微小 びしょう 構造 こうぞう 変化 へんか 前 ぜん 臨床 りんしょう 試験 しけん 安定 あんてい 性 せい 最適 さいてき 化 か 治療 ちりょう 薬 やく 効力 こうりょく バイオアベイラビリティ 、および免疫 めんえき 原 ばら 性 せい 影響 えいきょう 及 およ 可能 かのう 性 せい 抗体 こうたい 流 りゅう 一般 いっぱん 的 てき 受 う 入 い 精製 せいせい 方法 ほうほう プロテインA (英語 えいご 版 ばん 製品 せいひん 捕捉 ほそく 溶出 ようしゅつ 潜在 せんざい 的 てき 哺乳 ほにゅう 動物 どうぶつ 不 ふ 活性 かっせい 化 か 酸性 さんせい 化 か 続 つづ イオンクロマトグラフィー (最初 さいしょ 陰 かげ (英語 えいご 版 ばん 次 つぎ 陽 ひ 含 ふく [要 よう 出典 しゅってん 。
置換 ちかん (英語 えいご 版 ばん 見 み 変異 へんい 体 たい 動物 どうぶつ 薬物 やくぶつ 動態 どうたい 試験 しけん 前 ぜん 臨床 りんしょう 評価 ひょうか 適 てき 量 りょう 同定 どうてい 特性 とくせい 明 あき 使用 しよう [21] [22] 前 ぜん 臨床 りんしょう 開発 かいはつ 段階 だんかい 得 え 知識 ちしき 製品 せいひん 品質 ひんしつ 対 たい 理解 りかい 深 ふか 重要 じゅうよう 管理 かんり 規制 きせい 柔軟 じゅうなん 性 せい 高 たか 基礎 きそ 最近 さいきん 米国 べいこく 食品 しょくひん 医薬品 いやくひん 局 きょく クオリティ・バイ・デザイン イニシアチブは、開発 かいはつ 関 かん 提供 ていきょう 製品 せいひん 製造 せいぞう 可能 かのう 性 せい 高 たか 有効 ゆうこう 性 せい 安全 あんぜん 性 せい 最大 さいだい 化 か 製品 せいひん 設計 せっけい 促進 そくしん [23]
組 くみ 換 か (英語 えいご 版 ばん 抗体 こうたい 作製 さくせい クローニング 、CRISPR/Cas9 、またはファージディスプレイ /酵母 こうぼ 技術 ぎじゅつ 用 もち [24] 組 くみ 換 か 抗体 こうたい (英語 えいご 版 ばん 工学 こうがく ウイルス や酵母 こうぼ 使用 しよう 抗体 こうたい 作製 さくせい 技術 ぎじゅつ 免疫 めんえき 遺伝子 いでんし 迅速 じんそく 基 もと アミノ酸 あみのさん 配列 はいれつ 異 こと 抗体 こうたい 作成 さくせい 目的 もくてき 特異 とくい 性 せい 持 も 抗体 こうたい 選択 せんたく [25] 抗体 こうたい 抗原 こうげん 別 べつ 形 がた [26] 技術 ぎじゅつ 抗体 こうたい 抗原 こうげん 認識 にんしき 特異 とくい 性 せい 環境 かんきょう 条件 じょうけん 安定 あんてい 性 せい 治療 ちりょう 効果 こうか 診断 しんだん 用途 ようと 検出 けんしゅつ 性 せい 高 たか 使用 しよう [27] 発酵 はっこう 槽 そう 大 だい 規模 きぼ 抗体 こうたい 生産 せいさん 使用 しよう
マウスとヒトの抗体 こうたい 構造 こうぞう 的 てき 類似 るいじ マウス モノクローナル抗体 こうたい 注射 ちゅうしゃ 違 ちが 免疫 めんえき 応答 おうとう 引 ひ 起 お 十分 じゅうぶん 結果 けっか 抗体 こうたい 血液 けつえき 中 ちゅう 速 すみ 除去 じょきょ 全身 ぜんしん 性 せい 炎症 えんしょう 作用 さよう ヒト抗 こう 抗体 こうたい (英語 えいご 版 ばん 産 さん 生 せい
組 くみ 換 か 滞留 たいりゅう 時間 じかん 長 なが 年代 ねんだい 後半 こうはん 探究 たんきゅう 研究 けんきゅう 抗体 こうたい 結合 けつごう 部分 ぶぶん 生 なま 細胞 さいぼう 中 なか 抗体 こうたい 産 さん 生 せい 融合 ゆうごう キメラ 」または「ヒト化 か 細胞 さいぼう 培養 ばいよう 発現 はつげん 一部 いちぶ 一部 いちぶ 抗体 こうたい 産 さん 生 せい [28] [29]
ヒトのモノクローナル抗体 こうたい 単 たん 離 はなれ 開発 かいはつ [18] モノクローナル抗体 こうたい 作製 さくせい 発見 はっけん 以来 いらい 科学 かがく 者 しゃ ヒト化 か 抗体 こうたい またはキメラ抗体 こうたい 副作用 ふくさよう 軽減 けいげん 完全 かんぜん 製品 せいひん 作製 さくせい 目標 もくひょう 成功 せいこう トランスジェニックマウス (英語 えいご 版 ばん [30] ファージディスプレイ [11] 単一 たんいつ 細胞 さいぼう 確認 かくにん [18]
2016年 ねん 月 がつ 現在 げんざい 市販 しはん 完全 かんぜん 抗体 こうたい 治療 ちりょう 薬 やく 種 しゅ 種 しゅ トランスジェニック マウス技術 ぎじゅつ 由来 ゆらい
トランスジェニック技術 ぎじゅつ 採用 さいよう 市場 いちば 出 だ 組織 そしき 次 つぎ
ファージディスプレイ は、繊維状 せんいじょう 外皮 がいひ タンパク質 たんぱくしつ 上 じょう 可変 かへん 抗体 こうたい 発現 はつげん 使用 しよう 可能 かのう [39] [40] [41] 抗体 こうたい 研究 けんきゅう 用途 ようと 使用 しよう [42] [43] 年 ねん 発表 はっぴょう [44] 罹患 りかん 組織 そしき 非 ひ 罹患 りかん 組織 そしき 対 たい 抗体 こうたい 行 おこな 酵素 こうそ 反応 はんのう 利用 りよう 特定 とくてい タンパク質 たんぱくしつ 近接 きんせつ 分子 ぶんし 標識 ひょうしき [45] [46]
モノクローナル抗体 こうたい 癌 がん 心 こころ 血管 けっかん 疾患 しっかん 炎症 えんしょう 性 せい 疾患 しっかん 黄 き 斑 むら 変性 へんせい 症 しょう 移植 いしょく 拒絶 きょぜつ 反応 はんのう 多発 たはつ 性 せい 硬化 こうか 症 しょう 感染 かんせん 症 しょう 治療 ちりょう 承認 しょうにん
2006年 ねん 月 がつ 米国 べいこく 研究 けんきゅう 製薬 せいやく 工業 こうぎょう 協会 きょうかい (英語 えいご 版 ばん 報告 ほうこく 米国 べいこく 企業 きぎょう 種類 しゅるい 抗体 こうたい 臨床 りんしょう 試験 しけん 中 ちゅう 米国 べいこく 食品 しょくひん 医薬品 いやくひん 局 きょく 承認 しょうにん 待 ま [47]
モノクローナル抗体 こうたい 製造 せいぞう 複雑 ふくざつ 関与 かんよ 全般 ぜんぱん 的 てき 分子 ぶんし 低 てい 分子 ぶんし 化合 かごう 物 ぶつ 高 たか 新 あたら 化学 かがく 物質 ぶっしつ 患者 かんじゃ 提供 ていきょう 膨大 ぼうだい 研究 けんきゅう 開発 かいはつ 費 ひ 追加 ついか 製造 せいぞう 業者 ぎょうしゃ 多額 たがく 投資 とうし 費用 ひよう 回収 かいしゅう 価格 かかく 設定 せってい 米国 べいこく 価格 かかく 統制 とうせい 場合 ばあい 価値 かち 高 たか 価格 かかく 高 たか ピッツバーグ大学 だいがく の7人 にん 研究 けんきゅう 者 しゃ 患者 かんじゃ 一 いち 人 にん 当 あ 療法 りょうほう 年間 ねんかん 費用 ひよう 腫瘍 しゅよう 学 がく 血液 けつえき 学 がく 領域 りょういき 他 た 疾病 しっぺい 約 やく 万 まん 高 たか 結論 けつろん 新 しん 血管 けっかん 疾患 しっかん 代謝 たいしゃ 性 せい 疾患 しっかん 免疫 めんえき 領域 りょういき 感染 かんせん 症 しょう 眼科 がんか 各 かく 領域 りょういき 比較 ひかく [48]
ある物質 ぶっしつ 対 たい 抗体 こうたい 使 つか 物質 ぶっしつ 存在 そんざい 検出 けんしゅつ タンパク質 たんぱくしつ ウェスタンブロット やイムノドットブロット を使用 しよう 検出 けんしゅつ 免疫 めんえき 組織 そしき 化学 かがく 検査 けんさ 抗体 こうたい 使用 しよう 固定 こてい 組織 そしき 切片 せっぺん 中 ちゅう 抗原 こうげん 検出 けんしゅつ 同様 どうよう 免疫 めんえき 蛍光 けいこう 検査 けんさ 凍結 とうけつ 組織 そしき 切片 せっぺん 生 なま 細胞 さいぼう 中 ちゅう 物質 ぶっしつ 検出 けんしゅつ
抗体 こうたい 免疫 めんえき 沈降 ちんこう 法 ほう 使用 しよう 混合 こんごう 物 ぶつ 標的 ひょうてき 化合 かごう 物 ぶつ 精製 せいせい 使用 しよう
治療 ちりょう 用 よう 抗体 こうたい 標的 ひょうてき 分子 ぶんし 機能 きのう 遮断 しゃだん 標的 ひょうてき 分子 ぶんし 発現 はつげん 細胞 さいぼう アポトーシス 誘導 ゆうどう 伝達 でんたつ 経路 けいろ 調節 ちょうせつ 複数 ふくすう 機構 きこう 通 つう 作用 さよう [49] [50]
抗体 こうたい 臨床 りんしょう 適用 てきよう [ 編集 へんしゅう ] 1970年代 ねんだい 発明 はつめい 抗体 こうたい 臨床 りんしょう 革命 かくめい 的 てき 変化 へんか 起 お 後 ご 年間 ねんかん 臨床 りんしょう 試験 しけん 上手 うま 主 おも マウス の抗体 こうたい ヒト に抗原 こうげん 認識 にんしき 原因 げんいん 年代 ねんだい CHO細胞 さいぼう 内 うち 免疫 めんえき 遺伝子 いでんし 発現 はつげん プラスミド を直接 ちょくせつ 形質 けいしつ 転換 てんかん 方法 ほうほう 開発 かいはつ 以降 いこう 問題 もんだい 克服 こくふく 方法 ほうほう 進化 しんか 現在 げんざい 使用 しよう 兆 ちょう 個 こ 分子 ぶんし 莫大 ばくだい 最適 さいてき 抗体 こうたい 遺伝子 いでんし 細胞 さいぼう 大量 たいりょう 生産 せいさん 方法 ほうほう 用 もち 抗体 こうたい 生産 せいさん トランスジェニックマウス を使 つか 直接 ちょくせつ 抗体 こうたい 得 え 方法 ほうほう 用 もち 方法 ほうほう 前 ぜん 臨床 りんしょう 段階 だんかい 開発 かいはつ 費 ひ 約 やく 億 おく 円 えん 済 す 従来 じゅうらい 古典 こてん 的 てき 化学 かがく 薬品 やくひん 億 おく 円 えん 比較 ひかく 非常 ひじょう 効率 こうりつ 細胞 さいぼう 培養 ばいよう 必要 ひつよう 最終 さいしゅう 製品 せいひん 製造 せいぞう 費用 ひよう 化学 かがく 合成 ごうせい 化学 かがく 薬品 やくひん 比 くら 非常 ひじょう 高 たか
モノクローナル抗体 こうたい タンパク質 たんぱくしつ 薬品 やくひん 化学 かがく 薬品 やくひん 違 ちが 経口 けいこう 投与 とうよ 普通 ふつう 週 しゅう 一 いち 回 かい 注射 ちゅうしゃ 製造 せいぞう 費用 ひよう 非常 ひじょう 高 たか 細胞 さいぼう 内部 ないぶ 侵入 しんにゅう 欠点 けってん 持 も 標的 ひょうてき 分子 ぶんし 結合 けつごう 患者 かんじゃ 自身 じしん 免疫 めんえき 機構 きこう 働 はたら 標的 ひょうてき 分子 ぶんし 含 ふく がん細胞 さいぼう を高率 こうりつ 破壊 はかい 利点 りてん 免疫 めんえき 自体 じたい 体内 たいない 存在 そんざい 分子 ぶんし 自身 じしん 副作用 ふくさよう 予想 よそう
原理 げんり 的 てき 抗体 こうたい 臨床 りんしょう 使用 しよう 可能 かのう 人間 にんげん 患者 かんじゃ 薬品 やくひん 使用 しよう 薬品 やくひん 内 ない 分子 ぶんし 化学 かがく 的 てき 厳密 げんみつ 定義 ていぎ 極 きわ 高 こう 純度 じゅんど 安定 あんてい 的 てき 大量 たいりょう 生産 せいさん 必要 ひつよう 現実 げんじつ 不可能 ふかのう 血漿 けっしょう 由来 ゆらい 血液 けつえき 製剤 せいざい 免疫 めんえき 製剤 せいざい 一種 いっしゅ 抗体 こうたい 様々 さまざま 難病 なんびょう 対 たい 使用 しよう 有効 ゆうこう 性 せい 示 しめ 血液 けつえき 由来 ゆらい 免疫 めんえき 製剤 せいざい 組 くみ 換 か 抗体 こうたい 医薬品 いやくひん 容易 ようい 置 お 換 か 上記 じょうき 品質 ひんしつ 管理 かんり 困難 こんなん
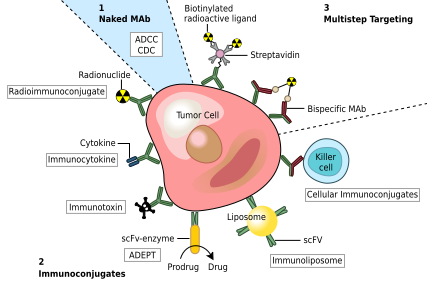
癌 がん 治療 ちりょう 法 ほう 一 ひと 癌 がん 細胞 さいぼう 特異 とくい 的 てき 抗原 こうげん 結合 けつごう 標的 ひょうてき 癌 がん 細胞 さいぼう 対 たい 免疫 めんえき 応答 おうとう 誘発 ゆうはつ 抗体 こうたい 考 かんが 抗体 こうたい 毒素 どくそ 放射 ほうしゃ 性 せい 同位 どうい 体 たい サイトカイン 、その他 た 活性 かっせい 送達 そうたつ 用 よう 修飾 しゅうしょく Fab領域 りょういき (英語 えいご 版 ばん 標的 ひょうてき 抗原 こうげん 細胞 さいぼう 両方 りょうほう 結合 けつごう 二 に 重 じゅう 特異 とくい 性 せい 抗体 こうたい 設計 せっけい 抗体 こうたい Fc領域 りょういき で細胞 さいぼう 受容 じゅよう 体 たい 他 た タンパク質 たんぱくしつ 結合 けつごう
癌 がん 対 たい 抗体 こうたい ADEPT (英語 えいご 版 ばん 抗体 こうたい 指向 しこう 性 せい 酵素 こうそ 療法 りょうほう ADCC :抗体 こうたい 依存 いぞん 性 せい 細胞 さいぼう 傷害 しょうがい CDC :補 ほ 体 たい 依存 いぞん 性 せい 細胞 さいぼう 傷害 しょうがい 抗体 こうたい scFv :単 たん 鎖 くさり 可変 かへん [51] 米国 べいこく 食品 しょくひん 医薬品 いやくひん 局 きょく 癌 がん 対 たい 承認 しょうにん 抗体 こうたい 次 つぎ [52]
自己 じこ 免疫 めんえき 疾患 しっかん 用 もち 抗体 こうたい インフリキシマブ やアダリムマブ があり、TNF-α あるふぁ に結合 けつごう 阻害 そがい 関節 かんせつ クローン病 びょう 、潰瘍 かいよう 性 せい 大腸 だいちょう 炎 えん 強直 きょうちょく 性 せい 脊椎 せきつい 炎 えん 効果 こうか [53] バシリキシマブ とダクリズマブ (英語 えいご 版 ばん 活性 かっせい 化 か T細胞 さいぼう のIL-2 を阻害 そがい 腎 じん 移植 いしょく 急性 きゅうせい 拒絶 きょぜつ 反応 はんのう 予防 よぼう 役立 やくだ [53] オマリズマブ は、ヒト免疫 めんえき 阻害 そがい 中等 ちゅうとう 症 しょう 重症 じゅうしょう アレルギ あれるぎ 性 せい 喘息 ぜんそく 治療 ちりょう 有用 ゆうよう
治療 ちりょう 用 よう 抗体 こうたい 例 れい [ 編集 へんしゅう ] 研究 けんきゅう 用 よう 抗体 こうたい 抗体 こうたい 直接 ちょくせつ CiteAb (英語 えいご 版 ばん 専門 せんもん 家 か 検索 けんさく 使用 しよう 入手 にゅうしゅ 次 つぎ 臨床 りんしょう 的 てき 重要 じゅうよう 抗体 こうたい 例 れい
モノクローナル抗体 こうたい 使用 しよう イムノクロマト法 ほう で各種 かくしゅ 迅速 じんそく 診断 しんだん 販売 はんばい 分 ふん 分 ふん 診断 しんだん 感染 かんせん 症 しょう インフルエンザウイルス 、RSウイルス 、A群 ぐん β べーた 溶連菌 ようれんきん 、アデノウイルス 、肺炎 はいえん ヒトメタニュウモウイルス 、ノロウイルス 、ロタウイルス 、肺炎 はいえん 球菌 きゅうきん レジオネラ 、病原 びょうげん 性 せい 大腸菌 だいちょうきん 便 びん 中 ちゅう 菌 きん
心筋 しんきん 炎 えん 心筋梗塞 しんきんこうそく トロポニン Tの迅速 じんそく 診断 しんだん
ベバシズマブ やセツキシマブ などのいくつかのモノクローナル抗体 こうたい 種類 しゅるい 副作用 ふくさよう 引 ひ 起 お 可能 かのう 性 せい [57] 副作用 ふくさよう 一般 いっぱん 的 てき 副作用 ふくさよう 重 じゅう 篤 あつし 副作用 ふくさよう 分類 ぶんるい [58]
一般 いっぱん 的 てき 副作用 ふくさよう 次 つぎ
めまい
頭痛 ずつう アレルギー
下痢 げり 咳 せき 発熱 はつねつ かゆみ
背中 せなか 痛 いた 全身 ぜんしん 脱力 だつりょく 感 かん 食欲 しょくよく 不振 ふしん 不眠症 ふみんしょう 便秘 べんぴ [59]
重大 じゅうだい 副作用 ふくさよう 可能 かのう 性 せい 次 つぎ
米 べい 産業 さんぎょう 役割 やくわり [ 編集 へんしゅう ] モノクローナル抗体 こうたい 年代 ねんだい 後半 こうはん バイオテクノロジー 産業 さんぎょう 革命 かくめい 現在 げんざい 薬品 やくひん 分 ぶん 抗体 こうたい 年 ねん 社 しゃ Rituxan 抗体 こうたい 抗 こう 抗体 こうたい 非 ひ 腫 しゅ 対 たい 認可 にんか Herceptin , Avastin などのシグナルトランスダクションやアンジオジェネシスを標的 ひょうてき 新型 しんがた 現在 げんざい 以上 いじょう 抗体 こうたい 治療 ちりょう 使 つか 少 すく 超 こ 抗体 こうたい 臨床 りんしょう 試験 しけん 開発 かいはつ 特 とく 治療 ちりょう 使 つか 年 ねん 売 う 上 あ 約 やく 億 おく 年 ねん 抗体 こうたい 売 う 上 あ 億 おく 超 こ 予想 よそう 次世代 じせだい 抗体 こうたい 呼 よ 放射 ほうしゃ 性 せい 同位 どうい 体 たい 結合 けつごう 抗体 こうたい 可変 かへん 部位 ぶい 極小 きょくしょう 型 がた 新型 しんがた 開発 かいはつ
成功 せいこう 抗体 こうたい 売 う 上 あ 莫大 ばくだい 年 ねん 抗 こう TNF-α あるふぁ 抗体 こうたい Remicade (Centocor社 しゃ 億 おく 億 おく 製品 せいひん 特 とく 社 しゃ 開発 かいはつ 抗体 こうたい 製品 せいひん 全 すべ 認可 にんか 全 すべ 製品 せいひん 一般 いっぱん 年 ねん 及 およ 臨床 りんしょう 試験 しけん 製品 せいひん 生 い 残 のこ 確 かく 率 りつ 考 かんが 米 べい 製薬 せいやく 業界 ぎょうかい 史上 しじょう 稀 まれ 成功 せいこう
モノクローナル抗体 こうたい 最 もっと 成功 せいこう 要因 よういん 抗体 こうたい 生体 せいたい 防御 ぼうぎょ タンパク質 たんぱくしつ 進化 しんか 分子 ぶんし 他 た タンパク質 たんぱくしつ 比 くら 極 きわ 安定 あんてい 性 せい 高 たか 半減 はんげん 期 き 長 なが 標的 ひょうてき 結合 けつごう 後 のち 身体 しんたい 免疫 めんえき 機構 きこう 利用 りよう 増幅 ぞうふく 効果 こうか 期待 きたい 同 おな 年代 ねんだい 開発 かいはつ 中 ちゅう 薬品 やくひん 標的 ひょうてき 細胞 さいぼう 内 ない 核 かく 内 ない 輸送 ゆそう 自体 じたい 至難 しなん 業 わざ 社 しゃ 社 しゃ 莫大 ばくだい 開発 かいはつ 費 ひ 投 とう 製品 せいひん 全 すべ 失敗 しっぱい 終 お
日本 にっぽん 上市 かみいち 医薬品 いやくひん [ 編集 へんしゅう ]
モノクローナル抗体 こうたい 薬 やく 名称 めいしょう 語尾 ごび
^ “Cytochrome P450 Mediated Drug and Carcinogen Metabolism using Monoclonal Antibodies ”. home.ccr.cancer.gov . 2019年 ねん 月 がつ 20日 はつか 時点 じてん オリジナル よりアーカイブ。2021年 ねん 月 がつ 日 にち 閲覧 えつらん ^ Gelboin HV, Krausz KW, Gonzalez FJ, Yang TJ (November 1999). “Inhibitory monoclonal antibodies to human cytochrome P450 enzymes: a new avenue for drug discovery” . Trends in Pharmacological Sciences 20 (11): 432–8. doi :10.1016/S0165-6147(99)01382-6 . PMID 10542439 . http://www.cell.com/trends/pharmacological-sciences/comments/S0165-6147(99)01382-6 . ^ Tansey EM, Catterall PP (July 1994). “Monoclonal antibodies: a witness seminar in contemporary medical history” . Medical History 38 (3): 322–7. doi :10.1017/s0025727300036632 . PMC 1036884 . PMID 7934322 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1036884/ . ^ Schwaber J, Cohen EP (August 1973). “Human x mouse somatic cell hybrid clone secreting immunoglobulins of both parental types”. Nature 244 (5416): 444–7. doi :10.1038/244444a0 . PMID 4200460 . ^ Cambrosio A, Keating P (1992). “Between fact and technique: the beginnings of hybridoma technology”. Journal of the History of Biology 25 (2): 175–230. doi :10.1007/BF00162840 . PMID 11623041 . ^ a b c “The Story of César Milstein and Monoclonal Antibodies ”. WhatisBiotechnology.org . 23 September 2020 閲覧 えつらん
^ Riechmann L, Clark M, Waldmann H, Winter G (March 1988). “Reshaping human antibodies for therapy”. Nature 332 (6162): 323–7. Bibcode : 1988Natur.332..323R . doi :10.1038/332323a0 . PMID 3127726 . ^ Altmann DM (November 2018). “A Nobel Prize-worthy pursuit: cancer immunology and harnessing immunity to tumour neoantigens” . Immunology 155 (3): 283–284. doi :10.1111/imm.13008 . PMC 6187215 . PMID 30320408 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6187215/ . ^ Yang J1, Shen MH. Polyethylene glycol-mediated cell fusion. Methods Mol Biol. 2006; 325:59-66.
^ National Research Council (US) Committee on Methods of Producing Monoclonal Antibodies. Recommendation 1: Executive Summary : Monoclonal Antibody Production. Washington (DC): National Academies Press (US); 1999. ISBN 978-0-309-07511-4
^ a b Ho M, Feng M, Fisher RJ, Rader C, Pastan I (May 2011). “A novel high-affinity human monoclonal antibody to mesothelin” . International Journal of Cancer 128 (9): 2020–30. doi :10.1002/ijc.25557 . PMC 2978266 . PMID 20635390 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2978266/ .
^ Seeber S, Ros F, Thorey I, Tiefenthaler G, Kaluza K, Lifke V, Fischer JA, Klostermann S, Endl J, Kopetzki E, Pashine A, Siewe B, Kaluza B, Platzer J, Offner S (2014). “A robust high throughput platform to generate functional recombinant monoclonal antibodies using rabbit B cells from peripheral blood” . PLOS ONE 9 (2): e86184. Bibcode : 2014PLoSO...986184S . doi :10.1371/journal.pone.0086184 . PMC 3913575 . PMID 24503933 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3913575/ . ^ Wardemann H, Yurasov S, Schaefer A, Young JW, Meffre E, Nussenzweig MC (September 2003). “Predominant autoantibody production by early human B cell precursors”. Science 301 (5638): 1374–7. Bibcode : 2003Sci...301.1374W . doi :10.1126/science.1086907 . PMID 12920303 . ^ Koelsch K, Zheng NY, Zhang Q, Duty A, Helms C, Mathias MD, Jared M, Smith K, Capra JD, Wilson PC (June 2007). “Mature B cells class switched to IgD are autoreactive in healthy individuals” . The Journal of Clinical Investigation 117 (6): 1558–65. doi :10.1172/JCI27628 . PMC 1866247 . PMID 17510706 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1866247/ . ^ Smith K, Garman L, Wrammert J, Zheng NY, Capra JD, Ahmed R, Wilson PC (2009-01-01). “Rapid generation of fully human monoclonal antibodies specific to a vaccinating antigen” . Nature Protocols 4 (3): 372–84. doi :10.1038/nprot.2009.3 . PMC 2750034 . PMID 19247287 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2750034/ . ^ Duty JA, Szodoray P, Zheng NY, Koelsch KA, Zhang Q, Swiatkowski M, Mathias M, Garman L, Helms C, Nakken B, Smith K, Farris AD, Wilson PC (January 2009). “Functional anergy in a subpopulation of naive B cells from healthy humans that express autoreactive immunoglobulin receptors” . The Journal of Experimental Medicine 206 (1): 139–51. doi :10.1084/jem.20080611 . PMC 2626668 . PMID 19103878 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2626668/ . ^ Huang J, Doria-Rose NA, Longo NS, Laub L, Lin CL, Turk E, Kang BH, Migueles SA, Bailer RT, Mascola JR, Connors M (October 2013). “Isolation of human monoclonal antibodies from peripheral blood B cells” . Nature Protocols 8 (10): 1907–15. doi :10.1038/nprot.2013.117 . PMC 4844175 . PMID 24030440 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4844175/ . ^ a b c Ho M (June 2018). “Inaugural Editorial: Searching for Magic Bullets” . Antibody Therapeutics 1 (1): 1–5. doi :10.1093/abt/tby001 . PMC 6086361 . PMID 30101214 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6086361/ .
^ Vlasak J, Ionescu R (December 2008). “Heterogeneity of monoclonal antibodies revealed by charge-sensitive methods”. Current Pharmaceutical Biotechnology 9 (6): 468–81. doi :10.2174/138920108786786402 . PMID 19075686 . ^ Beck A, Wurch T, Bailly C, Corvaia N (May 2010). “Strategies and challenges for the next generation of therapeutic antibodies”. Nature Reviews. Immunology 10 (5): 345–52. doi :10.1038/nri2747 . PMID 20414207 . ^ Khawli LA, Goswami S, Hutchinson R, Kwong ZW, Yang J, Wang X, Yao Z, Sreedhara A, Cano T, Tesar D, Nijem I, Allison DE, Wong PY, Kao YH, Quan C, Joshi A, Harris RJ, Motchnik P (2010). “Charge variants in IgG1: Isolation, characterization, in vitro binding properties and pharmacokinetics in rats” . mAbs 2 (6): 613–24. doi :10.4161/mabs.2.6.13333 . PMC 3011216 . PMID 20818176 . http://www.landesbioscience.com/journals/mabs/abstract.php?id=13333 . ^ Zhang T, Bourret J, Cano T (August 2011). “Isolation and characterization of therapeutic antibody charge variants using cation exchange displacement chromatography”. Journal of Chromatography A 1218 (31): 5079–86. doi :10.1016/j.chroma.2011.05.061 . PMID 21700290 . ^ Rathore AS, Winkle H (January 2009). “Quality by design for biopharmaceuticals”. Nature Biotechnology 27 (1): 26–34. doi :10.1038/nbt0109-26 . PMID 19131992 . ^ van der Schoot JM, Fennemann FL, Valente M, Dolen Y, Hagemans IM, Becker AM, Le Gall CM, van Dalen D, Cevirgel A, van Bruggen JA, Engelfriet M, Caval T, Bentlage AE, Fransen MF, Nederend M, Leusen JH, Heck AJ, Vidarsson G, Figdor CG, Verdoes M, Scheeren FA (August 2019). “Functional diversification of hybridoma-produced antibodies by CRISPR/HDR genomic engineering” . Science Advances 5 (8): eaaw1822. doi :10.1126/sciadv.aaw1822 . PMC 6713500 . PMID 31489367 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6713500/ . ^ Siegel DL (January 2002). “Recombinant monoclonal antibody technology”. Transfusion Clinique et Biologique 9 (1): 15–22. doi :10.1016/S1246-7820(01)00210-5 . PMID 11889896 . ^ “Dr. George Pieczenik ”. LMB Alumni . MRC Laboratory of Molecular Biology (LMB) (17 September 2009). 23 December 2012時 じ 点 てん オリジナル よりアーカイブ。17 November 2012 閲覧 えつらん ^ Schmitz U, Versmold A, Kaufmann P, Frank HG (2000). “Phage display: a molecular tool for the generation of antibodies--a review”. Placenta 21 Suppl A (Suppl A): S106-12. doi :10.1053/plac.1999.0511 . PMID 10831134 . ^ Boulianne GL, Hozumi N, Shulman MJ (1984). “Production of functional chimaeric mouse/human antibody”. Nature 312 (5995): 643–6. doi :10.1038/312643a0 . PMID 6095115 . ^ Chadd HE, Chamow SM (April 2001). “Therapeutic antibody expression technology”. Current Opinion in Biotechnology 12 (2): 188–94. doi :10.1016/S0958-1669(00)00198-1 . PMID 11287236 . ^ Lonberg N, Huszar D (1995). “Human antibodies from transgenic mice”. International Reviews of Immunology 13 (1): 65–93. doi :10.3109/08830189509061738 . PMID 7494109 . ^ “Bristol-Myers Squibb Bets Big on a Mouse ”. Bloomberg.com . Bloomberg L.P.. 2021年 ねん 月 がつ 日 にち 閲覧 えつらん ^ “Amgen Completes Acquisition of Abgenix; Acquisition Provides Amgen with Full Ownership of Panitumumab and Eliminates a Denosumab Royalty | Amgen Inc. ”. investors.amgen.com . 2021年 ねん 月 がつ 日 にち 閲覧 えつらん ^ “Archived copy ”. June 29, 2009時 じ 点 てん オリジナル よりアーカイブ。July 28, 2009 閲覧 えつらん ^ “Proprietary antibody platform ”. 2013年 ねん 月 がつ 日 にち 時点 じてん オリジナル よりアーカイブ。2013年 ねん 月 がつ 日 にち 閲覧 えつらん ^ “Naturally optimized human antibodies ”. 2013年 ねん 日 にち 時点 じてん オリジナル よりアーカイブ。2021年 ねん 月 がつ 日 にち 閲覧 えつらん ^ “Ligand to Acquire OMT, Inc., a Leader in Human Antibody Generation, for $178 Million in Cash and Stock :: Ligand Pharmaceuticals Incorporated (LGND) ”. investor.ligand.com . 2021年 ねん 月 がつ 日 にち 閲覧 えつらん ^ “Proprietary antibody platform ”. 2021年 ねん 月 がつ 日 にち 閲覧 えつらん ^ “Proprietary antibody platform ”. 2021年 ねん 月 がつ 日 にち 閲覧 えつらん ^ McCafferty J, Griffiths AD, Winter G, Chiswell DJ (December 1990). “Phage antibodies: filamentous phage displaying antibody variable domains”. Nature 348 (6301): 552–4. Bibcode : 1990Natur.348..552M . doi :10.1038/348552a0 . PMID 2247164 . ^ Marks JD, Hoogenboom HR, Bonnert TP, McCafferty J, Griffiths AD, Winter G (December 1991). “By-passing immunization. Human antibodies from V-gene libraries displayed on phage”. Journal of Molecular Biology 222 (3): 581–97. doi :10.1016/0022-2836(91)90498-U . PMID 1748994 . ^ Carmen S, Jermutus L (July 2002). “Concepts in antibody phage display”. Briefings in Functional Genomics & Proteomics 1 (2): 189–203. doi :10.1093/bfgp/1.2.189 . PMID 15239904 . ^ Osbourn JK (2002). “Proximity-guided (ProxiMol) antibody selection”. Antibody Phage Display . Methods Mol. Biol.. 178 . pp. 201–5. doi :10.1385/1-59259-240-6:201 . ISBN 978-1-59259-240-1 . PMID 11968489 ^ Abeloff MD, Armitage JO, Niederhuber JE, Kastan MB, McKenna G (2008). “Therapeutic Antibodies and Immunologic Conjugates”. Abeloff's Clinical Oncology (4th ed.). Elsevier ^ “Cambridge Antibody Technology ”. 2011年 ねん 月 がつ 日 にち 時点 じてん オリジナル よりアーカイブ。2021年 ねん 月 がつ 日 にち 閲覧 えつらん ^ Osbourn JK, Derbyshire EJ, Vaughan TJ, Field AW, Johnson KS (January 1998). “Pathfinder selection: in situ isolation of novel antibodies”. Immunotechnology 3 (4): 293–302. doi :10.1016/S1380-2933(97)10007-0 . PMID 9530562 . ^ “The Current State of Proteomic Technology ”. 2011年 ねん 月 がつ 日 にち 時点 じてん オリジナル よりアーカイブ。2009年 ねん 月 がつ 日 にち 閲覧 えつらん ^ PhRMA Reports Identifies More than 400 Biotech Drugs in Development. Pharmaceutical Technology, August 24, 2006. Retrieved 2006-09-04.^ Hernandez I, Bott SW, Patel AS, Wolf CG, Hospodar AR, Sampathkumar S, Shrank WH (February 2018). “Pricing of monoclonal antibody therapies: higher if used for cancer?”. The American Journal of Managed Care 24 (2): 109–112. PMID 29461857 . ^ Breedveld FC (February 2000). “Therapeutic monoclonal antibodies” . Lancet 355 (9205): 735–40. doi :10.1016/S0140-6736(00)01034-5 . PMID 10703815 . http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(00)01034-5/fulltext . ^ Australian Prescriber (2006). “Monoclonal antibody therapy for non-malignant disease” . Australian Prescriber 29 (5): 130–133. doi :10.18773/austprescr.2006.079 . http://www.australianprescriber.com/magazine/29/5/130/3/#2 . ^ Modified from Carter P (November 2001). “Improving the efficacy of antibody-based cancer therapies”. Nature Reviews. Cancer 1 (2): 118–29. doi :10.1038/35101072 . PMID 11905803 .
^ Takimoto CH, Calvo E. (January 01, 2005) "Principles of Oncologic Pharmacotherapy" in Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (Eds) Cancer Management
^ a b c d e f g h i j Rang HP (2003). Pharmacology . Edinburgh: Churchill Livingstone. pp. 241, for the examples infliximab, basiliximab, abciximab, daclizumab, palivusamab, gemtuzumab, alemtuzumab and rituximab, and mechanism and mode. ISBN 978-0-443-07145-4
^ a b Staff, Adis Insight. Bavituximab profile Last updated Jan 27 2016
^ "Coronavirus (COVID-19) Update: FDA Authorizes Monoclonal Antibodies for Treatment of COVID-19" . U.S. Food and Drug Administration (FDA) (Press release). 21 November 2020. 2020年 ねん 日 にち 閲覧 えつらん 。この記述 きじゅつ アメリカ合衆国 あめりかがっしゅうこく 内 うち パブリックドメイン となっている記述 きじゅつ 含 ふく ^ "FDA Authorizes Monoclonal Antibodies for Treatment of COVID-19" . U.S. Food and Drug Administration (FDA) (Press release). 10 February 2021. 2021年 ねん 月 がつ 日 にち 閲覧 えつらん 。この記述 きじゅつ アメリカ合衆国 あめりかがっしゅうこく 内 うち パブリックドメイン となっている記述 きじゅつ 含 ふく ^ “Monoclonal antibodies to treat cancer | American Cancer Society ”. www.cancer.org . 2018年 ねん 月 がつ 日 にち 閲覧 えつらん ^ “Monoclonal antibody drugs for cancer: How they work” . Mayo Clinic . https://www.mayoclinic.org/diseases-conditions/cancer/in-depth/monoclonal-antibody/art-20047808 2018年 ねん 月 がつ 日 にち 閲覧 えつらん ^ a b “Monoclonal Antibodies: List, Types, Side Effects & FDA Uses (Cancer)” . MedicineNet . https://www.medicinenet.com/monoclonal_antibodies/article.htm#what_drugs_or_other_compounds_interact_with_monoclonal_antibodies ? 2018年 ねん 月 がつ 日 にち 閲覧 えつらん





 この
この この
この